
科目: 来源: 题型:
【题目】已知:氯化铁易潮解.如图是制取无水氯化铁的实验装置图,将分液漏斗中的浓盐酸加入到盛有二氧化锰的烧瓶中,请回答下列问题: 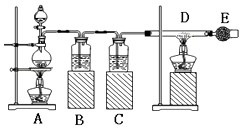
(1)烧瓶中发生反应的化学方程式是;
(2)B瓶中的溶液是;C瓶中的溶液是 .
(3)玻璃管D中发生反应的化学方程式为 .
(4)干燥管E中盛有碱石灰,其作用是(回答一点即可).
查看答案和解析>>
科目: 来源: 题型:
【题目】在科学史上每一次重大的发现都极大地推进了科学的发展。俄国科学家门捷列夫对化学的突出贡献在于
A. 开发了合成氨的生产工艺
B. 提出了元素周期律
C. 揭示了燃烧的本质
D. 提取了治疟药物青蒿素
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 水玻璃、漂白粉、胆矾均为混合物
B. 碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物
C. 能电离出H+的物质属于酸
D. 酸性氧化物一定不能与酸起反应
查看答案和解析>>
科目: 来源: 题型:
【题目】对燃煤烟气和汽车尾气进行脱硝、脱碳和脱硫等处理,可实现绿色环保、节能减排等目的.汽车尾气脱硝脱碳的主要原理为:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)△H=a kJmol﹣1 .
N2(g)+2CO2(g)△H=a kJmol﹣1 .
(1)已知:2NO(g)+O2(g)=2NO2(g)△H=b kJmol﹣1;CO的燃烧热为c kJmol﹣1 . 写出消除汽车尾气中NO2的污染时,NO2与CO反应的热化学方程式 .
(2)一定条件下,在一密闭容器中,用传感器测得该反应在不同时间的NO和CO浓度如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/molL﹣1 | 1.00 | 0.8 | 0.64 | 0.55 | 0.5 | 0.5 |
c(CO)/molL﹣1 | 3.50 | 3.30 | 3.14 | 3.05 | 3.00 | 3.00 |
①在恒容密闭容器中充入CO,NO气体,下列图象如图1正确且能说明反应达到平衡状态的是 . 
②前2s内的平均反应速率υ(N2)=mol/(Ls)(保留两位小数,下同);此温度下,该反应的平衡常数为 .
③采用低温臭氧氧化脱硫脱硝技术,同时吸收SO2和NOx , 获得(NH4)2SO4的稀溶液.已知常温下,该溶液的PH=5,则 ![]() =(已知该温度下NH3H2O的Kb=1.7×10﹣5).若向此溶液中再加入少量 (NH4)2SO4固体,
=(已知该温度下NH3H2O的Kb=1.7×10﹣5).若向此溶液中再加入少量 (NH4)2SO4固体, ![]() 的值将(填“变大”、“不变”或“变小”).
的值将(填“变大”、“不变”或“变小”).
(3)如图2所示,用无摩擦、无质量的活塞1、2将反应器隔成甲、乙两部分,在25℃和101kPa下达到平衡时,各部分体积分别为V甲、V乙 . 此时若去掉活塞1,不引起活塞2的移动.则x= , V甲:V乙= .
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上常以烃的含氧衍生物X为主要原料生产可降解塑料PCL{ ![]() }及阻燃剂四溴双酚A.合成线路如下:
}及阻燃剂四溴双酚A.合成线路如下: 
已知:①X的蒸汽密度是相同条件下H2的47倍,遇FeCl3溶液显紫色;C为 ![]()
② ![]()
![]()
![]()
③RCOCH2R′ ![]() RCOOCH2R′
RCOOCH2R′
请回答下列问题:
(1)X的分子式为;B的名称是 .
(2)B→C还需要的反应试剂及条件是 . C→D的反应类型是 .
(3)写出X→Y的化学方程式: .
(4)0.5mol四溴双酚A在一定条件下与足量的NaOH溶液反应,最多消耗molNaOH.
(5)符合以下条件的D的同分异构体有种(不考虑空间异构).
①含有两个甲基和两种官能团 ②能使溴的CCl4溶液褪色 ③能发生银镜反应
(6)已知由烯烃直接制备不饱和酯的新方法为:
2CH3![]() =CH2+2ROH+2CO+O2
=CH2+2ROH+2CO+O2 ![]() 2CH3
2CH3![]() =CHCOOR+2H2O
=CHCOOR+2H2O
利用乙烯为有机原料(无机物和反应条件自选)合成聚合物涂料 ![]() ,写出合成该涂料的反应流程图: .
,写出合成该涂料的反应流程图: .
查看答案和解析>>
科目: 来源: 题型:
【题目】用适当的化学用语来表示下列反应原理
(1)氢氧化亚铁放置于空气中,颜色发生改变,有关化学方程式:;
(2)小苏打溶于水,其电离方程式:;
(3)铁红中铁的化合价为: , 它与盐酸反应的离子方程式为;
(4)明矾[KAl(SO4)212H2O]能净水是由于其溶于水后生成了(写化学式);
(5)工业上制取漂白液,有关离子方程式并用双线桥标明电子得失: .
查看答案和解析>>
科目: 来源: 题型:
【题目】“甲型H1N1”流感疫情已构成“具有国际影响的公共卫生紧急事态”.已知扎那米韦是流感病毒神经氨酸酶抑制剂,其对流感病毒的抑制是以慢结合的方式进行的,具有高度特异性,其分子结构如图所示.下列说法正确的是( ) 
A.该物质的分子式为C12H20N4O7
B.1mol该物质与NaOH溶液反应,可以消耗4molNaOH
C.在一定条件下,该物质可以发生消去、加成、取代等反应
D.该物质能使溴水或高锰酸钾溶液褪色,能与FeCl3溶液发生显色反应
查看答案和解析>>
科目: 来源: 题型:
【题目】第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物.
(1)①H、C、N、O四种元素的电负性由小到大的顺序为 .
②下列叙述不正确的是 . (填字母)
a.因为HCHO与水分子间能形成氢键,所以HCHO易溶于水
b.HCHO和CO2分子中的中心原子均采用sp2杂化
c.C6H6分子中含有6个σ键和1个大π键,C2H2是非极性分子
d.CO2晶体的熔点、沸点都比二氧化硅晶体的低
③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式 .
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是
②六氰合亚铁离子[Fe(CN)6]4﹣中不存在 .
A.共价键 B.非极性键 C.配位键 D.σ键 E.π键
写出一种与 CN﹣互为等电子体的单质分子式 .
(3)根据元素原子的外围电子排布特征,可将周期表分成五个区域,其中Ti属于区.
(4)一种Al﹣Fe合金的立体晶胞如图所示.请据此回答下列问题: 
①确定该合金的化学式 .
②若晶体的密度=ρ g/cm3 , 则此合金中最近的两个Fe原子之间的距离 (用含ρ的代数式表示,不必化简)为cm.
查看答案和解析>>
科目: 来源: 题型:
【题目】根据题意解答
(1)工业上制取硝酸的主要流程图如图1: 
(I)工业合成氨的原料是N2和H2 . 装置A的名称是;其中N2可从空气中分离出来,方法是先将空气 , 然后即可得到;H2可以水和天然气为原料在催化剂作用下高温制取,其化学方程式为 .
(II)在原料气制备过程中混有的CO对催化剂有毒害作用,欲除去原料气中的CO,可通过如下反应:CO(g)+H2O(g)═CO2(g)+H2(g)来实现.已知1100K时该反应的平衡常数K=0.64,若要使CO的转化率超过80%,则起始物中c(H2O):c(CO)不低于 .
(2)利用石灰乳来除去硝酸工业的尾气(含NO、NO2),既能净化尾气,又能获得应用广泛的Ca(NO2)2 , 其部分工艺流程如图2.已知NO和NO2按1:1通入碱液中生成亚硝酸盐. 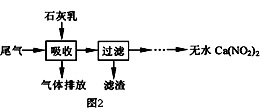
(I)上述工艺中采用气﹣液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),其目的是;滤渣可循环使用,滤渣的主要成分是(填化学式).
(II)该工艺需控制NO 和NO2 物质的量之比接近1:1.若n(NO):n(NO2)>1:1,则会导致;若n(NO):n(NO2)<1:1,则会导致 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com