
科目: 来源: 题型:
【题目】按要求写出方程式.
(1)碳酸氢铵溶液中加入过NaOH溶液,并加热(写出离子方量程式) .
(2)已知4℃时四种化合物在水中和液氨中的溶解度如表:
AgNO3 | Ba(NO3)2 | AgCl | BaCl2 | |
H2O (液) | 170g | 9.2g | 1.5×10﹣4g | 33.3g |
NH3(液) | 86g | 97.2g | 0.8g | 0g |
上述四种物质在水中形成复分解反应的离子方程式为 , 在液氨中发生复分解反应的化学方程式为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关分散系的叙述中,不正确的是
A.胶体区别于其他分散系伪本质特征是胶体粒子的直径大小在1nm~100nm之间
B.区别Fe(OH)3胶体和FeCl3溶液可利用胶体具有丁达尔效应
C.溶液很稳定,胶体、悬浊液和乳浊液均不稳定
D.溶液、胶体的分散质的粒子能透过滤纸,悬浊液的分散质的粒子不能透过滤纸
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是( )
A.在原电池的负极和电解池的阴极上都发生失电子的氧化反应
B.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2
C.用惰性电极电解饱和NaCl溶液,若有0.1 mol电子转移,则生成0.1 mol NaOH
D.镀层破损后,镀锌铁板比镀锡铁板更易腐蚀
查看答案和解析>>
科目: 来源: 题型:
【题目】在MgCl2、KCl、K2SO4三种盐的混合溶液中,若K+、Cl-各为1.5mol/L,Mg2+为0.5mol/L,则SO42-的物质的量浓度为( )
A. 0.1mol/LB. 0.5mol/LC. 0.15mol/LD. 0.25mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】某气态烃1体积只能与1体积Br2发生加成反应,生成溴代烷,此溴代烷1 mol可与4 mol Cl2发生完全取代反应,则该烃的结构简式为( )
A. CH2=CH2B. CH3CH=CH2C. CH3CH3D. CH2=CHCH=CH2
查看答案和解析>>
科目: 来源: 题型:
【题目】用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂﹣KNO3的U形管)构成一个原电池(如图).以下有关该原电池的叙述正确的是
①在外电路中,电子由铜电极流向银电极
②正极反应为:Ag++e﹣=Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同( )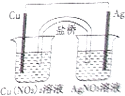
A.①②
B.①②④
C.②③
D.①③④
查看答案和解析>>
科目: 来源: 题型:
【题目】为验证卤素单质氧化性的相对强弱,某小组用如图所示装置进行实验(夹持仪器已略去,气密性已检验). 
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸.
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹.
Ⅲ.当B中溶液由黄色变为棕色时,关闭活塞a.
Ⅳ.…
(1)A中产生的是黄绿色气体,其电子式是 , 在该反应中浓盐酸表现了性和性.
(2)验证氯气的氧化性强于碘的实验现象是 .
(3)B中溶液发生反应的离子方程式是 .
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是 .
(5)过程Ⅲ实验的目的是 .
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下 , 得电子能力逐渐减弱.
查看答案和解析>>
科目: 来源: 题型:
【题目】四种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
X | Y | |
Z | W |
请回答下列问题:
(1)元素Z位于周期表中的位置;
(2)这些元素的氢化物中,水溶液碱性最强的是(写化学式);
(3)XW2的电子式为;
(4)Y的最高价氧化物的化学式为;
(5)W和Y形成的一种二元化合物具有色温效应,其相对分子质量在170~190之间,且W的质量分数约为70%.该化合物的化学式为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质间的反应,其能量变化符合如图所示的是( ) 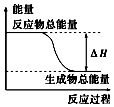
A.铝粉与氧化铁在加热条件下的反应
B.灼热的碳与二氧化碳反应
C.Ba(OH)28H2O晶体和NH4Cl晶体混合
D.碳与水高温条件下制取水煤气的反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com