
科目: 来源: 题型:
【题目】已知NaHSO2溶液在不同温度下均可被过量KlO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率.将浓度均为0.020 molL﹣1的NaHSO3溶液(含少量淀粉)10.0 mL、KIO3(过量)酸性溶液40.0 mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下列判断不正确的是( ) 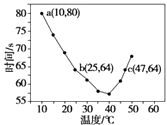
A.40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反
B.图中a点对应的NaHSO3反应速率为5.0×10﹣5 molL﹣1s﹣1
C.图中b、c两点对应的NaHSO3反应速率相等
D.40℃之后,淀粉不宜用作该实验的指示剂
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质中所含分子物质的量最多的是( )
A. 56 g N2 B. 标准状况下3.36 L O2
C. 6 g H2 D. 3.01×1023个H2SO4分子
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值.下列说法不正确的是( )
A.常温常压下,8 g O2含有4NA个电子
B.盛有SO2的密闭容器中含有NA个氧原子,则SO2的物质的量为0.5 mol
C.常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA
D.常温常压下,22.4 L的NO2和CO2混合气体含有2NA个O原子
查看答案和解析>>
科目: 来源: 题型:
【题目】下面是用98%的浓H2SO4(ρ=1.84g/cm3)配制成0.5mol/L的稀H2SO4 500mL的操作,请按要求填空:
(1)用量筒量取所需浓H2SO4的体积为
(2)如果实验室有15mL、20mL、50mL量筒,应选用mL量筒最好.量取时发现量筒不干净,用水洗净后直接量取,所配溶液浓度将(填偏高、偏低、无影响).
(3)将量取的浓H2SO4沿烧杯内壁慢慢注入盛有约100mL水的里,并不断搅拌,目的是
(4)将冷却后的上述溶液沿注入中,并用50mL蒸馏水洗涤烧杯次,洗涤液也要注入容量瓶中,并摇匀.如未冷却就转移,则所配溶液的浓度会(填偏高、偏低或无影响);若未洗涤烧杯,则所配溶液的浓度会(填偏高、偏低或无影响).
(5)加水至液面距刻度线下时,改用加水,使溶液的 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式中正确的是( )
A.向硫酸铜蓝色溶液中加入BaCl2溶液:Ba2++SO42﹣═BaSO4↓
B.碳酸氢钙溶液跟盐酸反应:Ca(HCO3)2+2H+=Ca2++2H2O+2CO2↑
C.锌与盐酸的反应:Zn+2H++2Cl﹣═Zn2++2Cl﹣+H2↑
D.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O ![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
查看答案和解析>>
科目: 来源: 题型:
【题目】在下列三个化学反应中,按氮元素被氧化、被还原、既不被氧化又不被还原的顺序排列,正确的是( )
①N2+O2 ![]() 2NO
2NO
②4AgNO3 ![]() 2Ag2O+4NO2↑+O2↑
2Ag2O+4NO2↑+O2↑
③2NH4Cl+Ba(OH)2 ![]() BaCl2+2NH3↑+2H2O.
BaCl2+2NH3↑+2H2O.
A.①②③
B.②①③
C.③②①
D.③①②
查看答案和解析>>
科目: 来源: 题型:
【题目】以冶铝的废弃物铝灰为原料制取超细α﹣氧化铝,既降低环境污染又可提高铝资源的利用率.已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下: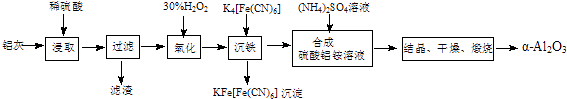
(1)铝灰中氧化铝与硫酸反应的化学方程式为
(2)用图中“滤渣”和NaOH焙烧制备硅酸钠,可采用的装置为(填选项编号).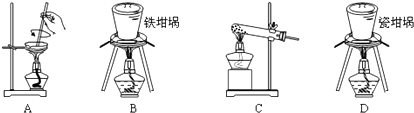
(3)在实验流程中,加30%的H2O2溶液发生的离子反应方程式为 .
(4)验证“沉铁”后,溶液中是否还含有铁离子的操作方法为 .
(5)若用调节pH溶液“沉铁”,则得到Fe(OH)3 , 已知:25℃时,Ksp[Fe(OH)3]=4.0×10﹣38 , 则该温度下反应Fe3++3H2OFe(OH)3+3H+的平衡常数为 .
(6)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)212H2O] ![]() 2Al2O3+2NH3↑+N2↑+
2Al2O3+2NH3↑+N2↑+
5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置.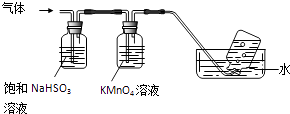
①集气瓶中收集到的气体是 (填化学式).
②KMnO4溶液褪色,发生的离子反应方程式为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com