
科目: 来源: 题型:
【题目】下列关于如图所示电化学装置的分析正确的是( ) 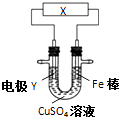
A.若X为直流电源,Y为铜棒接正极,则Fe棒上镀铜
B.若X为直流电源,Y为碳棒接负极,则Fe棒被保护
C.若X为电流计,Y为锌棒,则SO42﹣ 移向Fe棒
D.若X为导线,Y为铜棒,则Fe棒发生还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外活动小组学生模拟呼吸面具中的反应原理(过氧化钠与潮湿二氧化碳的反应)。
用如图所示仪器来制取氧气并测量氧气的体积。
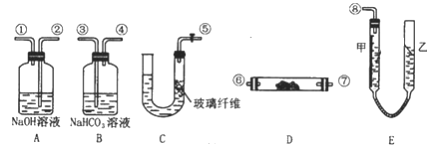
上图中的量气装置E是由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水。甲管有刻度(0~ 50mL),供量气用,乙管可上下移动,以调节液面高低。
实验室可供选用的药品还有:稀硫酸、稀盐酸、过氧化钠、碳酸钠、大理石、水。
(1)上述装置的连接顺序是(填各接口的編号,其中连接胶管及夹持装置均省略)____________。
(2)C 装置中放入的反应物是_________________________。
(3)装置A的作用是__________,装置B的作用是___________。
(4)为了较准确地测量氧气的体积,除了必须检查整个装置的气密性之外,在读取反应前后甲管中液面的读数并求其差值的过程中,需要注意___________。
A.视线与凹液面最低处平切。
B.待体系恢复至室温再读数。
C.上下移动乙管,使甲、乙两管内液面持平时再读数。
D.反应停止后立即读数。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)SO2与O2的混合气体中,氧元素的质量分数为70%,则SO2与O2的物质的量之比是__________,这种混合气体的密度是同温同压下氧气密度的_____倍。
(2)某气态氧化物化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则R的摩尔质量为______________.
(3)在一定温度下,把mg相对分子质量为M的可溶性盐溶解在VmL水中(水的密度为1g·cm-3),恰好形成饱和溶液(密度为pg.cm-3),则该溶液中溶质的质量分数是____%,溶质的物质的量浓度是_________mol·L-1,该温度下此盐的溶解度是 _____g。
查看答案和解析>>
科目: 来源: 题型:
【题目】醋酸亚铬水合物{[Cr(CH3COO)2]22H2O,相对分子质量为376}是一种深红色晶体,不溶于冷水,是常用的氧气吸收剂,实验室中以锌粒,三氯化铬溶液、醋酸钠溶液和盐酸为主要原料制备醋酸亚铬水合物,其装置如图所示,且仪器2中预先加入锌粒,已知二价铬不稳定,极易被氧气氧化,不与锌反应.制备过程中发生的相关反应如下:
Zn(s)+2HCl(aq)═ZnCl2(aq)+H2(g)
2CrCl3(aq)+Zn(s)═2CrCl2(aq)+ZnCl2(aq)
2Cr2+(aq)+4CH3COO﹣(aq)+2H2O(l)═[Cr(CH3COO)2]22H2O(s)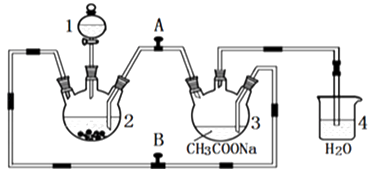
请回答下列问题:
(1)仪器1的名称是 .
(2)往仪器2中加盐酸和三氯化铬溶液的顺序最好是(选下面的A、B或C);目的是 .
A.盐酸和三氯化铬溶液同时加入 B.先加三氯化铬溶液一段时间后再加盐酸C.先加盐酸一段时间后再加三氯化铬溶液
(3)为使生成的CrCl2溶液与CH3COONa溶液顺利混合,应关闭阀门(填“A”或“B”,下同),打开阀门 .
(4)本实验中锌粒要过量,其原因除了让产生的H2将CrCl2溶液压入装置3与CH3COONa溶液反应外,另一个作用是 .
(5)已知其它反应物足量,实验时取用的CrCl3溶液中含溶质9.51g,取用的醋酸钠溶液为1.5L0.1mol/L;实验后得干燥纯净的[Cr(CH3COO)2]22H2O9.4g,则该实验所得产品的产率为(不考虑溶解的醋酸亚铬水合物).
(6)铬的离子会污染水,常温下要除去上述实验中多余的Cr2+ , 最好往废液中通入足量的,再加入碱液,调节pH至少为才能使铬的离子沉淀完全(铬的离子浓度应小于10﹣5mol/L).【已知Cr(OH)3的溶度积为6.3×10﹣31 , ![]() ≈4,lg2≈0.3】
≈4,lg2≈0.3】
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质转化过程为吸热的是
A. 生石灰与水作用制熟石灰B. 食物因氧化而腐败
C. Ba(OH)2·8H2O与NH4Cl晶体混合D. 盐酸与氢氧化钠混合
查看答案和解析>>
科目: 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是一种食品添加剂.实验室用如图1所示装置制备Na2S2O5 , 实验步骤如下: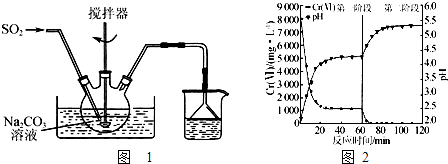
Ⅰ.在Na2CO3溶液中通入SO2至pH为4.1,生成NaHSO3溶液;
Ⅱ.加碳酸钠粉末调至pH为7~8;
Ⅲ.再通SO2至pH为4.1;
Ⅳ.从过饱和溶液中析出Na2S2O5晶体.
(1)制备焦亚硫酸钠总反应的化学方程式为 .
(2)Na2S2O5溶于水且与水能反应,所得溶液显酸性,其原因是 . 步骤Ⅲ中测定溶液的pH的方法是;pH>4.1时,则产品中会有副产物,其化学式是 .
(3)利用碘量法可测定Na2S2O5产品中+4价硫的含量,实验方案为:将一定量的Na2S2O5产品放入碘量瓶(带磨口塞的锥形瓶)中, , 重复如上步骤2次,记录数据.(实验中必须使用的试剂有:c1molL﹣1的标准碘溶液、c2molL﹣1的标准Na2S2O3溶液、冰醋酸、淀粉溶液、蒸馏水;已知:2Na2S2O3+I2═Na2S4O6+2NaI)
(4)含铬废水中常含有六价铬[Cr(Ⅵ)].利用Na2S2O5和FeSO47H2O先后分两个阶段处理含Cr2O72﹣的废水,实验结果见右图.
①实验过程中溶液的pH不断升高的原因是 .
②已知:Ksp[Cr(OH)3]=6.4×10﹣31 , lg2≈0.3,c(Cr3+)<1.0×10﹣5 molL﹣1时视为完全沉淀.现将废水中Cr2O72﹣全部转化为Cr(OH)3而除去,需调节溶液的pH范围为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛.回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar] , 有个未成对电子.
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键.从原子结构角度分析,原因是 .
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因
GeCl4 | GeBr4 | GeI4 | |
熔点/℃ | ﹣49.5 | 26 | 146 |
沸点/℃ | 83.1 | 186 | 约400 |
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂.Zn、Ge、O电负性由大至小的顺序是 .
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为 , 微粒之间存在的作用力是 .
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ![]() ,0,
,0, ![]() ),C为(
),C为( ![]() ,
, ![]() ,0).则D原子的坐标参数为 .
,0).则D原子的坐标参数为 .
②晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数a=565.76pm,其密度为gcm﹣3(列出计算式即可).
查看答案和解析>>
科目: 来源: 题型:
【题目】丙烯腈(CH2=CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH2=CHCHO)和乙腈(CH3CN)等,回答下列问题:
(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的热化学方程式如下:
C3H6(g)+NH3(g)+ ![]() O2(g)=C3H3N(g)+3H2O(g)△H=﹣515kJ/mol
O2(g)=C3H3N(g)+3H2O(g)△H=﹣515kJ/mol
C3H6(g)+O2(g)=C3H4O(g)+H2O(g)△H=﹣353kJ/mol
两个反应在热力学上趋势均很大,其原因是;有利于提高丙烯腈平衡产率的反应条件是;提高丙烯腈反应选择性的关键因素是 .
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应温度为460℃.低于460℃时,丙烯腈的产率(填“是”或者“不是”)对应温度下的平衡
产率,判断理由是;高于460℃时,丙烯腈产率降低的可能原因是(双选,填标号)
A.催化剂活性降低 B.平衡常数变大 C.副反应增多 D.反应活化能增大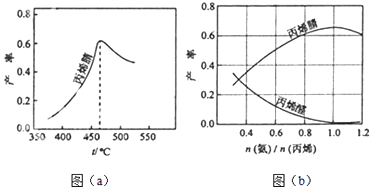
(3)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图(b)所示.由图可知,最佳n(氨)/n(丙烯)约为 , 理由是 . 进料气氨、空气、丙烯的理论体积比约为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com