
科目: 来源: 题型:
【题目】以下对化学反应描述的观点中正确的有几项:①放热反应在常温下均能自发进行;②电解过程中,化学能转化为电能而“储存”起来;③原电池工作时所发生的反应一定有氧化还原反应;④加热时,化学反应只向吸热反应方向进行;⑤盐类均能发生水解反应;⑥相同温度下,同一反应的化学平衡常数的大小与化学反应方程式的书写有关.( )
A.1项
B.2项
C.3项
D.4项
查看答案和解析>>
科目: 来源: 题型:
【题目】2015年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.
(1)汽车尾气净化的主要原理为:2NO(g)+2CO (g) ![]() 2CO2 (g)+N2 (g)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图1所示.
2CO2 (g)+N2 (g)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图1所示. 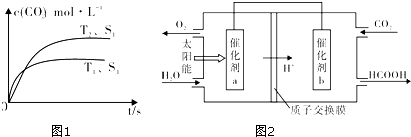
据此判断:
①该反应的平衡常数表达式为 .
②该反应的△H0(选填“>”、“<”).
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率.若催化剂的表面积S1>S2 , 在右图中画出c(CO2)在T2、S2条件下达到平衡过程中的变化曲线.
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题.
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染.
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=﹣867kJmol﹣1
2NO2(g)N2O4(g)△H=﹣56.9kJmol﹣1
写出CH4催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(g)的热化学方程式 .
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的.图2是通过光电转化原理以廉价原料制备新产品的示意图.写出上述光电转化过程的化学反应方程式 . 催化剂a、b之间连接导线上电子流动方向是(填a→b或b→a).
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关热化学方程式的叙述正确的是( )
A.已知2H2 (g)+O2(g)═2H2O(g)△H=﹣483.6kJ/mol,则氢气的燃烧热为241.8kJ/mol
B.含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=﹣57.4kJ/mol
C.已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定
D.已知C (s)+O2(g)═CO2(g)△H1;C(s)+1/2 O2(g)═CO(g)△H2 , 则△H1>△H2
查看答案和解析>>
科目: 来源: 题型:
【题目】由硫酸钾、硫酸铝和硫酸组成的混合溶液,其中c(H+)=0.1mol/L,c(Al3+)=0.4mol/L,c(SO42﹣)=0.8mol/L,则c(K+)为( )
A. 0.15 mol/L B. 0.2 mol/L C. 0.3 mol/L D. 0.4 mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】判断下列反应的熵值的变化,在每小题后面的横线上填上“增加”“减小”或“无明显变化”。
(1)2H2(g)+O2(g)![]() 2H2O(l) 。
2H2O(l) 。
(2)H2(g)+Cl2(g)![]() 2HCl(g) 。
2HCl(g) 。
(3)(NH4)2CO3(s)![]() NH4HCO3(s)+NH3(g) 。
NH4HCO3(s)+NH3(g) 。
(4)Cu(s)+Cl2(g)![]() CuCl2(s) 。
CuCl2(s) 。
(5)将少量KNO3晶体溶解在水中 。
查看答案和解析>>
科目: 来源: 题型:
【题目】如下图所示,在图(1)中A、B两容器里分别收集着两种互不作用的理想气体。压强不变,若将中间活塞打开[如图(2)],两种气体分子立即都占满了两个容器。这是一个不伴随能量变化的自发过程。关于此过程的下列说法不正确的是( )
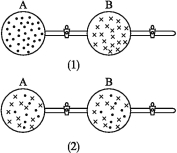
理想气体的自发混合
A.此过程为混乱程度小的向混乱程度大的方向进行的变化过程,即熵增大的过程
B.此过程为自发过程,而且没有热量的吸收或放出
C.此过程从有序到无序,混乱度增大
D.此过程是自发可逆的
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学教师为“氯气与金属钠反应”设计了如下装置与操作以替代相关的课本实验. 
实验操作:先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,并产生大量白烟.以下叙述错误的是( )
A.钠着火燃烧产生苍白色火焰
B.反应生成的大量白烟是氯化钠晶体
C.管中部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气
D.管右端棉球外颜色变化可判断氯气是否被碱液完全吸收
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求填空
(1)室温下,将0.15molL﹣1稀硫酸V1 mL与0.1molL﹣1 NaOH溶液V2 mL混合,所得溶液的pH为1,则V1:V2= . (溶液体积变化忽略不计)
(2)室温下,某水溶液中存在的离子有:Na+、A﹣、H+、OH﹣ , 根据题意,回答下列问题:
①若由0.1molL﹣1 HA溶液与0.1molL﹣1 NaOH溶液等体积混合而得,则溶液的pH7.
②若溶液pH>7,则c(Na+)c(A﹣),理由是
③若溶液由pH=3的HA溶液V1 mL与pH=11的NaOH溶液V2 mL混合而得,则下列说法正确的是(填选项代号).
A.若反应后溶液呈中性,则c(H+)+c(OH﹣)=2×10﹣7 molL﹣1
B.若V1=V2 , 反应后溶液的pH一定等于7
C.若反应后溶液呈酸性,则V1一定大于V2
D.若反应后溶液呈碱性,则V1一定小于V2 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com