
科目: 来源: 题型:
【题目】硒化锌是一种透明色半导体,也可作为红光外学材料,熔点1520℃.
(1)基态锌原子的价电子排布式是
(2)根据元素周期律,电负性SeS,第一电离能SeAs(填“>”或“<”)
(3)H2Se的分子构型是 , 其中Se的杂化轨道类型是 .
(4)H2O的沸点(100℃)高于H2Se的沸点(﹣42℃)其原因是 .
(5)晶体Zn为六方最密堆积,其配位数是 .
(6)ZnSe晶胞如图,假设阿伏伽德罗常数值为NA , 则144gZnSe晶体中的晶胞数是 . 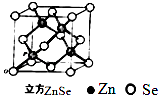
查看答案和解析>>
科目: 来源: 题型:
【题目】利用硫酸渣(主要含Fe2O3、FeO,杂质为Al2O3和SiO2等)生产铁基颜料铁黄(FeOOH) 的制备流程如图: 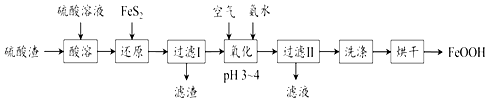
已知:FeS2难溶于水,不与H2SO4反应,在“还原”步骤中,Fe3+通过反应Ⅰ、Ⅱ被FeS2还原,其中反应Ⅰ为FeS2+14Fe3++8H2O═15Fe2++2SO42﹣+16H+;反应Ⅱ中氧化产物为单质硫.
(1)“酸溶”中硫酸要适当过量,目的是:①提高铁的浸出率;② .
(2)写出酸溶时硫酸渣中主要成分发生反应的一个化学方程式: .
(3)加入FeS2“还原”时反应Ⅱ的离子方程式为 . 滤渣的主要成分是FeS2、S和(填化学式)
(4)“氧化”时,生成FeOOH的离子方程式为 . 氧化时,温度不宜过高,否则会导致产品颜色偏红,可能含有的杂质是(填化学式).
(5)滤液中溶质是Al2(SO4)3和(填化学式).
查看答案和解析>>
科目: 来源: 题型:
【题目】分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可以采取多种分类方法。下列关于“Na2CO3”的分类不正确的是
A. 电解质B. 弱酸盐C. 强碱盐D. 碱性氧化物
查看答案和解析>>
科目: 来源: 题型:
【题目】氮及其化合物在生产、生活中有着重要的作用.请回答下列问题: 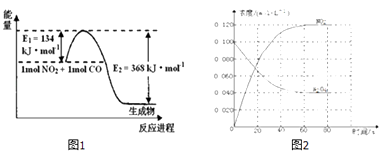
(1)图1是常温下1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:
(2)在恒温、恒容的密闭容器中,通入一定量的N2O4发生反应N2O4(g)2NO2(g)△H如图2
①在0﹣60s时段,反应速率v(N2O4)为molL﹣1s﹣1 .
②温度升高,混合气体的颜色变深,则△H0(填“>”或“<”).
③改变条件重新达到平衡时,要使N2O4的体积分数变大,可采取的措施有(填字母).
a.向混合气体中通入N2O4 b.升高温度
c.向混合气体中通入NO2 d.使用高效催化剂
(3)实验室可用NaOH溶液吸收NO2 , 反应2NO2+2NaOH=NaNO3+NaNO2+H2O.含0.2molNaOH的水溶液与0.2molNO2恰好完全反应得1L溶液A,溶液B为0.1molL﹣1的CH3COONa溶液.
①A、B两溶液中c(NO3﹣)、c(NO2﹣)和c(CH3COO﹣)由大到小的顺序为(已知HNO2的电离
常数Ka=7.1×10﹣4molL﹣1 , CH3COOH的电离常数Ka=1.7×10﹣5molL﹣1).
②可使A、B两溶液的PH相等的方法是(填字母).
a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
(4)铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O(方程式未配平).0.6molCu被硝酸完全溶解后,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】教材中给出了Na2O2与水反应的化学方程式,某学习小组通过实验研究Na2O2与水发反应机理
操作 | 现象 |
Ⅰ.向盛有4.0gNa2O2的烧杯中加入50mL蒸馏水 | 剧烈反应,产生的气体能使带火星木条复燃,固体全部溶解后,得到的无色溶液a |
Ⅱ.向溶液a中滴入两滴酚酞 | 溶液变红,10分钟后溶液颜色明显变浅,稍后,溶液变为无色 |
Ⅲ.向溶液中加入少量MnO2粉末 | 又有大量气泡产生,产生的气体也能使带火星木条复燃 |
(1)Na2O2的电子式为 , 很明显,实验证实了溶液a中H2O2的存在,应用同位素示踪原理可以表示反应的机理,写出Na218O2与H2O反应的化学方程式 .
(2)操作Ⅱ中红色褪去的可能原因是 .
(3)用反应2MnO4﹣+5H2O2+6H+=2Mn2++502↑+8H2O测定溶液a中H2O2含量.取20.00mL溶液a,用稀(填化学式)酸化,用0.002molL﹣1KMnO4溶液滴定,至终点时平均消耗10.00mLKMnO4溶液.滴定时KMnO4溶液应装在(填酸或碱)式滴定管中,终点确定的方法是 , 经计算溶液a中c(H2O2)=molL﹣1
(4)向溶液a中滴加FeSO4溶液,发生反应的离子方程式为 .
(5)向FeSO4溶液中加入一定量Na202固体,并以物质的量为2:1发生反应,反应中无气体生成,写出反应的离子方程式 .
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,下列有关电解质溶液的说法正确的是( )
A.向蒸馏水中加入Na2O,水的电离程度变小
B.向0.1mol?L﹣1的醋酸溶液中加水稀释后溶液中 ![]() 不变
不变
C.向0.1mol?L﹣1的醋酸溶液中加水稀释后溶液中 ![]() 不变
不变
D.向0.1mol?L﹣1的醋酸溶液稀释到原体积的10倍后,溶液的PH=2
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁电池是以高铁酸盐(K2FeO4)和锌为电极材料,具有能量密度大、体积小、重量轻、寿命长、无污染等优点,除比亚迪外目前还没有其他厂家宣称其产品可以大规模实用化.电池的总反应为:3Zn+2K2FeO4+8H2O ![]() 3Zn(OH)2+2Fe(OH)3+4KOH.下列说法正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH.下列说法正确的是( )
A.充电时阳极反应式为:Zn﹣2e﹣+2OH﹣=Zn(OH)2
B.0.1molK2FeO4发生反应,转移电子数约为1.806×1024
C.充电时K2FeO4发生氧化反应
D.放电时正极反应为:2FeO42﹣+6e﹣+8H2O=2Fe(OH)3+10OH﹣
查看答案和解析>>
科目: 来源: 题型:
【题目】在某无色透明的酸性溶液中,能共存的离子组是()
A. NH4+、NO3-、A13+、Cl- B. Na+、Fe2+、K+、NO3-
C. MnO4-、K+、SO42-、Na+ D. K+、SO42-、HCO3-、Na+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com