
科目: 来源: 题型:
【题目】根据题意解答
(1)Fe3+具有氧化性,实验室测定含碘废液中I﹣的含量的过程如下:量取25.00mL废液于250mL锥形瓶中,分别加入5mL 2molL﹣1 H2SO4和10mL 20% Fe2(SO4)3溶液,摇匀.小火加热蒸发至碘完全升华,取下锥形瓶冷却后,加入几滴二苯胺磺酸钠(用作指示剂),用0.02500molL﹣1标准K2Cr2O7溶液进行滴定到终点.重复3次,数据记录如表:
次数 | 1 | 2 | 3 |
滴定体积/mL | 19.98 | 20.02 | 19.00 |
(i)在盛有废液的锥形瓶中先加入5mL 2molL﹣1 H2SO4的目的是 . (用离子方程式和语言叙述解释)
(ii)上述过程中涉及的反应:①2Fe3++2I﹣═2Fe2++I2② .
(iii)根据滴定有关数据,该废液中I﹣含量是gL﹣1 .
(iv)在滴定过程中,下列操作(其他操作正确)会造成测定结果偏低的是 .
A.终点读数时俯视读数,滴定前平视读数
B.锥形瓶水洗衣后未干燥
C.滴定管未用标准K2Cr2O7溶液润洗
D.盛标准K2Cr2O7溶液的滴定管,滴定前有气泡,滴定后无气泡.
(2)Fe3+和Ag+的氧化性相对强弱一直是实验探究的热点.某学习小组同学设计如下实验:
实验编号 | 实验操作 | 现象 |
1 | 向10mL 3mol/L KNO3酸性溶液(pH=1)中插入一根洁净的Ag丝,并滴加NaCl溶液 | 无白色沉淀生成 |
2 | 向10mL 1mol/L AgNO3溶液中滴加2mL 0.1mol/L FeSO4溶液,振荡,再滴加酸性KMnO4溶液 | 紫红色不褪去 |
3 | 向10mL 1mol/L Fe(NO3)3酸性溶液(pH=1)中插入一根洁净的Ag丝,并滴加NaCl溶液 | 有白色沉淀生成 |
请回答:
(i)设计实验①的目的是 .
(ii)实验③可得出结论是 .
(iii)写出实验②中反应的离子方程式
(iv)根据以上实验,Fe3+和Ag+的氧化性相对强弱与离子有关.
查看答案和解析>>
科目: 来源: 题型:
【题目】某学生准备用18.4mol/L的浓硫酸配制0.4mol/L的稀硫酸250mL,试回答下列问题:
(1)通过计算求出浓硫酸所需体积并用量筒量取,读取的数值为V=______mL。(计算结果保留小数点后一位)
(2)下列配制溶液的操作中,正确的顺序是________。(填序号)
①将浓硫酸转移至含有少量蒸馏水的烧杯中,并用玻璃棒搅拌
②冷却后,将稀释好的溶液转入250mL容量瓶中
③用量筒量取V mL浓硫酸
④盖好瓶塞,反复上下颠倒,摇匀
⑤小心地往250mL容量瓶中加蒸馏水至距离刻度线1-2cm处
⑥用胶头滴管滴加蒸馏水至液面与刻度线相切
⑦用少量蒸馏水洗涤烧杯2-3次,将洗涤液转移至250mL容量瓶中,轻轻摇动容量瓶,使溶液混合均匀
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验能达到相应目的是( )
选项 | A | B | C | D |
实验过程 |
|
|
|
|
实验目的 | 将乙二醇(HOCH2CH2OH)转化为乙二酸(H2C2O4) | 比较氯化铁和二氧化锰对H2O2分解反应的催化效果 | 证明稀硝酸与铜反应时表现出氧化性 | 用SO2与Ba(NO3)2反应获得BaSO3沉淀 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目: 来源: 题型:
【题目】某粗铜含铁、金和铅等杂质,通过电解精炼铜后,阳极泥含有Cu、Au(金)和PbSO4等杂质,为充分利用电解后的阳极泥和电解液,设计如下工艺流程: 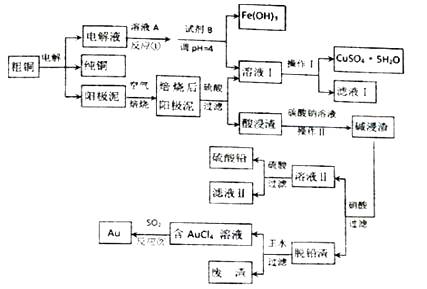
回答下列问题:
(1)溶液A是一种绿色氧化剂,则反应①的离子方程式为 .
(2)试剂B为 .
(3)焙烧阳极泥时,为了提高焙烧效率,采取的合理措施是(写一点即可).
(4)操作Ⅰ的主要步骤为过滤,洗涤,干燥
(5)写出反应②的离子方程式 .
(6)为了减少废液排放、充分利用有用资源,工业上将滤液Ⅰ并入溶液Ⅰ进行循环操作,请指出流程图中另一处类似的做法 .
(7)已知298K时,Ksp(PbCO3)=1.46×10﹣13 , Ksp(PbSO4)=1.2×10﹣8 , 用离子方程式表示加入碳酸钠溶液的作用 .
查看答案和解析>>
科目: 来源: 题型:
【题目】已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):
![]() 试通过计算和推理完成下面的问题:
试通过计算和推理完成下面的问题:
(1)A物质可以导致酸雨的形成。A应该属于________(用字母代号填写)。
a. 酸 b. 碱 c. 盐 d. 酸性氧化物 e. 碱性氧化物
(2)A物质可以使酸性![]() 溶液褪色,此反应中(填写化学式,下同)_______失去电子,氧化剂是________。
溶液褪色,此反应中(填写化学式,下同)_______失去电子,氧化剂是________。
(3)足量的铜片与10mL 18mol/L的浓![]() 充分反应,如果该反应过程中转移了0.1mol电子,生成的
充分反应,如果该反应过程中转移了0.1mol电子,生成的![]() 的物质的量为_______mol,生成的A气体在标准状况下体积为________L(假设气体全部逸出)。
的物质的量为_______mol,生成的A气体在标准状况下体积为________L(假设气体全部逸出)。
(4)计算:将反应后得到的溶液与足量![]() 溶液混合,充分反应。反应后所得沉淀的质量为______g。
溶液混合,充分反应。反应后所得沉淀的质量为______g。
查看答案和解析>>
科目: 来源: 题型:
【题目】在蒸馏实验中,下列叙述不正确的是
A. 蒸馏实验之前放入几粒沸石B. 将温度计水银球插入自来水中
C. 冷水从冷凝管下口入,上口出D. 收集蒸馏水时,应弃去开始馏出的部分
查看答案和解析>>
科目: 来源: 题型:
【题目】NA代表阿伏伽德罗常数的值.下列叙述正确的是( )
A.常温常压下,2.24 LSO2中所含氧原子数为0.2NA
B.将1 mol Cl2通入水中,HClO,Cl﹣、ClO﹣粒子数之和为2NA
C.1 mol NO2与足量H2O反应,转移的电子数为NA
D.0.1 mol熔融的NaHSO4中阳离子数目为0.1NA
查看答案和解析>>
科目: 来源: 题型:
【题目】反应体系中的物质有: ![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 。
。
(1)请将![]() 之外的反应物与生成物分别填入以下空格内(不用配平)。_____
之外的反应物与生成物分别填入以下空格内(不用配平)。_____
![]()
(2)反应中,被还原的元素是(标出价态)________。
(3)将氧化剂与还原剂及配平后的系数填入下列空格中(如果系数为1也要填写),并标出电子转移的方向和数目。_____

查看答案和解析>>
科目: 来源: 题型:
【题目】电浮选凝聚法是工业上采用的一种污水处理方法,即保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体,Fe(OH)3胶体具有吸附作用,可吸附水中的污物而使其沉淀下来,起到净水的作用,其原理如图所示.下列说法正确的是( ) 
A.石墨电极上发生氧化反应
B.根据图示,物质A为CO2
C.为增强污水的导电能力,可向污水中加入适量乙醇
D.甲烷燃料电池中CO32﹣向空气一极移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com