
科目: 来源: 题型:
【题目】周期表中前四周期元素R、W、X、Y、Z的原子序数依次递增.R基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子.工业上通过分离液态空气获得X单质.Y原子的最外层电子数与电子层数之积等于R、W、X三种元素的原子序数之和.Z基态原子的最外能层只有一个电子,其他能层均已充满电子.请回答下列问题:
(1)Z2+基态核外电子排布式为 .
(2)YX4﹣的空间构型是;与YX4﹣互为等电子体的一种分子为(填化学式);HYX4酸性比HYX2强,其原因是 .
(3)结构简式为RX(W2H3)2的化合物中R原子的杂化轨道类型为;1molRX(W2H3)2分子中含有σ键数目为 .
(4)往Z的硫酸盐溶液中通入过量的WH3 , 可生成[Z(WH3)4]SO4 , 下列说法正确的是 .
A.[Z(WH3)4]SO4中所含的化学键有离子键、极性键和配位键
B.在[Z(WH3)4]2+中Z2+给出孤对电子,WH3提供空轨道
C.[Z(WH3)4]SO4组成元素中第一电离能最大的是氧元素
(5)某Y与Z形成的化合物的晶胞如图所示(黑点代表Z原子). 
①该晶体的化学式为 .
②已知Z和Y的电负性分别为1.9和3.0,则Y与Z形成的化合物属于(填“离子”、“共价”)化合物.
③已知该晶体的密度为ρg.cm﹣3 , 阿伏伽德罗常数为NA , 则该晶体中Z原子和Y原子之间的最短距离为pm(只写计算式).
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上以铬铁矿(主要成份为FeO.Cr2O3 , 还含有Al2O3、SiO2等杂质)为主要原料生产红矾钠晶体(Na2Cr2O7 . 2H2O),其主要工艺流程如图:
已知:NaBiO3在碱性条件下能将Cr3+氧化为CrO42﹣ .
(1)固体A为
(2)实验室中操作①②的名称为
(3)固体C中含有的物质是Al( OH)3和Fe(OH)3 , 则H2 O2的作用是 .
已知:KsP[Fe(OH)3]=3.0×10﹣39 , KsP[Al(OH)3]=1×10﹣33 , 当pH=5.6时Cr(OH)3开始沉淀.室温下,Ⅱ中需调节溶液pH范围为(杂质离子浓度小于1×10﹣6mol/L视为沉淀完全).
(4)写出Ⅲ中发生反应的离子方程式 .
(5)Ⅳ中酸化是用硫酸而不用盐酸酸化,理由是(结合化学方程式回答);工业上也可设计如图示装置,用锂离子电池(LixC+Li1﹣xCoO2 ![]() C+LioO2 , LixC为难电离锂碳化合物)为电源,电解Na2CrO4溶液制取Na2Cr2O7 , 该装置工作时E电极的名称是极;电源的A极的电极反应式为 . 当电解过程中转移了0.5mol电子时,理论上右侧溶液的质量减少 g.
C+LioO2 , LixC为难电离锂碳化合物)为电源,电解Na2CrO4溶液制取Na2Cr2O7 , 该装置工作时E电极的名称是极;电源的A极的电极反应式为 . 当电解过程中转移了0.5mol电子时,理论上右侧溶液的质量减少 g.
查看答案和解析>>
科目: 来源: 题型:
【题目】锌是一种应用广泛的金属,目前工业上主要采用“湿法”工艺冶炼锌,某含锌矿的主要成分为ZnS(还含少量FeS等其他成分),以其为原料冶炼锌的工艺流程如图所示: 
回答下列问题:
(1)硫化锌精矿的焙烧在氧气气氛的沸腾炉中进行,所产生焙砂的主要成分的化学式为 .
(2)焙烧过程中产生的含尘烟气可净化制酸,该酸可用于后续的操作.
(3)浸出液“净化”过程中加入的主要物质为 , 其作用是 .
(4)电解沉积过程中的阴极采用铝板,阳极采用Pb﹣Ag合金惰性电极,阳极逸出的气是 .
(5)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质.“氧压酸浸”中发生主要反应的离子方程式为 .
(6)我国古代曾采用“火法”工艺冶炼锌,明代宋应星著的《天工开物》中有关于“升炼倭铅”的记载:“炉甘石十斤,装载入一泥罐内,…,然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…,冷淀,毁罐取出,…,即倭铅也.”该炼锌工艺过程主要反应的化学方程式为 . (注:炉甘石的主要成分为碳酸锌,倭铅是指金属锌)
查看答案和解析>>
科目: 来源: 题型:
【题目】水合肼(N2H4 . H2O)是无色、有强还原性的液体,实验室制备水合肼的原理为:CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4H2O+NaCl.据此,某学生设计了下列实验.
(1)【制备NaClO溶液】实验装置如图甲所示(部分夹持装置已省略)
已知:3NaClO ![]() 2NaCl+NaClO3
2NaCl+NaClO3
(i)配制30%NaOH溶液时,所需玻璃仪器除量筒外还有(填字母).
A.容量瓶 B.烧杯 C.移液管 D.玻璃棒
(ii)装置工中发生的离子反应方程式是;Ⅱ中玻璃管a的作用为;为了提高NaClO的产率,需对I中产生的Cl2进行净化,所用试剂是;Ⅱ中用冰水浴控制温度在30℃以下,其主要目的
(2)【制取水合肼】实验装置如图乙所示
仪器A的名称为;反应过程中,如果分液漏斗中溶液的滴速过快,部分N2H4H2O参与A中反应并产生大量氮气,产品产率因此降低,请
写出降低产率的相关化学反应方程式;充分反应后,加热蒸馏A内的溶液即可得到水合肼的粗产品.
(3)【测定肼的含量】
称取馏分0.3000g,加水配成20.0mL溶液,在一定条件下,用0.1500molL﹣1 的I2溶液滴定.
已知:N2H4H2O+2I2=N2↑+4Hl+H2O.
①滴定时,可以选用的指示剂为;
②实验测得消耗I2溶液的平均值为20.00mL,馏分中N2H4 . H2O的质量分数为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】三聚氰酸[C3N3(OH)3]可用于消除汽车尾气中的NO2。其反应原理为:
C3N3(OH)3![]() 3HNCO;8HNCO+6NO2
3HNCO;8HNCO+6NO2![]() 7N2+8CO2+4H2O
7N2+8CO2+4H2O
下列说法正确的是
A. C3N3(OH)3与HNCO为同一物质
B. HNCO是一种很强的氧化剂
C. 1 molNO2在反应中转移的电子为4mol
D. 反应中NO2是还原剂
查看答案和解析>>
科目: 来源: 题型:
【题目】由碳的氧化物直接合成乙醇燃料已进入大规模生产.
(1)如采取以CO和H2为原料合成乙醇,化学反应方程式:2CO(g)+4H2(g)CH3CH2OH(g)+H2O(g)△H;若密闭容器中充有10molCO与20molH2 , 在催化剂作用下反应生成乙醇,CO的转化率(α)与温度、压强的关系如图1所示. 
已知:2CO(g)+O2(g)═2CO2(g)△H1=﹣566kJmol﹣1
2H2(g)+O2(g)═2H2O(l)△H2=﹣572kJmol﹣1
CH3CH2OH(g)+3O2(g)═2CO2(g)+3H2O(g)△H3=﹣1366kJmol﹣1
H2O(g)═H2O(l)△H4=﹣44kJmol﹣1
①△H=kJmol﹣1
②若A、C两点都表示达到的平衡状态,则从反应开始到达平衡状态所需的时间tAtC(填“>”、“<”或“﹦”).
③若A、B两点表示在某时刻达到的平衡状态,此时在A点时容器的体积为10L,则该温度下的平衡常数:K=;
④熔融碳酸盐燃料电池(MCFS),是用煤气(CO+H2)格负极燃气,空气与CO2的混合气为正极助燃气,用一定比例Li2CO3和Na2CO3低熔混合物为电解质,以金属镍(燃料极)为催化剂制成的.负极上CO反应的电极反应式为 .
(2)工业上还可以采取以CO2和H2为原料合成乙醇,并且更被化学工作者推崇,但是在相同条件下,由CO制取CH3CH2OH的平衡常数远远大于由CO2制取CH3CH2OH 的平衡常数.请推测化学工作者认可由CO2制取CH3CH2OH的优点主要是: .
(3)目前工业上也可以用CO2来生产甲醇.一定条件下发生反应CO2(g)+3H2(g)CH3OH(g)+H2O(g).若将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化的曲线如图2所示(实线). 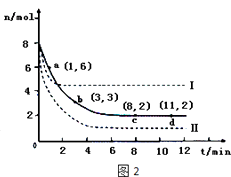
①请在图中绘出甲醇的物质的量随时间变化曲线.
②仅改变某一实验条件再进行两次实验,测得H2的物质的量随时间变化如图中虚线所示,曲线I对应的实验条件改变是 , 曲线Ⅱ对应的实验条件改变是 .
(4)将标准状况下4.48L CO2通入1L 0.3molL﹣1NaOH溶液中完全反应,所得溶液中微粒浓度关系正确的是 A.c(Na+)=c(HCO3﹣)+c(CO32﹣)+c(H2CO3)
B.c(OH﹣)+c(CO32﹣)=c(H2CO3)+c(H+)
C.c(Na+)+c(H+)=c(HCO3﹣)+2c(CO32﹣)+c(OH﹣)
D.2c(Na+)=3c(HCO3﹣)+3c(CO32﹣)+3c(H2CO3)
查看答案和解析>>
科目: 来源: 题型:
【题目】在一隔热系统中,向20.00mL 0.01000molL﹣1的醋酸溶液中逐滴加入0.01000mol.L﹣1的NaOH溶液,测得混合溶液的温度变化如图.下列相关说法正确的是( ) 
A.若a点溶液呈酸性,则a点有:c(CH3COO﹣)>c(Na+)>c(CH3COOH)
B.从b到c: ![]() 逐渐增大
逐渐增大
C.水的电离程度:b点<c点
D.b点有0.01000mol?L﹣1+c(H+)=c(Na)+﹣c(CH3COOH)+c(OH﹣)
查看答案和解析>>
科目: 来源: 题型:
【题目】某有色电解质溶液中,可能存在大量的![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 。你认为一定有的离子是_______,一定没有的离子是_______,还需进一步确认的离子是_______,请写出可行的实验方案_______(包括操作、现象和结论)。
。你认为一定有的离子是_______,一定没有的离子是_______,还需进一步确认的离子是_______,请写出可行的实验方案_______(包括操作、现象和结论)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com