
科目: 来源: 题型:
【题目】二氯化硫(SCl2)熔点-78℃,沸点59℃,密度1.638g/mL,遇水易分解,二氯化硫与三氧化硫作用可生成重要化工试剂亚硫酰氯(SOCl2)。以下是氯气与硫合成二氯化硫的实验装置。
试回答下列问题:

(1)装置A中发生反应的化学方程式为 。
(2)装置B、C应盛放的药品分别是 、 。
(3)实验开始前先在D中放一定量的硫粉.加热使硫熔化,然后转动和摇动烧瓶使硫附着在烧瓶内壁形成一薄层表面,这样做的目的是 。
(4)实验时,D装置需加热至50—59℃.最好采用的措施是 、如何防止E中液体挥发? 。
(5)F装置中干燥管内所盛物质是 ,作用是 。
(6)由二氯化硫与SO3作用生成亚硫酰氯的化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】海带中含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:

请填写下列空白:
(1)步骤①灼烧海带的目的是_____,除需要三脚架、玻璃棒、酒精灯之 外还需要用到的实验仪器是_________;
(2)步骤③实验操作名称是_____,步骤⑤用到的玻璃仪器是_____;
(3)如何检验步骤③后得到溶液中是否含有 I-________________;
(4)步骤④反应的离子方程式是_____;
(5)步骤④通入的氯气不能过量,理由是_____;
(6)步骤⑤中,某学生选择用苯来提取碘的理由是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化还原反应在生产、生活中具有广泛的用途。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是_____(选填编号)。
a. 海水提溴 b. 工业制氯碱 c. 海水晒盐 d. 海带提碘
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。“四种基本反应类型与氧化还原反应的关”可用下图表示。

试写出有水参加且符合反应类型 IV 的一个化学方程式:___________________。
(3)工业上利用NaIO3和NaHSO3反应来制取单质I2。
①配平下列化学方程式并标明电子转移的方向和数目:
_____NaIO3+ NaHSO3→ I2+ Na2SO4+ H2SO4+ H2O
②该反应还原剂是_____,_____元素被还原,若生成 1mol 氧化产物则转移电子数目为_____NA。
(4)已知:HSO3-、I2、I-、SO42-和一些未知物组成的一个氧化还原反应,其中SO42-是氧化产物,该反应中还原性HSO3-_____I-(填“>”或“<”),完成该反应_____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某氧原子的质量为a g,12C原子的质量为b g,且NA表示阿氏常数,下列说法中正确的是: ( )
A.氧元素的相对原子质量为12a/b B.1mol该原子质量为bNAg
C.x g该氧原子所含电子数为8x/a D.y g 该氧原子的中子数一定为8y/a
查看答案和解析>>
科目: 来源: 题型:
【题目】A~D 其性质或结构信息如下表:
元素 | A | B | C | D |
性质或结构信息 | 原子核内只有 1个质子 | 单质的体积分数在空气中排第二 | M 层上两种不同能量电子数的差值为 3 | 其单质常温下是唯一一种液态非金属单质 |
请根据表中的信息回答下列问题:
(1)四种元素为:A_____;B_____;C_____;D_____;
(2)B 原子的电子式:_____;C 原子核外电子共占据_____个轨道;
(3)D 单质与A2B反应的化学方程式为_____;
(4)写出 A 单质在 C 单质中燃烧的现象_____;
(5)请从结构上说明 C 单质的氧化性为什么大于 D_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为反应2X(g)+Y(s)2Z(g)的反应过程和能量关系图,下列说法正确的是( ) 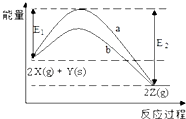
A.曲线a和b表示两个反应过程的反应热不同
B.曲线a一定表示反应是在无催化剂时的反应过程
C.增大压强,X的转化率一定增大
D.反应达平衡,升高温度,平衡常数K值一定减小
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、L、M五种元素的原子序数依次增大.X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素.
回答下列问题:
(1)L的元素符号为;M在元素周期表中的位置为;五种元素的原子半径从大到小的顺序是(用元素符号表示).
(2)Z、X两元素按原子数目比l:3和2:4构成分子A和B,A的电子式为 , B的结构式为 .
(3)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为 , 其最高价氧化物对应的水化物化学式为 . 该族2~5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1mol硒化氢反应热的是(填字母代号).
a.+99.7molL﹣1 b.+29.7molL﹣1 c.﹣20.6molL﹣1 d.﹣241.8kJmol﹣1 .
查看答案和解析>>
科目: 来源: 题型:
【题目】在容积为1.00L的容器中,通入一定量的N2O4 , 发生反应N2O4(g)2NO2(g),随温度的升高,混合气体的颜色变深.
回答下列问题:
(1)反应的△H0(填“大于”或“小于”);100℃时,体系中各物质浓度随时间变化如图所示.在0~60s时段,反应速率v(N2O4)为molL﹣1s﹣1;反应的平衡常数K1为 .
(2)100℃时达平衡后,改变反应温度为T,c(N2O4)以0.0020molL﹣1s﹣1的平均速率降低,经10s又达到平衡.
①T100℃(填“大于”或“小于”),判断理由是 .
②列式计算温度T时反应的平衡常数K2 .
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向(填“正反应”或“逆反应”)方向移动,判断理由是 . 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com