
科目: 来源: 题型:
【题目】下列有关石油加工及其产品的说法不正确的是( )
A. 石油的分馏是物理变化
B. 石油裂化的主要目的是提高汽油的产量和质量
C. 石油催化重整的主要目的是得到芳香烃
D. 直馏汽油和裂化汽油均可萃取溴水中的溴
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:I2+2S2O32﹣═S4O62﹣+2I﹣
相关物质的溶度积常数见下表:
物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
Ksp | 2.2×10﹣20 | 2.6×10﹣39 | 1.7×10﹣7 | 1.3×10﹣12 |
(1)某酸性CuCl2溶液中含有少量的FeCl3 , 为得到纯净的CuCl22H2O晶体,加入 , 调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)= . 过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl22H2O晶体.
(2)在空气中直接加热CuCl22H2O晶体得不到纯的无水CuCl2 , 原因是(用化学方程式表示).由CuCl22H2O晶体得到纯的无水CuCl2的合理方法是 .
(3)某学习小组用“间接碘量法”测定含有CuCl22H2O晶体的试样(不含能与I﹣发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀.用0.100 0molL﹣1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.
①可选用作滴定指示剂,滴定终点的现象是 .
②CuCl2溶液与KI反应的离子方程式为 .
③该试样中CuCl22H2O的质量百分数为
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组利用如图装置进行“铁与水反应”的实验,并检验产物的性质,请回答下列问题:

(1)A装置的作用是________________,B中反应的化学方程式为_____________。
(2)D的作用是____________________________________________________________。
(3)E中的现象是__________________________________________________________。
(4)A、B两个装置中应先点燃_______处的酒精灯,点燃E处酒精灯之前应进行的操作是_______________________________________________________________________。
【答案】 产生水蒸气 3Fe+4H2O(g) ![]() Fe3O4+4H2 吸收未反应的水蒸气 黑色固体变为红色,右端管壁有水珠生成 A 收集H2,并检验其纯度
Fe3O4+4H2 吸收未反应的水蒸气 黑色固体变为红色,右端管壁有水珠生成 A 收集H2,并检验其纯度
【解析】(1)铁与水蒸气反应的条件是高温,水的状态是气体,所以A装置的作用是产生水蒸气,B中是铁与水蒸气反应生成氢气和四氧化三铁,方程式为3Fe+4H2O(g)![]() Fe3O4+4H2;(2)生成的氢气中含有水蒸气,则D中碱石灰的作用是吸收未反应的水蒸气;(3)氢气还原氧化铜得到铜和水即H2+CuO
Fe3O4+4H2;(2)生成的氢气中含有水蒸气,则D中碱石灰的作用是吸收未反应的水蒸气;(3)氢气还原氧化铜得到铜和水即H2+CuO![]() Cu+H2O,所以实验现象是硬质玻璃管中黑色固体变为红色,硬质玻璃管右端管壁有液滴生成;(4)若先点燃B处,铁会与氧气先发生反应,所以须先点燃A处;氢气是可燃性气体混有空气会发生爆炸,所以点燃E处酒精灯之前应进行的操作是验证氢气的纯度。
Cu+H2O,所以实验现象是硬质玻璃管中黑色固体变为红色,硬质玻璃管右端管壁有液滴生成;(4)若先点燃B处,铁会与氧气先发生反应,所以须先点燃A处;氢气是可燃性气体混有空气会发生爆炸,所以点燃E处酒精灯之前应进行的操作是验证氢气的纯度。
【题型】实验题
【结束】
20
【题目】某研究性学习小组为研究氯气是否具有漂白性,设计如图所示实验装置。试根据实验装置回答下列问题:

A、C中为干燥的有色布条,B为无色液体,D中为NaOH溶液。
(1)在常温下,KMnO4固体可以与浓盐酸反应生成氯气,其反应方程式为2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O,则其反应装置应选用甲、乙、丙中的_______。
(2)B中的液体为____________,其作用为____________________________________。
(3)A、C中有色布条的颜色变化分别为__________________________________,A、C的实验现象说明氯气是否具有漂白性?________(填“是”或“否”)。
(4)D中NaOH溶液的作用是________________________________________(用离子方程式说明)。
(5)将产生的氯气通入滴有酚酞的NaOH溶液中,溶液红色褪去。小组内有甲、乙两种意见:
甲:氯气溶于水后溶液显酸性,中和了NaOH,使溶液褪为无色;
乙:氯气溶于水生成漂白性物质,使溶液褪为无色。
丙同学在褪色后的溶液中逐渐加入足量的NaOH溶液,溶液一直未见红色,则______(填“甲”或“乙”)的意见正确。
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求填空
(1)常温下,0.05mol/L硫酸溶液中,pH值为 , 水电离出的c(H+)=mol/L.
(2)某温度时,测得0.01molL﹣1的NaOH溶液的pH为11,则该温度下水的离子积常数为
在此温度下,将pH=a的H2SO4溶液VaL与pH=b的NaOH溶液VbL混合.
①若所得混合液为中性,且a=2,b=12,则Va:Vb= .
②若所得混合液的pH=10,且a=2,b=12,则Va:Vb=
查看答案和解析>>
科目: 来源: 题型:
【题目】已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:
醋酸 | 碳酸 | 亚硫酸 |
Ka=1.75×10﹣5 | Ka1=4.30×10﹣7 Ka2=5.61×10﹣11 | Ka1=1.54×10﹣2 Ka2=1.02×10﹣7 |
(1)写出碳酸的第一步电离平衡常数表达式:Ka1= .
(2)在相同条件下,试比较H2CO3、HCO3﹣和HSO3﹣的酸性强弱:>>
(3)①如图表示常温时稀释醋酸、碳酸两种酸的稀溶液时,溶液PH随水量的变化图象中,曲线I表示的酸是(填化学式).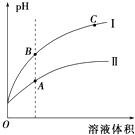
②a、b、c三点中,水的电离程度最大的是(填字母).
查看答案和解析>>
科目: 来源: 题型:
【题目】标准状况下将35 mL气态烷烃完全燃烧,恢复到原来状况下,得到二氧化碳气体140 mL,则该烃的分子式为
A. C5H12B. C4H10C. C3H6D. C3H8
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质中,X是主要物质,Y是少量杂质,Z是为除去杂质所要加入的试剂,其中所加试剂正确的组合是 ( )
A | B | C | D | |
X | FeCl2溶液 | FeCl3溶液 | Fe | Na2SO4溶液 |
Y | FeCl3 | CuCl2 | Al | Na2CO3 |
Z | Cu | Fe | NaOH溶液 | BaCl2溶液 |
A. A B. B C. C D. D
【答案】C
【解析】A.铜粉与氯化铁反应生成氯化亚铁和氯化铜,会引入新杂质,故A错误;B.二者均与Fe反应,不符合除杂的原则,不能除杂,故B错误;C.Al与NaOH溶液反应,而Fe不能,则加NaOH溶解后过滤可除杂,故C正确;D.二者均与BaCl2溶液反应,应加适量硫酸除杂,故D错误;故选C。
【题型】单选题
【结束】
19
【题目】某化学兴趣小组利用如图装置进行“铁与水反应”的实验,并检验产物的性质,请回答下列问题:
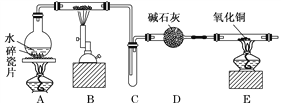
(1)A装置的作用是________________,B中反应的化学方程式为_____________。
(2)D的作用是____________________________________________________________。
(3)E中的现象是__________________________________________________________。
(4)A、B两个装置中应先点燃_______处的酒精灯,点燃E处酒精灯之前应进行的操作是_______________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组为研究氯气是否具有漂白性,设计如图所示实验装置。试根据实验装置回答下列问题:

A、C中为干燥的有色布条,B为无色液体,D中为NaOH溶液。
(1)在常温下,KMnO4固体可以与浓盐酸反应生成氯气,其反应方程式为2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O,则其反应装置应选用甲、乙、丙中的_______。
(2)B中的液体为____________,其作用为____________________________________。
(3)A、C中有色布条的颜色变化分别为__________________________________,A、C的实验现象说明氯气是否具有漂白性?________(填“是”或“否”)。
(4)D中NaOH溶液的作用是________________________________________(用离子方程式说明)。
(5)将产生的氯气通入滴有酚酞的NaOH溶液中,溶液红色褪去。小组内有甲、乙两种意见:
甲:氯气溶于水后溶液显酸性,中和了NaOH,使溶液褪为无色;
乙:氯气溶于水生成漂白性物质,使溶液褪为无色。
丙同学在褪色后的溶液中逐渐加入足量的NaOH溶液,溶液一直未见红色,则______(填“甲”或“乙”)的意见正确。
【答案】 丙 浓硫酸 干燥氯气或吸收氯气中的水蒸气 A中有色布条褪色,C中有色布条不褪色 否 Cl2+2OH-===Cl-+ClO-+H2O 乙
【解析】(1)高锰酸钾固体和浓盐酸反应制备氯气,反应不需要加热,为固体与液体反应,且氯气能溶于水,甲装置适用于固体和液体加热制备气体,乙装置适用于固体和液体反应,要求固体难溶于水且生成的气体难溶于水,丙装置适合,故选丙;(2)浓硫酸具有吸水性,且浓硫酸和氯气不反应,所以B中的液体为浓硫酸,作用是干燥氯气;(3)高锰酸钾固体和浓盐酸反应生成的氯气中有水蒸气,进入A中,氯气和水蒸气反应生成盐酸和次氯酸,HClO有漂白性,A中有色布条褪色,B中浓硫酸具有吸水性干燥氯气,干燥氯气不能使有色布条褪色,所以C中有色布条不褪色,A、C的实验现象不能说明氯气具有漂白性;(4)氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠与水,反应离子方程式为Cl2+2OH-===Cl-+ClO-+H2O;(5)因在褪色后的溶液中逐渐加入足量的NaOH溶液,因溶液中有酚酞,碱性溶液应显红色,溶液一直未见红色,说明氯气溶于水生成漂白性物质,使溶液褪为无色,不是由于碱被中和褪色,故乙正确。
【题型】实验题
【结束】
21
【题目】有一无色溶液100 mL,其中可能含有Fe3+、Al3+、Na+、Mg2+、Cu2+、NH![]() 、K+、CO
、K+、CO![]() 、SO
、SO![]() 等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如下图所示。
等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如下图所示。

请回答下列问题:
(1)焰色反应是________(填“物理”或“化学”)变化;实验②中经过滤得到白色沉淀,该沉淀如何洗涤?______________________________________________________________。
(2)原溶液中一定存在的离子有________(写化学式),可能存在的离子有________。
(3)实验③中产生的白色沉淀的成分可能是_________________________________。
(4)若溶液中K+物质的量为0.04 mol,则c(Na+)=________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有机物不能由CH2=CH2通过加成反应制取的是( )
A. CH3CH2ClB. CH2Cl—CH2Cl
C. CH3—CH2OHD. CH3—COOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com