
科目: 来源: 题型:
【题目】元素A、B、C、D、E、F、G在元素周期表中的位置如图1所示,回答下列问题: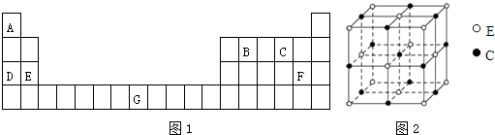
(1)G的基态原子核外电子排布式为 . 原子的第一电离能:DE(填“>”或“<”).
(2)根据价层电子互斥理论,价层电子对之间的斥力大小有如下顺序:l﹣l>l﹣b>b﹣b(l为孤对电子对,b为键合电子对),则关于A2C中的A﹣C﹣A键角可得出的结论是 .
A.180°
B.接近120°,但小于120°
C.接近120°,但大于120°
D.接近109°28′,但小于109°28′
(3)化合物G(BC)5的熔点为﹣20℃,沸点为103℃,其固体属于晶体,该物质中存在的化学键类型有 , 它在空气中燃烧生成红棕色氧化物,反应的化学方程式为 .
(4)化合物BCF2的立体构型为 , 其中B原子的杂化轨道类型是 , 写出两个与BCF2具有相同空间构型的含氧酸根离子 .
(5)化合物EC的晶胞结构如图2所示,晶胞参数a=0.424nm.每个晶胞中含有个E2+ , 列式计算EC晶体的密度 gcm﹣3 .
查看答案和解析>>
科目: 来源: 题型:
【题目】向一定量的Fe、FeO、Fe2O3的混合物中加入100mL浓度为1.0mol·L-1的盐酸,恰好使混合物完全溶解,有气体放出,所得溶液中加入KSCN溶液后无红色出现。若用足量的CO在高温下还原相同质量此混合物,能得到铁的质量是( )
A. 11.2g B. 5.6g
C. 2.8g D. 1.4g
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 溶液焰色反应时,如果火焰呈黄色就说明该溶液一定有钠元素,一定没有钾元素
B. 除去CO2中的HCl气体,只需将气体通过NaOH溶液
C. 在某溶液中滴加硝酸酸化的氯化钡溶液,有白色沉淀生成,说明溶液中一定含SO![]()
D. 在氧化还原反应中,阳离子也能失去电子被氧化,阴离子也能得到电子被还原
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,若锥形瓶内是水,分液漏斗内的液体是盐酸,向烧杯内滴加少量盐酸时,发现U形管内液体右移,静止冷却后液面左边低于右边,则烧杯内的物质不可能是
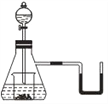
A. 过氧化钠 B. 碳酸氢钠
C. 氧化钠 D. 铝
查看答案和解析>>
科目: 来源: 题型:
【题目】N4的分子结构类似白磷分子,它的结构如图所示,已知断裂1mol N﹣N键需要吸收167kJ热量,生成1mol N≡N键需放出942kJ热量.根据以上信息和数据,下列说法中正确的是( ) 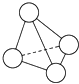
A.1 mol N4气体转变为N2将放出775 kJ热量
B.1 mol N4气体转变为N2将放出882 kJ热量
C.1 mol N4气体转变为N2将吸收775 kJ热量
D.1 mol N4气体转变为N2将吸收882 kJ热量
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质的熔沸点高低比较正确的是( )
A.邻二甲苯( ![]() )、邻羟基苯甲醛(
)、邻羟基苯甲醛( ![]() )熔沸点均于其对应对位取代物
)熔沸点均于其对应对位取代物
B.卤素元素的单质及其氢化物的熔沸点随原子半径的增大而升高
C.石墨、金刚石、碳化硅、晶体硅、白磷、水、干冰熔沸点依次降低
D.NaCl、MgCl2、MgO,Al2O3熔沸点依次减小
查看答案和解析>>
科目: 来源: 题型:
【题目】纯碱是造纸、玻璃、纺织、制革等行业的重要原料.
(1)路布兰法制备纯碱:①食盐与硫酸反应生成硫酸钠;②将硫酸钠、石灰石和足量煤混合,高温下共熔制得碳酸钠,反应有硫化钙生成.第②步反应的化学方程式为 .
(2)①原盐水中含少量Mg2和Ca2 , 结合生产实际,精制盐水需要的试剂时、 . (填化学式)
②步骤 II保持在30﹣35℃进行,反应的化学方程式为 , 该反应能发生的原因是 . 该工艺中循环利用的物质是 .
③索尔维制纯碱不需要用到的一种设备是 (填正确答案标号).
A.吸氨塔 B.蒸氨塔 C.碳酸化塔 D.沸腾炉 E.石灰窑
④该工艺中食盐利用率大约只有70%,食盐损失的主要原因是 . 我国科学家侯德榜将合成氨工业得到的NH3和CO2引入纯碱的生产,向上述工艺的“母液”中通入NH3并加入食盐固体,降温结晶得到副产品(填化学式),剩余母液返回“吸氨”步骤,大大提高了食盐的利用率.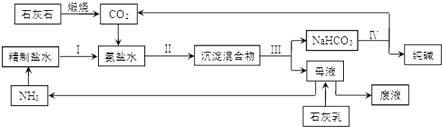
(3)纯碱产品中可能含有碳酸氢钠.用热重分析的方法测定纯碱中碳酸氢钠的质量分数为ω(NAHCO3)=(列出算式,所需数据用字母表示,并说明各字母的含义).
查看答案和解析>>
科目: 来源: 题型:
【题目】已知在25℃、101kPa下,1g C8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量.表示上述反应的热化学方程式正确的是( )
A.C8H18(l)+ ![]() O2(g)=8CO2(g)+9H2O(g)△H=﹣48.40 kJmol﹣1
O2(g)=8CO2(g)+9H2O(g)△H=﹣48.40 kJmol﹣1
B.C8H18(l)+ ![]() O2(g)=8CO2(g)+9H2O(l)△H=﹣5518 kJmol﹣1
O2(g)=8CO2(g)+9H2O(l)△H=﹣5518 kJmol﹣1
C.C8H18(l)+ ![]() O2(g)=8CO2(g)+9H2O(l)△H=+5518 kJmol﹣1
O2(g)=8CO2(g)+9H2O(l)△H=+5518 kJmol﹣1
D.C8H18(l)+ ![]() O2(g)=8CO2(g)+9H2O(l)△H=﹣48.40 kJmol﹣1
O2(g)=8CO2(g)+9H2O(l)△H=﹣48.40 kJmol﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com