
科目: 来源: 题型:
【题目】在恒容绝热(不与外界交换能量)条件下进行2A(g)+B(g)3C(g)+2D(s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高.
物质 | A | B | C | D |
起始投料/mol | 2 | 2 | 3 | 0 |
该反应的平衡常数表达式为K= . 升高温度,平衡常数将(填“增大”“减小”或“不变”).
查看答案和解析>>
科目: 来源: 题型:
【题目】硅单质及其化合物应用范围很广。请回答下列问题:
(1)制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:
![]()
①写出由石英砂和焦炭在高温下制备粗硅的化学反应方程式:_____________。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种气体,写出配平的化学反应方程式: _____________;H2还原SiHCl3过程中若混入O2,可能引起的后果是______________。
(2)下列有关硅材料的说法正确的是_____________ (填字母代号)。
A.氮化硅硬度大、熔点高,可用于制作高温陶瓷和轴承
B.石英坩埚耐高温性强,可用于加热熔融氢氧化钠
C.神舟10号飞船所用太阳能电池板可将光能转换为电能,所用转换材料单晶硅也可以制作电脑芯片
D.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
E.盐酸可以与硅反应,故可采用盐酸为抛光液抛光单晶硅
F.玛瑙饰品的主要成分与建筑材料砂子相同
查看答案和解析>>
科目: 来源: 题型:
【题目】用下面两种方法可以制得白色的Fe(OH)2沉淀:
【方法一】用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应来制备。
实验室用硫酸亚铁晶体配制上述FeSO4溶液时,一般需加入铁粉和稀硫酸,加入铁粉的目的是_____________。
【方法二】在如图所示的装置中,用NaOH溶液、铁屑、稀H2SO4等试剂来制备。

(1)实验开始时,止水夹e是______(填“打开”或“关闭”)的。
(2)如何检验装置内空气已经排尽?________________。
(3)排尽装置内空气后,为了制得白色Fe(OH)2沉淀,操作步骤是________。
(4)开启活塞f放掉约2/3液体,此时裝置B中试剂瓶中发生的化学反应方程式为________。
(5)下列各图示中________(填序号)能较长时间看到Fe(OH)2白色沉淀。
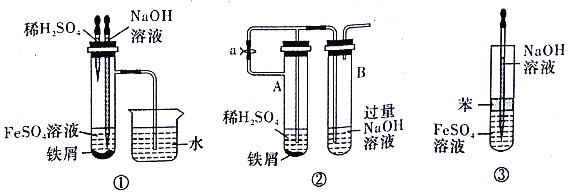
查看答案和解析>>
科目: 来源: 题型:
【题目】可以用来断定碳酸氢钠粉末中是否混有碳酸钠的实验方法是( )
A. 加热时有无气体放出
B. 滴加盐酸时有无气泡放出
C. 溶于水后,滴加稀的氯化钙溶液看有无白色沉淀生成
D. 溶于水后,滴加澄清石灰水,看有无白色沉淀生成
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化铁是常见的水处理剂,利用废铁屑可制备无水氯化铁.实验室制备装置和工业制备流程图如图: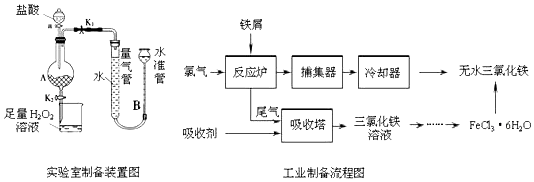
已知:①无水FeCl3的熔点为555K、沸点为588K.
②废铁屑中的杂质不与盐酸反应
③不同温度下六水合氯化铁在水中的溶解度如表:
温度/℃ | 0 | 20 | 80 | 100 |
溶解度(g/100 g H2O) | 74.4 | 91.8 | 525.8 | 535.7 |
实验室制备操作步骤如下:
Ⅰ打开弹簧夹K1 , 关闭弹簧夹K2 , 并打开活塞a,缓慢滴加盐酸.
Ⅱ当装置A中不产生气泡或量气管和水准管液面不变时,关闭弹簧夹K1 , 打开弹簧夹K2 , 当A中溶液完全进入烧杯后关闭活塞a.
Ⅲ将烧杯中溶液经过一系列操作后得到FeCl36H2O晶体.
(1)烧杯中足量的H2O2溶液的作用是 .
(2)为了测定废铁屑中铁的质量分数,操作Ⅱ中“…”的内容是 .
(3)从FeCl3溶液制得FeCl36H2O晶体的操作步骤是:加入后、蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(4)试写出吸收塔中反应的离子方程式: .
(5)捕集器温度超过673K时,存在相对分子质量为325的铁的氯化物,该物质的分子式为
(6)FeCl3的质量分数通常可用碘量法测定:称取m g无水氯化铁样品,溶于稀盐酸,配制成100mL溶液;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入几滴淀粉溶液,并用c molL﹣1 Na2S2O3溶液滴定,消耗V mL(已知:I2+2S2O32﹣═2I﹣+S4O62﹣).
①滴定过程中可能造成实验结果偏低的是
A.锥形瓶未润洗 B.锥形瓶中溶液变色后立刻停止滴定,进行读数
C.滴定管尖嘴内滴定前无气泡,滴定终点发现气泡 D.滴定终点时仰视读数
②样品中氯化铁的质量分数.
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组欲测定某已部分变质的小苏打样品中Na2CO3的质量分数,设计如下实验方案。
【方案一】称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为_______________。
(2)实验中,需加热至恒重的目的是_______________。
【方案二】称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤、干燥沉淀,称量固体质量,计算。(已知:Ba2++OH-+HCO3-==BaCO3↓+H2O)
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为_______________。
(3)实验中判断沉淀是否完全的方法是_______________。
【方案三】按如下图所示装置进行实验:
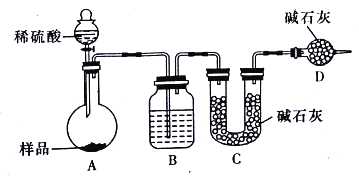
(1)D装置的作用是_______________。分液漏斗中_________(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.90g样品,实验后测得C装置增重8.80g,则样品中Na2CO3的质量分数为________________(保留三位有效数字)
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存的在一个明显缺陷是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有一种用CO2生产甲醇燃料的方法.已知:
CO2(g)+3H2(g)CH3OH(g)+H2O(l)△H=﹣akJmol﹣1;
CH3OH(g)═CH3OH(l)△H=﹣bkJmol﹣1;
2H2(g)+O2(g)═2H2O(l)△H=﹣ckJmol﹣1;
则表示CH3OH(l)燃烧热的热化学方程式为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验操作中,不正确的是
A. 用量筒量取 30mL 溶液 B. 用四氯化碳萃取碘水中的碘
C. 用托盘天平称取 2.5g 固体 D. 用温度计代替玻璃棒搅拌溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com