
科目: 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A. 向氯化铝溶液中加入过量氨水:Al3++4NH3·H2O===AlO2—+4NH4++2H2O
B. 用浓NaOH溶液溶解Al2O3:2OH-+Al2O3===2AlO![]() +H2O
+H2O
C. 向浓烧碱溶液中加入铝片Al+2OH-=== AlO2—+H2↑
D. 向碳酸镁中滴加稀盐酸:CO32—+2H+===CO2↑+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】随原子序数的递增,八种短周期元素(用字母X等表示)原子半径的相对大小、最高正价或最低负价的变化如图1所示.
根据判断出的元素回答问题:
(1)z在元素周期表的位置是 .
(2)比较d、f简单离子的半径大小(用化学符号表示,下同)>;比较d、g元素的简单气态氢化物的稳定性大小> .
(3)任选上述元素组成一种四原子共价化合物,写出其电子式 .
(4)已知1mol固体e的单质在足量d2气体中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式 .
(5)由上述元素组成的离子化合物 Q:eh 和W:e2gd4 , 若电解含2molQ和2molW的混合水溶液,当阳极产生44.8L气体(标准状况下,且不考虑气体的溶解和损失)时,电路中转移电子的物质的量为mol.
(6)上述元素可组成盐R:zx4f(gd4)2 . 向盛有10mL1molL﹣1R溶液的烧杯中滴加1molL﹣1 NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如图2:①R溶液中,离子浓度由大到小的顺序是 .
②写出m点发生反应的离子方程式 .
③若在R溶液中改加20mL 1.2molL﹣1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为mol.
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是
A. 从性质的角度分类,SO2属于酸性氧化物
B. 从对大气及环境影响的角度,SO2是一种大气污染物
C. 从在水中是否发生电离的角度,SO2属于电解质
D. 从元素化合价的角度分类,SO2即可作氧化剂又可作还原剂
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)如图所示,将氯气依次通过盛有干燥的有色布条和湿润的有色布条的广口瓶,可观察到的现象是__________________________________.
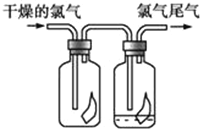
(2)写出C12与水反应的化学方程式________________________
(3)为防止氯气污染空气,可用氢氧化钠溶液吸收多余的氯气,原理是________________(用化学方程式表示).根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是________(填化学式,下同)。
(4)氯气泄漏时,人们需尽快远离现场,可用浸有一定浓度某物质水溶液的毛巾捂住口鼻,最适宜采用的物质是__________.
A.NaOH B.NaCl C.KBr D.Na2CO3.
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述中正确的是( )
A.体积相同、浓度均为0.1 mol?L﹣1的NaOH溶液、氨水,分别稀释m倍、n倍,溶液的pH都变成9,则m<n
B.有甲、乙两氨水溶液,测得甲的pH=a,乙的pH=a+1,则甲乙两溶液c(H+)之比为10:1
C.相同温度下,0.2 mol?L﹣1乙酸溶液与0.1 mol?L﹣1乙酸溶液中c(H+)之比为2:1
D.已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为α,K= ![]() .若加入少量醋酸钠固体,则CH3COOH?CH3COO﹣+H+向左移动,α减小,K变小
.若加入少量醋酸钠固体,则CH3COOH?CH3COO﹣+H+向左移动,α减小,K变小
查看答案和解析>>
科目: 来源: 题型:
【题目】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)下列物质不属于硅酸盐的是(____)
A.陶瓷 B.玻璃
C.水泥 D.生石灰
(2)SiO2是玻璃的主要成分之一,SiO2与氢氧化钠溶液反应的化学方程式为_______________________,工艺师常用________(填物质名称)来雕刻玻璃。
(3)Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是________。
A.普通玻璃坩埚 B.石英玻璃坩埚
C.氧化铝坩埚 D.铁坩埚
(4)工业上常利用反应2C+SiO2![]() Si+2CO↑制备硅单质,该反应中氧化剂是________。
Si+2CO↑制备硅单质,该反应中氧化剂是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有关氨的实验室制取和性质实验如下:
(1)实验室制取氨气的化学方程式为____________________________.验证氨气是否收集满的方法是________________________。
(2)如图是实验室进行氨气溶于水的喷泉实验装置,下列叙述错误的是________.


A.该实验说明氨气是一种极易溶于水的气体
B.进入烧瓶中的液体颜色由无色变为红色,说明氨水呈碱性
C.形成喷泉的原因是氨气溶于水后,烧瓶内的气压小于大气压
D.用氯气代替氨气,利用此装置也可进行喷泉实验
(3)干燥的氨气在高温下能被氧化铜氧化,生成两种单质和一种化合物.反应的化学方程式是___________________________________.
(4)写出Cu与浓硫酸在加热条件下反应的化学方程式_____________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】铝土矿的主要成分是Al2O3,还含有Fe2O3、SiO2等杂质。
Ⅰ.从铝土矿中提取氧化铝的流程如下图所示:
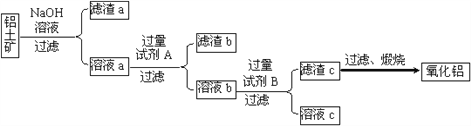
(1)试剂A是________;溶液b与试剂B反应的离子方程式为________。
(2)加入NaOH溶液进行的反应的离子方程式为_________、____________。
Ⅲ.新型陶瓷氮化铝可用以下两种方法制备
(3)①氧化铝高温还原法: Al2O3 + C + N2 ![]() AlN + CO(请配平)
AlN + CO(请配平)
②氯化铝与氨气高温合成法:AlCl3+NH3 ![]() AlN+3HCl
AlN+3HCl
(4)方法②比方法①在生产上更具优势。下列说法中,正确的是_______。
A.方法①中的 Al2O3、C、N2结构稳定,反应时破坏化学键需要消耗更多的能量
B.方法①中的Al2O3和C容易残留在氮化铝中
C.两种方法中氮化铝均为还原产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com