
科目: 来源: 题型:
【题目】医学上常用酸性高锰酸钾溶液和草酸溶液的反应来测定血钙的含量。回答下列问题:
H++ MnO4-+ H2C2O4— CO2↑+ Mn2++ ![]()
(1)配平以上离子方程式,并在![]() 中填上所需的微粒。_____________
中填上所需的微粒。_____________
(2)该反应中的还原剂是___________________。
(3)测定血钙的含量的方法:取2 mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液与其反应。
①稀硫酸溶解CaC2O4沉淀的化学方程式是________________________。
②溶解沉淀时____(“能”或“不能”)用稀盐酸,原因是________________。
③若消耗了1.0×10-4mol·L-1的KMnO4溶液20.00 mL,则100 mL该血液中含钙____mg。
查看答案和解析>>
科目: 来源: 题型:
【题目】四种短周期元素A、B、C、D的性质或结构信息如下:信息①原子半径大小:A>B>C>D
信息②四种元素之间形成的某三种分子的比例模型及部分性质:
请根据上述信息回答下列问题.
(1)B元素在周期表中的位置;
(2)BC2分子的电子式;
(3)A元素的单质与物质甲发生反应的离子方程式;
(4)丙的钠盐溶液呈性,用化学用语表示其原因;
(5)物质丁的元素组成和甲相同,丁分子具有18电子结构.向盛有一定浓度丁溶液的试管中,逐滴加入用少量稀硫酸酸化的硫酸亚铁溶液.滴加过程中的现象是:①浅绿色溶液变成深棕黄色;
②有少量气泡出现(经验证是氧气),片刻后反应变得剧烈 , 并放出较多热量,继续滴加溶液,静置一段时间;
③试管底部出现红褐色沉淀 . 向浊液中再滴入稀硫酸,沉淀溶解,溶液呈黄色.
请用化学方程式或离子方程式及必要的文字解释①、②、③中划线的字.
①;
②;
③ .
查看答案和解析>>
科目: 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性,回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式________________________________。
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①H3PO2中,P元素的化合价为__________。
②利用H3PO2进行化学镀银反应中,当氧化产物为H3PO4时,氧化剂与还原剂的物质的量之比为__________。
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式:_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质溶于水的电离方程式正确的是( )
A. Al2(SO4)3 = 2Al3+ + 3SO42-B. NaHCO3 = Na+ + H++ CO32-
C. NaHSO4= Na+ + HSO4-D. KClO3 = K+ + Cl-+ 3O2-
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:乙二酸晶体熔点101.5℃;乙二酸晶体加热分解的方程式为:H2C2O42H2O![]() 3H2O + CO2↑+ CO↑。现利用下列装置验证反应产物中含有CO2和CO(装置不能重复使用)。请回答下列问题:
3H2O + CO2↑+ CO↑。现利用下列装置验证反应产物中含有CO2和CO(装置不能重复使用)。请回答下列问题:

(1)检验装置A气密性的方法是________________________________________________
(2)A装置是否有误_____________(填“是”或“否”),原因为_______________________
(3)按气流方向连接各仪器,用数字表示接口的连接顺序:①→_________________________;
(4)该套装置有明显缺陷,请予以更正________________________________________________
(5)证明CO存在的实验现象是_________________________________________________;
(6)根据题给的数据,假设反应产生的气体全部排出,并与吸收液充分反应(提示:B、C中澄清石灰水均先变浑浊,后又变澄清),最终D中生成了两种物质,则这两种生成物的化学式及对应的物质的量分别是①_______________,②_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图,请计算出FeCl3、AlCl3的物质的量浓度各为多少? 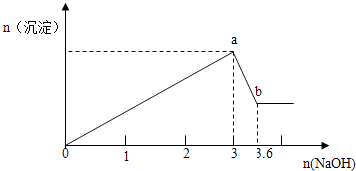
查看答案和解析>>
科目: 来源: 题型:
【题目】配平下列化学方程式(其中(3)用双线桥标出转移的电子数
(1) Cu + HNO3(稀) — Cu(NO3)2 + NO↑ + H2O___________
(2) S+ NaOH— Na2S+ Na2SO3+ H2O_______________
(3) KClO3+ HCl— KCl+ Cl2↑+ H2O_____________
(4) Cr2O72-+ Fe2++ — Cr3++ Fe3++ ,_________________
查看答案和解析>>
科目: 来源: 题型:
【题目】将 Cl2 通入 NaBr 和 NaI 的混合液中,待反应充分后将所得的溶液加热蒸干,并灼烧,最后将得 到的固体冷却、称量.称量所得固体的质量与通入 Cl2 的体积关系如图所示.则原混合液中 NaI 的物 质的量为( )

A. 0.5 mol B. 0.4 mol C. 0.3 mol D. 0.25 mol
查看答案和解析>>
科目: 来源: 题型:
【题目】X,Y,Z,W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法中错误的是( ) ![]()
A.Y的气态氢化物的稳定性较Z的强
B.原子半径:W>Z>Y>X
C.最高价氧化物的水化物酸性W较Z强
D.四种元素的单质中,Z的熔沸点最高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com