
科目: 来源: 题型:
【题目】在硝酸铝和硝酸镁的混合溶液中,逐滴加入稀氢氧化钠溶液,直至过量。下列表示氢氧化钠加入量(X)与溶液中沉淀物的量(Y)的关系示意图中正确的是( )

A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】将mg Al2O3和Fe2O3的混合物溶于100mL盐酸中,然后逐滴加入1mol/LNaOH溶液,其结果如图所示:
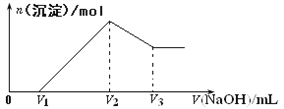
(1)最初加入V1mLNaOH溶液的作用是____________;
(2)盐酸的物质的量浓度是___________________;
(3)若mg混合物中Al2O3和Fe2O3按不同比例进行上述实验(其他条件不变),则V2的值会不会改变__________(填“会”或 “不会”),(V2—V1)的取值范围是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 物质的量可以理解为物质的质量或数量
B. 1mol任何物质所含有的原子数都相同
C. 物质的量是量度物质所含微观粒子多少的一个物理量
D. 国际上规定,0.012kgC中所含有的碳原子数目为1mol
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某纯碱试样中含有 NaCl 杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。
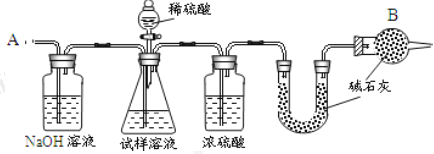
主要实验步骤如下:
①按图组装仪器,并检查装置的气密性;
②将 a g 试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液;
③称量盛有碱石灰的 U 形管的质量,得到 b g;
④从分液漏斗滴入 6 molL-1的硫酸,直到不再产生气体时为止;
⑤从导管 A 处缓缓鼓入一定量的空气;
⑥再次称量盛有碱石灰的 U 型管的质量,得到 c g;
⑦重复步骤⑤和⑥的操作,直到 U 型管的质量基本不变,为 d g;
请填空和回答问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明_________________。
(2)装置中干燥管 B 的作用是______________________。
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果_________(填偏高、偏低或不变)。
(4)步骤⑤的目的是__________________________。
(5)步骤⑦的目的是__________________________。
(6)该试样中纯碱的质量分数的计算式为_______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列是用98%的浓H2SO4(ρ=1.84g/cm3)配制500mL 0.5molL﹣1的稀硫酸的实验操作,请按要求填空:
(1)实验中量取浓硫酸的体积为mL.
(2)如果实验室有10mL、20mL、50mL的量筒,应选规格的量筒最好,如果量取浓硫酸时仰视读数,所配溶液浓度将(填“偏高”、“偏低”或“无影响”) .
(3)将量取的浓硫酸沿烧杯内壁慢慢注入盛有约少量水的烧杯里,并不断搅拌,搅拌的目的是 .
(4)将冷却至室温的上述溶液沿玻璃棒注入中,并用50mL蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液要转入到容量瓶中,并振荡;在转移过程中有少量液体洒在桌子是,则最终所配浓度将(填“偏高”、“偏低”或“无影响”) .
(5)加水至距刻度线1~2cm处,改用加水至刻度线,使溶液的凹液面恰好跟容量瓶刻度线相平,把容量瓶塞好,反复颠倒振荡,摇匀溶液.
查看答案和解析>>
科目: 来源: 题型:
【题目】CO,CH4均为常见的可燃气体.
(1)等体积的CO,CH4在相同的条件下分别完全燃烧,转移的电子数之比为 .
(2)120℃,101kPa下,a mL由CO,CH4组成的混合气体在b mL氧气中完全燃烧后,恢复至原来的温度与压强.
①若混合气体与氧气恰好完全反应,产生b mLCO2 , 则混合气体中CH4的体积分数为%.
②若燃烧后气体体积缩小了 ![]() mL,则a与b的关系为(数学表达式表示).
mL,则a与b的关系为(数学表达式表示).
查看答案和解析>>
科目: 来源: 题型:
【题目】物质A—J间的转化关系如下图所示,A、C为金属氧化物,其中A为红棕色粉末,B、D是生活中常见金属单质,F、J是难溶于水的白色化合物,G、J受热后容易分解

(1)A的化学式是_________,A与B反应的反应类型是________(填四大基本反应类型)。
(2)I→J反应的离子方程式是___________________________________________。
(3)F转化为G的过程中观察到的现象是__________,反应的化学方程式是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用碳棒作电极,在Na+、Cu2+、Cl﹣、SO ![]() 等离子中选出适当离子组成电解质,电解其溶液,写出符合条件的一种电解质的化学式:
等离子中选出适当离子组成电解质,电解其溶液,写出符合条件的一种电解质的化学式:
(1)当阴极放出H2 , 阳极放出O2时,电解质是;
(2)当阴极析出金属,阳极放出O2时,电解质是;
(3)当阴极放出H2 , 阳极放出Cl2时,电解质是;
(4)通过电子的物质的量与阴极析出的金属的物质的量、阳极析出的气体的物质的量之比为4:2:1时,电解质的化学式是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com