
科目: 来源: 题型:
【题目】把镁条投入盛有盐酸的敞口容器中,产生氢气的速率变化如图所示.下列因素中,可能影响该反应的反应速率的因素是( )
①盐酸的浓度 ②镁条的表面积③溶液的温度 ④Cl﹣的浓度.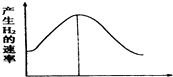
A.①④
B.③④
C.①②③
D.②③
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于物质分类的组合正确的是
组合 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
A | 纯碱 | H3PO4 | CaCO3 | CaO | SO2 |
B | 苛性钠 | HClO | NaCl | Na2O | CO |
C | 熟石灰 | H2SO4 | CuSO45H2O | Na2O2 | CO2 |
D | 烧碱 | HCl | NaHCO3 | Fe2O3 | SO3 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】用下列装置进行相应实验,能达到实验目的是( )
A.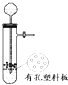 图所示装置用于Cu和浓H2SO4反应制取少量的SO2气体
图所示装置用于Cu和浓H2SO4反应制取少量的SO2气体
B.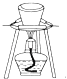 图所示装置用于除去碳酸氢钠固体中的少量碳酸钠
图所示装置用于除去碳酸氢钠固体中的少量碳酸钠
C.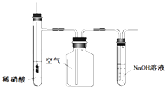 图所示装置用于制备并收集NO气体
图所示装置用于制备并收集NO气体
D.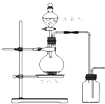 图所示装置制取并收集氨气
图所示装置制取并收集氨气
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.物质发生化学变化都伴随着能量变化
B.任何反应中的能量变化都表现为热量变化
C.伴有能量变化的物质变化都是化学变化
D.热化学方程式的计量数可以表示分子的个数
查看答案和解析>>
科目: 来源: 题型:
【题目】【化学——选修5:有机化学基础】
高聚物G的合成路线如图所示:
其中A苯环上的一氯代物只有两种,两分子F能形成六元环酯。
已知:① ![]()
② 
请回答下列问题:
(1)写出A的结构简式。
(2)B中官能团的名称是 , 按检验顺序写出检验B中官能团的试剂。
(3)C→D的反应类型为;D→E的反应条件为。
(4)写出两分子F形成的六元环酯的结构简式。
(5)写出F→G反应的化学方程式:。
(6)有机物H是F的一种同系物,相对分子质量比F少14,则符合下列条件的H的同分异构体有种。
a.苯环上只有两个取代基且处于对位
b.既能发生水解反应也能与FeCl3溶液反应
写出其中核磁共振氢谱有6个峰,峰面积之比为2∶2 ∶2 ∶2∶1∶1的结构简式。
查看答案和解析>>
科目: 来源: 题型:
【题目】【化学——选修3:物质结构与性质】
第四周期的过渡元素在工业、农业、科学技术以及人类生活等方面有重要作用。请回答:
(1)科学研究表明用TiO2作光催化剂可将废水中CN转化为OCN、并最终氧化为N2、CO2。OCN—中三种元素的第一电离能由大到小的顺序为。与OCN互为等电子体的一种分子为(填化学式)。
(2)Ti(BH4)2是一种储氢材料。写出基态Ti2+的电子排布式 , BH4中B原子的杂化轨道类型是。
(3)[Cr(H2O)4Cl2]Cl·2H2O中Cr的配位数为;
已知CrO5中Cr为+6价,则CrO5的结构式为。
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4 , 该物质晶胞呈正四面体构型。试推测Ni(CO)4的晶体类型为 , Ni(CO)4易溶于下列(填选项字母)中。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(5)FeO、NiO晶体中r(Ni2+)和r(Fe2+)分别为69 pm和78 pm,则熔点NiO FeO(填“>”或“<”),原因为。
(6)硒化锌(SnSe)是一种重要的半导体材料,其晶胞结构如图所示,则该晶胞中硒原子的配位数为;若该晶胞密度为ρ g·cm3 , 硒化锌的摩尔质量为M g/mol。NA代表阿伏加德罗常数,则晶胞参数a为pm。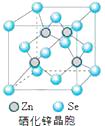
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
反应Ⅰ:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH1=49.58 kJ·mol1
CH3OH(g)+H2O(g) ΔH1=49.58 kJ·mol1
反应Ⅱ:CO2(g)+H2(g) ![]() CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2
反应Ⅲ:CO(g)+2H2(g) ![]() CH3OH(g) ΔH3=90.77 kJ·mol1
CH3OH(g) ΔH3=90.77 kJ·mol1
回答下列问题:
(1)反应Ⅱ的ΔH2=。
(2)反应Ⅲ能够自发进行的条件是(填“较低温度”、“较高温度”或“任何温度”)。
(3)恒温,恒容密闭容器中,对于反应Ⅰ,下列说法中能说明该反应达到化学平衡状态的是。
A.混合气体的密度不再变化
B.混合气体的平均相对分子质量不再变化
C.CO2、H2、CH3OH、H2O的物质的量之比为1∶3∶1∶1
D.甲醇的百分含量不再变化
(4)对于反应Ⅰ,不同温度对CO2的转化率及催化剂的效率影响如图所示,下列有关说法不正确的是______。
A.不同条件下反应,N点的速率最大
B.温度低于250 ℃时,随温度升高乙烯的产率增大
C.M点时平衡常数比N点时平衡常数大
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
(5)若在1 L密闭容器中充入 3mol H2 和1molCO2发生反应Ⅰ,则图中M点时,产物甲醇的体积分数为;该温度下,反应的平衡常数K=;若要进一步提高甲醇的体积分数,可采取的措施有。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列古诗词描述的场景中发生的化学反应不属于氧化还原反应的是
A. 爆竹声中一岁除——黑火药受热爆炸
B. 烈火焚烧若等闲——石灰石分解
C. 蜡烛成灰泪始干——石蜡的燃烧
D. 炉火照天地,红星乱紫烟——铁的冶炼
查看答案和解析>>
科目: 来源: 题型:
【题目】磷的单质及其化合物在生产、生活中有着重要的用途。回答下列问题:
(1)直链低聚磷酸盐的化学式可表示为M(n+2)PnOx(M为+1价金属离子),则x=(用n表示)。
(2)H3PO2及NaH2PO2具有较强还原性,均可将溶液中的银离子还原为银单质,从而可用于化学镀银。
①H3PO2是一元弱酸,写出其电离方程式:。NaH2PO2水溶液显(填“酸性”、“中性”、或者“碱性”)。
②H3PO2中,磷元素的化合价为 , 在碱性条件下,次磷酸盐可用于化学镀银,配平反应的离子方程式: ![]() +Ag+ +
+Ag+ + ![]()
![]() + Ag↓ +。
+ Ag↓ +。
(3)H3PO2可以通过电解的方法制备。工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
①写出阳极的电极反应式;
②分析产品室可得到H3PO2的原因;
③得到1 mol H3PO2的同时,阴极室制得NaOH质量为g。
(4)含磷(主要为H3PO4、磷酸盐等)废水需加入生石灰调节pH将磷元素转化为磷酸的钙盐沉淀并回收。若处理后的废水中c(PO43)=4×107 mol·L1 , 则溶液中c(Ca2+)=mol·L1。(已知Ksp[Ca3(PO4)2]=2×1029)
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种常见的食品添加剂。某兴趣小组用如图所示装罝制备NaNO2并对其性质作如下探究(A中加热装罝已略去)。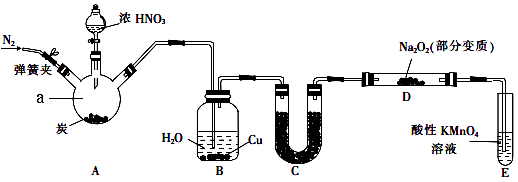
查阅资料可知:
① 2NO+Na2O2 ![]() 2NaNO2;2NO2+Na2O2
2NaNO2;2NO2+Na2O2 ![]() 2NaNO3。
2NaNO3。
② NO能被酸性KMnO4氧化成 ![]() 。
。
③ 在酸性条件下,NaNO2能将I氧化为I2; ![]() 能将I2还原为I ,即I2+2
能将I2还原为I ,即I2+2 ![]()
![]() 2I+
2I+ ![]() 。
。
(1)装置中仪器a的名称为 , A中反应的化学方程式是。
(2)装置B中观察到的主要现象是。
(3)装置C中盛放的试剂是。
(4)装置E的作用是。
(5)A中滴入浓硝酸之前,应先通入N2一段时间,原因是。
(6)为测定所得NaNO2的纯度,准确称取m g NaNO2样品放入锥形瓶中并加入适量水溶解,再加入过量KI溶液并滴入几滴淀粉溶液,然后滴加稀硫酸,用cmol/L Na2S2O3溶液滴定至终点,重复操作2~3次,平均消耗Na2S2O3V mL。滴定终点的现象是。该样品中NaNO2的质量分数为。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com