
科目: 来源: 题型:
【题目】A、B、C、D、E、F、G元素原子序数依次增大.已知B原子最外层有3个未成对电子,C原子最外层电子数与核外电子总数之比为3:4,E与C同主族,F﹣、D+、A+离子的半径逐渐减小,化合物AF常温下为气体,G的基态原子核外M能层填满电子,N能层只有1个电子.据此回答下列问题:
(1)写出D元素基态原子的核外电子排布式;B、C、E三种元素的第一电离能由大到小的顺序是 (用元素符号表示) .
(2)A与C可形成18电子分子,其水溶液中滴入少量氯化铁溶液时有大量气泡逸出,写出该反应的化学方程式 .
(3)某化合物由上述七种元素中的三种元素组成,为常见家用消毒剂的主要成分,其中化学键类型为;该化合物水溶液不呈中性的原因是(用离子方程式表示) .
(4)0.3mol G的低价氧化物能与mol B的最高价氧化物对应水化物的溶液恰好完全反应(设还原产物只有BO).
(5)卫星发射时可用B2A4为燃料,1 mol气态B2A4在适量C2中燃烧,生成B2和气态A2C,放出534 kJ的热量,1 mol液态A2C完全气化需吸收44 kJ热量.请写出气态B2A4在C2中燃烧生成B2和液态A2C时的热化学方程式 .
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室需要0.5mol/L的硫酸溶液480mL,根据溶液的配制情况回答下列问题。
(1)在下图所示仪器中,配制上述溶液肯定不需要的是_________(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是 ___________________________。
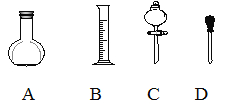
(2)根据计算得知,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为__mL,如果实验室有15mL、20mL、50mL量筒,应选用______ mL量筒最好。
(3)在容量瓶的使用方法中,下列操作不正确的是____________。
A、使用容量瓶前检验是否漏水
B、容量瓶用水洗净后,再用待配溶液洗涤
C、配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1—2cm处,用胶头滴管加蒸馏水至刻度线。
D、配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
E、盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(4)在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度______0.5mol/L(填“大于”“小于”或“等于”)。
(5)该同学在定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度。对所配溶液浓度的影响__________(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】用CO合成甲醇的化学方程式为:CO(g)+2H2(g)CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( ) 
A.温度:T1>T2>T3
B.正反应速率:υ(a)>υ(b)>υ(c)
C.平衡常数:K(b)>K(d)
D.CH3OH的体积分数(a)>(b)>(c)
查看答案和解析>>
科目: 来源: 题型:
【题目】海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)目前国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是____________________(填物理变化、化学变化);
(2)工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”。电解饱和食盐水的化学方程式为___________________________________________;
(3)实验室用MnO2和浓盐酸为原料制备氯气,该反应的化学方程式为_____________,尾气处理的化学方程式为_______________________________________。工业上制备漂白粉的化学方程式________________________________________。
(4)将实验室制的氯气配成新制的氯水含有多种微粒,试用化学方程式解释下列现象。
①将氯水滴加紫色石蕊溶液中,先变红后褪色________________________________。
②将氯水滴入硝酸银溶液中,有白色沉淀生成___________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】I 下列九种物质:①稀硝酸 ②CO ③NH3·H2O ④熔融NaHSO4⑤CaO ⑥Cu ⑦蔗糖⑧Fe2(SO4)3⑨酒精
(1)用序号填空: 属于电解质的是 __________ ;能导电的是_______________ ;
(2)写出④、⑧两种物质在水溶液中的电离方程式:
④______________________________;⑧__________________________________________ 。
II (1)画出S2-的结构示意图_______________________。
(2)质量数为A、中子数为N的离子R2+,该离子的核外电子数为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】NA代表阿伏加德罗常数。下列有关NA的叙述中,正确的是( )
A. 1 mol 任何物质所含的微粒数均为NA
B. 14 g氮气所含的N原子数为NA
C. 标准状况下,22.4 L水所含的H2O分子数为NA
D. 在钠与氧气的反应中,1 mol钠失去电子的数目为2 NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于物质分类正确组合是( )
分类组合 | 碱 | 酸 | 盐 | 氧化物 |
A | Na2CO3 | H2SO4 | NaCl | CO2 |
B | NaOH | HCl | NaHCO3 | H2SiO3 |
C | NaOH | H2CO3 | CaCl2 | SO2 |
D | KOH | NaHSO4 | CaCO3 | CO2 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】除去苯中所含的苯酚,可采用的适宜方法是( )
A.加70℃以上的热水,分液
B.加适量浓溴水,过滤
C.加足量NaOH溶液,分液
D.加适量FeCl3溶液,过滤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com