
科目: 来源: 题型:
【题目】用海水“晒盐”的方法得到的粗盐中,除氯化钠外,还含有氯化镁、氯化钙、硫酸钠等杂质。将此粗盐提纯的部分实验方案如下:
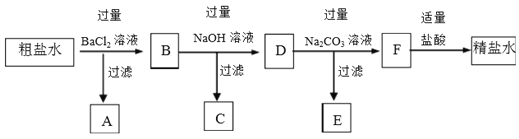
(1)粗盐水中含有的阳离子有_______,阴离子有__________。
(2)加入BaCl2溶液的目的是(用离子方程式表示)_________。
(3)生成沉淀C的离子方程式是______。
(4)D中所含离子有_______。
(5)E的主要成分的化学式是____。
(6)用文字描述加入适量盐酸的目的是________。
(7)某同学认为加入过量K2CO3溶液与加入过量Na2CO3溶液同样可以达到实验目的,这种说法是否合理,请说明理由______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室需要配制1.0mol/LNaCl溶液100mL,按下列操作步骤进行:
(1)选择仪器。
完成本实验所必需的仪器有:电子天平、药匙、烧杯、玻璃棒、胶头滴管、________(选填a、b、c)。

![]()

a b c
(2)计算、称量。
配制该溶液需称取NaCl固体_______g。
(3)溶解。
在该步操作中,某同学将称好的NaCl固体放入烧杯中,加100mL蒸馏水溶解。指出他操作的错误并说明原因______________________。
(4)转移洗涤。
将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁2-3次,洗涤液也注入容量瓶。洗涤烧杯内壁的目的是___________________。
(5)定容摇匀。
将蒸馏水注入容量瓶,液面离容量瓶颈刻度线下1-2厘米时,改用胶头滴管滴加蒸馏水至液面与刻度线相切。盖好瓶塞,反复上下颠倒、摇匀。若摇匀后发现溶液体积低于刻度线,这时应该________。
(6)装瓶保存。将配好的溶液静置一段时间后,倒入指定的试剂瓶,并贴好标签。对该份溶液,标签上应该写___________________。
(7)为精准配制溶液,需要做到:a.保证溶质的质量精准, b.保证溶液的体积精准。以下措施中是为达到a的是____,是为达到b的是______。
①将称好的溶质必须全部放入烧杯中溶解
②转移过程中,不能将溶液洒出
③若定容时滴加蒸馏水超过液面,就需要重新配制溶液。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上炼铁的主要反应为:Fe2O3 + 3CO![]() 2Fe + 3CO2 。
2Fe + 3CO2 。
(1)该反应中氧化剂是______(填化学式),判断依据是________;被氧化的物质是____(填化学式);若反应中消耗了3 mol CO,则生成______mol Fe。
(2)理论上来看,其中CO可用以下______组(选填a、b、c)物质代替,这些物质在反应中的作用都是_______。
a组: H2 、Cl2 、C b组: H2 、Al、C c组:C 、Al、 Cl2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列分离方法正确的是
A. 分离汽油和水可以用结晶的方法
B. 除去氯化钠溶液中的泥沙用分液的方法
C. 分离醋酸(沸点118℃)与乙酸乙酯(沸点77.1℃)用蒸馏的方法
D. 从含有少量氯化钠的硝酸钾溶液中提取硝酸钾用过滤的方法
查看答案和解析>>
科目: 来源: 题型:
【题目】物质A是生产各种塑料的重要单体,工业上采用物质B分解制备物质A的同时释放出氢气,其制备原理是:
B(g)A(g)+H2(g)△H=+125kJmol﹣1
(1)该反应的平衡常数表达式为K= . 随着温度的升高,K值(填“增大”、“减小”或“不变”).
(2)实际生产中常以高温水蒸气作为反应体系的稀释剂(稀释剂不参加反应).物质B的平衡转化率与水蒸气的用量、体系总压强关系如图.
①由图可得出:
结论一:其他条件不变,水蒸气的用量越大,平衡转化率越;
结论二:
②加人稀释剂能影响反应物B的平衡转化率的原因是: .
(3)某些工艺中,在反应的中途加入O2和特定的催化剂,有利于提高B的平衡转化率.试解释其原因: . 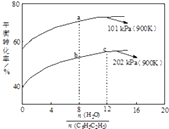
查看答案和解析>>
科目: 来源: 题型:
【题目】某探究小组利用丙酮的溴代反应(CH3COCH3+Br2 ![]() CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系.反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定.在一定温度下,获得如下实验数据:
CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系.反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定.在一定温度下,获得如下实验数据:
实验序号 | 初始浓度c/molL﹣1 | 溴颜色消失所需的时间t/s | ||
CH3COCH3 | HCl | Br2 | ||
① | 0.80 | 0.20 | 0.0010 | 290 |
② | 1.60 | 0.20 | 0.0010 | 145 |
③ | 0.80 | 0.40 | 0.0010 | 145 |
④ | 0.80 | 0.20 | 0.0020 | 580 |
分析实验数据所得出的结论不正确的是( )
A.增大c(CH3COCH3),v(Br2)增大
B.实验②和③的v(Br2)相等
C.增大c(HCl),v(Br2)增大
D.增大c(Br2),v(Br2)增大
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学实验操作中,不正确的是( )
A. 用灯帽盖灭酒精灯的火焰
B. 稀释浓硫酸时,将浓硫酸缓缓加到水中,并不断用玻璃棒搅拌
C. 将固体氢氧化钠直接放在托盘天平上称量
D. 给试管里的固体加热,试管口应稍稍向下倾斜
查看答案和解析>>
科目: 来源: 题型:
【题目】现有下列5种物质:① NO、②浓H2SO4、③浓HNO3、④ NaHCO3、⑤SO2。其中,遇空气变红棕色的是______(填序号,下同);能使蔗糖变黑的是______;能使品红溶液褪色的是_________。受热分解产生CO2的是______,写出该反应化学方程式__________;与铜反应产生红棕色气体的是______,写出该反应化学方程式_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】三草酸合铁酸钾晶体K3[Fe(C2O4)3]3H2O可用于摄影和蓝色印刷.某小组将无水三草酸合铁酸钾在一定条件下加热分解,对所得气体产物和固体产物进行实验和探究.该小组同学查阅资料知,固体产物中铁元素不可能以三价形式存在,而盐只有K2CO3 , 产生的气体中含有CO、CO2 . 请利用实验室常用仪器、用品和以下限选试剂完成验证和探究过程.
限选试剂:①蒸馏水 ②3%H2O2溶液 ③氧化铜 ④1.0 molL﹣1盐酸⑤浓硫酸⑥1.0 molL﹣1NaOH溶液 ⑦澄清石灰水 ⑧0.5 molL﹣1 CuSO4溶液 ⑨2%KSCN溶液 ⑩苯酚溶液
(1)若用一套连续实验装置检验气体产物中CO的存在,并验证检验过程中有CO2生成,应选用的试剂为(按先后顺序把所选试剂的标号填入空格内)
(2)提出合理假设假设1:只有Fe; 假设2:只有FeO; 假设3: .
(3)设计实验方案并实验验证步骤1:取适量固体产物于试管中,加入足量蒸馏水溶解,过滤分离出不溶固体.
步骤2:取少量上述不溶固体放入试管中,加入足量溶液,充分振荡.若固体无明显变化,则假设成立;若有暗红色固体生成,则反应的离子方程式为 .
步骤3:取步骤2所得暗红色固体于试管中,滴加过量 , 振荡后静置.若溶液基本无色,则假设成立;若溶液呈 , 则假设3成立.
(4)问题讨论若固体产物中FeO含量较少,用步骤3方法难以确定.请你设计实验方案证明假设3成立(写出实验的操作步骤、现象与结论): .
(5)拓展与延伸有资料介绍“在含Fe2+的溶液中,先滴加少量新制饱和氯水,然后滴加KSCN溶液,溶液呈红色;若再滴加过量氯水,却发现红色褪去”.假设溶液中的+3价铁还能被氯水氧化为更高价的QUOTE,试写出该反应的离子方程式 .
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室制备苯甲醇和苯甲酸的化学原理是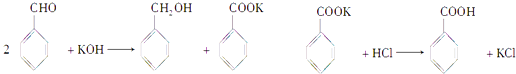
已知苯甲醛易被空气氧化,苯甲醇的沸点为205.3℃;苯甲酸的熔点为121.7℃,沸点为249℃,溶解度为0.34g;乙醚的沸点为34.8℃,难溶于水.制备苯甲醇和苯甲酸的主要过程如下:
苯甲醛 ![]() 白色糊状物
白色糊状物 ![]()
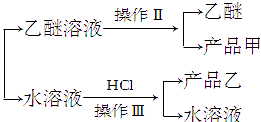
试根据上述信息回答下列问题:
(1)操作Ⅰ的名称是 , 乙醚溶液中所溶主要成分是 .
(2)操作Ⅱ的名称是 , 产品甲是 .
(3)操作Ⅲ的名称是 , 产品乙是 .
(4)如图所示,操作Ⅱ中温度计水银球上沿放置的位置应是(填“a”、“b”、“c”或“d”),该操作中,除需蒸馏烧瓶、温度计外,还需要的玻璃仪器是 , 收集产品乙醚的适宜温度为 . 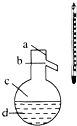
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com