
科目: 来源: 题型:
【题目】已知甲和乙的某些性质如下表所示:
物质 | 熔点(℃) | 沸点(℃) | 密度(g/mL) | 水中的溶解性 |
甲 | -98 | 37.5 | 0.93 | 可溶 |
乙 | -48 | 95 | 0.90 | 可溶 |
现有甲和乙的混合物,进行分离时,可采用的方法是( )
A. 蒸馏 B. 蒸发 C. 过滤 D. 萃取
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室欲用NaOH固体配制1.0 mol/L的NaOH溶液240 mL:
(1)配制溶液时,一般可以分为以下几个步骤:①称量②计算③溶解④倒转摇匀⑤转移⑥洗涤⑦定容⑧冷却。
其正确的操作顺序为___________ ⑤⑥⑤__________。本实验必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、胶头滴管、还有_____________________。
(2)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图,烧杯的实际质量为_________ g。要完成本实验该同学应称出_________ g NaOH。

(3)对所配制的NaOH溶液进行测定,发现其浓度低于1.0mol/L。在溶液配制过程中,下列操作会引起该误差的有_________(填序号)。
A.转移溶解的溶液后没有洗涤烧杯和玻璃棒
B.转移溶液时不慎有少量洒到容量瓶外面
C.容量瓶未干燥就用来配制溶液
D.称量NaOH固体时动作太慢,耗时太长
E.定容后摇匀溶液,发现液面低于刻度线,再加入少量水使液面与刻度线相平
F.定容时仰视刻度线
G.NaOH固体溶解后未经冷却即转移到容量瓶中
(4)氢氧化钠是一种用途十分广泛的重要化工原料,工业上主要通过电解氯化钠饱和溶液的方法![]() 。试用单线桥法标出该反应中电子转移的方向和数目____________________。实验测得,反应中生成的气体在标准状况下的体积为4.48L,则耗氧化剂的物质的量为_________mol。
。试用单线桥法标出该反应中电子转移的方向和数目____________________。实验测得,反应中生成的气体在标准状况下的体积为4.48L,则耗氧化剂的物质的量为_________mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】铅蓄电池的工作原理为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,研读图,下列判断不正确的是( ) 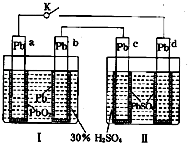
A.K闭合时,d电极反应式:PbSO4+2H2O﹣2e﹣=PbO2+4H++SO42﹣
B.当电路中转移0.2mol电子时,I中消耗的H2SO4为0.2 mol
C.K闭合时,II中SO42﹣向c电极迁移
D.K闭合一段时间后,II可单独作为原电池,d电极为正极
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y.若挤压滴管胶头,使液体Y滴入瓶中,振荡,过一会可见小气球a鼓起.气体X和液体Y不可能是( ) 
A.X是NH3 , Y是水
B.X是SO2 , Y是NaOH浓溶液
C.X是CO2 , Y是稀硫酸
D.X是HCl,Y是NaNO3稀溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子,在溶液中能大量共存,加入H2SO4溶液后既有气体放出又有沉淀生成的一组是( )
A.Ba2+、NO ![]() 、NH
、NH ![]() 、Cl﹣
、Cl﹣
B.Ba2+、HCO ![]() 、NH
、NH ![]() 、NO
、NO ![]()
C.K+、Cu2+、Cl﹣、OH﹣
D.Na+、CO ![]() 、SO
、SO ![]() 、K+
、K+
查看答案和解析>>
科目: 来源: 题型:
【题目】在同温同压下,某有机物和过量Na反应得到V1L氢气,另一份等量的该有机物和足量的NaHCO3反应得到V2L二氧化碳,若V1=V2≠0,则该有机物可能是( )
A.![]()
B.HOOC﹣COOH
C.HOCH2CH2OH
D.CH3COOH
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是( )
A. 同温同压下,相同体积的物质,其物质的量一定相等
B. 任何条件下,等物质的量的甲烷和一氧化碳所含的原子数一定相等
C. 1 L一氧化碳气体一定比1 L氧气的质量小
D. 相同条件下的一氧化碳和氮气,若体积相等,则质量也相等
查看答案和解析>>
科目: 来源: 题型:
【题目】用惰性电极电解CuSO4 和KNO3的混合溶液500mL,经过一段时间后,两极均得到标准状况下11.2L的气体,则原混合液中CuSO4的物质的量浓度为( )
A.0.5 molL﹣1
B.0.8 molL﹣1
C.1.0 molL﹣1
D.1.5 molL﹣1
查看答案和解析>>
科目: 来源: 题型:
【题目】氟在自然界中常以CaF2的形式存在.
(1)下列关于CaF2的表述正确的是 .
a.Ca2+与F﹣间仅存在静电吸引作用
b.F﹣的离子半径小于Cl﹣ , 则CaF2的熔点高于CaCl2
c.阴阳离子比为2:1的物质,均与CaF2晶体构型相同
d.CaF2中的化学键为离子键,因此CaF2在熔融状态下能导电
(2)CaF2难溶于水,但可溶于含Al3+的溶液中,原因是(用离子方程式表示).
已知AlF63﹣在溶液中可稳定存在.
(3)F2通入稀NaOH溶液中可生成OF2 , OF2分子构型为 , 其中氧原子的杂化方式为
(4)F2与其他卤素单质反应可以形成卤素互化物,例如ClF3、BrF3等.已知反应Cl2(g)+3F2(g)═2ClF3(g)△H=﹣313kJmol﹣1 , F﹣F键的键能为159kJmol﹣1 , Cl﹣Cl键的键能为242kJmol﹣1 , 则ClF3中Cl﹣F键的平均键能为kJmol﹣1 . ClF3的熔、沸点比BrF3的(填“高”或“低”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com