
实验室欲配制0.1mol/L NaOH溶液并进行有关性质实验,请据此回答下列问题
(1)实验时,若配制上述溶液500mL,应用托盘天平称取固体的质量为
2.0
2.0
g.
(2)在配制NaOH溶液时需用的玻璃仪器主要有量筒、烧杯、玻璃棒、
500mL容量瓶
500mL容量瓶
、
胶头滴管
胶头滴管
.
(3)若实验过程中遇到下列情况,则会造成所配溶液的浓度偏低的是
ab
ab
.(填字母)
a.加水时越过刻度线 b.未洗涤烧杯和玻璃棒
c.容量瓶内壁附有水珠而未干燥处理 d.定容时俯视刻度线
(4)向VmL上述浓度的NaOH溶液中,通入一定量的CO
2后,然后向该溶液中逐滴中入1mol?L
-1的盐酸,所加入盐酸溶液的体积与产生CO
2的体积关系如图所示:
①当加入35mL盐酸溶液时,产生二氧化碳的物质的量为
0.01
0.01
mol;
②计算所取氢氧化钠溶液的体积V=
450
450
mL.
(5)取上述氢氧化钠溶液200mL,加入足量的铝,该反应的化学方程式为
2Al+2NaOH+6H2O═2Na[Al(OH)4]+3H2↑
2Al+2NaOH+6H2O═2Na[Al(OH)4]+3H2↑
,反应中参与反应的氧化剂的物质的量为
0.06
0.06
.

 实验室欲配制0.1mol/L NaOH溶液并进行有关性质实验,请据此回答下列问题
实验室欲配制0.1mol/L NaOH溶液并进行有关性质实验,请据此回答下列问题 有如图实验装置,其中a、b、c为弹簧夹.
有如图实验装置,其中a、b、c为弹簧夹.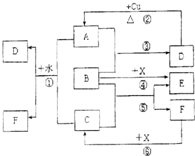 已知A~F是中学化学中常见物质,其中A、C、E为气体,B、D为液体,D是一种不挥发性酸,其浓溶液有强氧化性,F的溶液与X共热通常用于实验室制备单质C,X是一种黑色粉末,B分子中有18个电子,实验室常用B和X制备单质E.反应中部分生成物已略去.试回答下列问题:
已知A~F是中学化学中常见物质,其中A、C、E为气体,B、D为液体,D是一种不挥发性酸,其浓溶液有强氧化性,F的溶液与X共热通常用于实验室制备单质C,X是一种黑色粉末,B分子中有18个电子,实验室常用B和X制备单质E.反应中部分生成物已略去.试回答下列问题: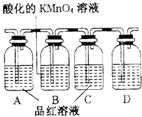 中学常见的某反应的化学方程式为A+B→C+D+H2O(未配平,反应条件略去).请回答下列有关问题.
中学常见的某反应的化学方程式为A+B→C+D+H2O(未配平,反应条件略去).请回答下列有关问题.