
科目: 来源: 题型:
【题目】为研究A的组成与结构,某同学进行了如下实验:
实 验 步 骤 | 实 验 结 论 |
(i)将9.0g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过足量的浓硫酸和碱石灰,发现两者分别增重5.4g和13.2g. | (i)A的实验式为 . |
(ii)通过质谱法测得其相对分子质量为90. | (ii)A的分子式为 |
(iii)另取9.0g A,跟足量的NaHCO3粉末反应,生成2.24L CO2(标准状况),若与足量金属钠反应则生成2.24L H2(标准状况). | (iii)A中含有的官能团名称为 . |
(iv)A的核磁共振氢谱有四组吸收峰,其峰面积之比为2:2:1:1. | (iv)综上所述,A的结构简式为 . |
查看答案和解析>>
科目: 来源: 题型:
【题目】氢能是一种极具发展潜力的清洁能源.以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法.其反应过程如图所示:
完成下列填空
(1)反应Ⅰ的化学方程式是 . 反应Ⅰ得到的产物用I2进行分离.该产物的溶液在过量I2的存在下会分成两层﹣﹣含低浓度I2的H2SO4层和高浓度的I2的HI层.
(2)根据上述事实,下列说法正确的是(选填序号).a.两层溶液的密度存在差异
b.加I2前,H2SO4溶液和HI溶液不互溶
c.I2在HI溶液中比在H2SO4溶液中易溶
(3)辨别两层溶液的方法: ,
(4)经检测,H2SO4层中c(H+):c(SO ![]() )=2.06:1.其比值大于2的原因是 . 反应Ⅱ:2H2SO4(l)→2SO2(g)+O2(g)+2H2O(g)﹣1100kJ 它由两步反应组成:
)=2.06:1.其比值大于2的原因是 . 反应Ⅱ:2H2SO4(l)→2SO2(g)+O2(g)+2H2O(g)﹣1100kJ 它由两步反应组成:
i.H2SO4(l)→SO3(g)+H2O(g)﹣177kJ ii.SO3(g)分解.
L(L1、L2),X可分别代表压强或温度.图2表示L一定时,ii中SO3(g)的平衡转化率随X的变化关系.
(5)X代表的物理量是 , 推断的依据是 .
(6)判断L1和L2的大小,并简述理由 .
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度时,在 2L 密闭容器中气态物质 X 和 Y 反应生成气态物质 Z,它们的物质的量随时间的变化如图所示,则下列说法正确的是(注:转化率=某反应物变化的浓度除它的起始浓度)

A. 反应的化学方程式是 X+2Y = 2Z
B. 该反应达到平衡时反应物 X 的转化率α等于 55%
C. 该反应在 0-3min 时间内产物 Z 的平均反应速率 0.083mol·L-1·min-1
D. 其他条件不变,升高温度,若正反应速率增大,则逆反应速率将减小
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:N2(g)+3H2(g) ![]() 2NH3(g) ΔH=-92.4 kJ·molˉ1。起始反应物为 N2 和 H2物质的量之比为 1︰3,且总物质的量不变,在不同压强和温度下,反应达到平衡时 体系中 NH3 的物质的量分数如下表:
2NH3(g) ΔH=-92.4 kJ·molˉ1。起始反应物为 N2 和 H2物质的量之比为 1︰3,且总物质的量不变,在不同压强和温度下,反应达到平衡时 体系中 NH3 的物质的量分数如下表:
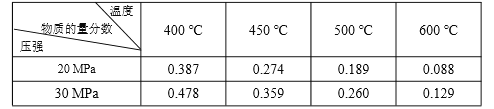
下列说法正确的是
A. 体系中 NH3 的物质的量分数越大,则正反应速率越大
B. 反应达到平衡时,N2 和 H2 的转化率之比均为 1
C. 反应达到平衡时,放出的热量均为 92.4 kJ
D. 600 ℃,30 MPa 下反应达到平衡时,生成 NH3 的物质的量最多
查看答案和解析>>
科目: 来源: 题型:
【题目】1.52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况).向反应后的溶液中加入1.0mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是( )
A.该浓硝酸中HNO3的物质的量浓度是12.0 mol/L
B.该合金中铜与镁的物质的量之比是2:1
C.NO2和N2O4的混合气体中,N2O4的体积分数是20%
D.得到2.54g沉淀时,加入NaOH溶液的体积是6.0 mL
查看答案和解析>>
科目: 来源: 题型:
【题目】已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+ . 现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中正确的是( ) 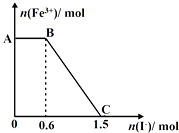
A.开始加入的K2Cr2O7为0.45mol
B.图中AB段的氧化剂为K2Cr2O7
C.图中BC段发生的反应为Fe3++2I﹣→Fe2++I2
D.K2Cr2O7可与FeSO4反应的物质的量为3:1
查看答案和解析>>
科目: 来源: 题型:
【题目】广东正在建设成为海洋强省。下列说法不正确的是( )
A.从海带中提取碘单质的过程涉及氧化还原反应
B.往淡水中加入NaCl等配成人造海水,可用于海产品的长途运输
C.赤潮主要是由工农业生产和生活废水引起沿海水域的富营养化而造成的
D.海洋经济专属区的资源开发可获得Fe、Co、K Au、Mg、B等金属
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的同周期元素,已知A、B、E 3种原子最外层共有11个电子,且这3种元素的最高价氧化物对应水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号: A ___,B____,C____,D____,E________。
(2)写出A、B两元素最高价氧化物对应水化物相互反应的化学方程式:_____________________________。
(3)比较C、D的最高价氧化物对应水化物的酸性:_____________(用化学式表示) 。
(4)用离子方程式表示实验室制取E的单质的原理:____________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质,前者属于电解质,后者属于非电解质的是( )
A. NaCl 晶体、 BaSO4 B. 液态的醋酸、酒精
C. 铜、二氧化硫 D. 熔融的 KNO3、硫酸溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com