
科目: 来源: 题型:
【题目】按要求完成下列问题
(1)镁原子的结构示意图_________________。
(2)氧化钠的电子式__________________。
(3)Si元素元素周期表中的位置在__________________________。
(4)在原子序数1~20号的元素中,最高价氧化物对应的水化物中碱性最强的是_____(用化学式表示)
(5)元素周期表中最高价氧化物对应水化物酸性最强的是________________(用化学式表示)
(6)短周期元素中,族序数为次外层电子数2倍的元素是_________________。(用元素符号表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列能正确表示热化学方程式中△H的含义的是( )
A.H2SO4(aq)+Ba(OH)2(aq)═BaSO4(s)+2H2O(l)△H(中和热)
B.![]() H2SO4(浓)+NaOH(aq)═
H2SO4(浓)+NaOH(aq)═ ![]() Na2SO4(aq)+H2O(l)△H(中和热)
Na2SO4(aq)+H2O(l)△H(中和热)
C.2H2(g)+O2(g)═2H2O(l)△H (燃烧热)
D.CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H(燃烧热)
查看答案和解析>>
科目: 来源: 题型:
【题目】某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行试验(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
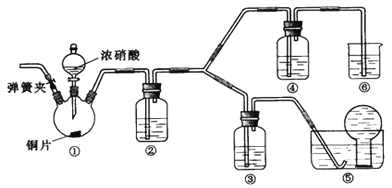
可选药品:浓硝酸、3mol/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应![]()
(1)装置①中发生反应的化学方程式是__________
(2)滴加浓硝酸之前的操作是检验装置的气密性,加入药品,打开弹簧夹通入_________气体(填化学式)一段时间,关闭弹簧夹,将装置⑤中导管末端伸入倒置的烧瓶内。
(3)实验应避免有害气体排放到空气中,装置③中盛放的药品是_________;装置⑥中盛放的药品是_________。
(4)装置②中盛放的药品是_________;该装置的作用是_______________________。
(5)该小组得出的结论所依据的试验现象是__________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】右图曲线a表示放热反应 2X(g)+Y(g)2Z(g) 进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( ) 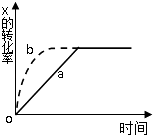
A.加催化剂
B.加大X的投入量
C.升高温度
D.增大体积
查看答案和解析>>
科目: 来源: 题型:
【题目】高纯碳酸锰在电子工业中有重要的应用,湿法浸出软锰矿(主要成分为MnO2 , 含少量Fe、Al、Mg等杂质元素)制备高纯碳酸锰的实验过程如下: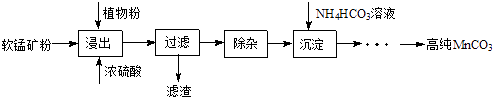
(1)浸出:浸出时温度控制在90℃~95℃之间,并且要连续搅拌3小时的目的是 , 植物粉的作用是 .
(2)除杂:①向浸出液中加入一定量的碳酸锰矿,调节浸出液的pH为3.5~5.5;②再加入一定量的软锰矿和双氧水,过滤;
③…
操作①中使用碳酸锰调pH的优势是;操作②中加入双氧水不仅能将Fe2+氧化为Fe3+ , 而且能提高软锰矿的浸出率.写出双氧水提高软锰矿浸出率的离子方程式 .
(3)制备:在30℃~35℃下,将碳酸氢铵溶液滴加到硫酸锰净化液中,控制反应液的最终pH在6.5~7.0,得到MnCO3沉淀.温度控制35℃以下的原因是;该反应的化学方程式为;生成的MnCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是 .
(4)计算:室温下,Ksp(MnCO3)=1.8×10﹣11 , Ksp(MgCO3)=2.6×10﹣5 , 已知离子浓度小于1.0×10﹣5molL﹣1时,表示该离子沉淀完全.若净化液中的c(Mg2+)=10﹣2mol/L,试计算说明Mg2+的存在是否会影响MnCO3的纯度.
查看答案和解析>>
科目: 来源: 题型:
【题目】依据图中氮元素及其化合物的转化关系,回答问题:
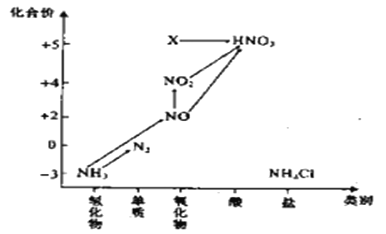
(1)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为________________________________________________________________。
(2)氮氧化物对大气污染主要的危害是____________________。(填一点即可)
(3)若要将NH3→N2,从原理上看,下列试剂可行的是_______________。
A.O2 B.Na
C.NH4Cl D.NO2
(4)图中X转化为HNO3的化学方程式为:____________________________________。
(5)图中在标准状况下将NO2、NO、O2混合并充满容器,将该容器倒置于水中,气体完全溶解,无气体剩余,若产物也不扩散,则所得溶液的物质的量浓度M,其数值大小范围为___________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】苯酚是一种重要的化工原料.以苯酚为主要起始原料,经下列反应可制得香料M和高分子化合物N.(部分产物及反应条件已略去)
(1)由苯酚生成A的化学方程式是 .
(2)已知C的分子式为C5H12O,C能与金属Na反应,C的一氯代物有2种,与C含有相同官能团的同分异构共有种,C的结构简式是;
(3)B与C反应的化学方程式是 .
(4)由苯酚生成D的化学方程式是由D生成N的反应类型是
(5)以苯酚为基础原料也可以合成防腐剂F.经质谱分析F的相对分子质量为152,其中氧元素的质量分数为31%,F完全燃烧只生成CO2和H2O.则F的分子式是 . 已知:①芳香族化合物F能与NaHCO3溶液反应,且不能发生水解反应;
②F的核磁共振氢谱显示其分子中含有4种氢原子;
③分子结构中不存在“﹣O﹣O﹣”的连接方式.F的结构简式是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于微量元素的叙述,错误的是 ( )
A.微量元素是细胞中含量很少的元素
B.微量元素的含量越多对生物体的生命活动就越有利
C.微量元素是维持正常生命活动不可缺少的元素
D.Mn、B、Mo都属于微量元素
查看答案和解析>>
科目: 来源: 题型:
【题目】2020年的新型冠状病毒中,口罩和医用酒精在防疫工作中起到重要作用,医用口罩由三层无纺布制成,无纺布的主要原料是聚丙烯树脂。下列说法正确的是( )
A.84消毒液、二氧化氯泡腾片可作环境消毒剂
B.聚丙烯树脂属于合成无机高分子材料
C.医用酒精中乙醇的体积分数为 95%
D.抗病毒疫苗冷藏存放的目的是避免蛋白质盐析
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com