
科目: 来源: 题型:
【题目】《本草纲目》中的“石碱”条目下写道:“采蒿蓼之属,晒干烧灰,以水淋汁,久则凝淀如石,浣衣发面,亦去垢发面。”这里的“石碱”是指( )
A.KOHB.KAl(SO4)2
C.KHCO3D.K2CO3
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是元素周期表的部分,针对表中的10种元素,用元素符号或化学式回答相关问题:
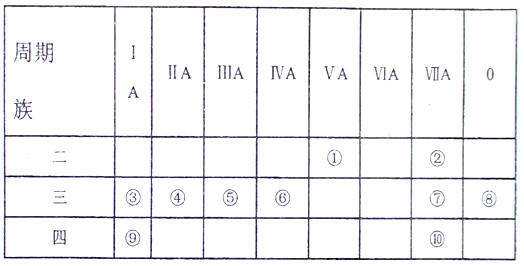
(1)画出④的阳离子结构示意图_________。
(2)这些元素中的最高价氧化物对应的水化物中,酸性最强的是______,碱性最强的是_____。
(3)将⑦单质通入③与⑩组成的化合物的水溶液中,发生反应的离子方程式为_________。
(4)写出下列物质的电子式:
①形成的单质_________ ②与⑨形成的物质_________
用电子式表示④与⑦所组成物质的形成过程_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用废铅蓄电池的铅泥(PbO、Pb及PbSO4等)可制备精细无机化工产品﹣3PbOPbSO4H2O (三盐),主要制备流程如下:
(1)步骤①PbSO4转化为难溶PbCO3的离子方程式为 .
(2)滤液1和滤液3经脱色、蒸发、结晶可得到的副产品为(写化学式).
(3)步骤③酸溶时,其中的铅与硝酸生成Pb(NO3)2及NO的离子方程式为;滤液2中溶质主要成分为(写化学式).
(4)步骤⑥合成三盐的化学方程式为 .
(5)步骤⑦洗涤操作时,检验沉淀是否洗涤完全的方法是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、L、M、R、Q是短周期主族元素,部分信息如下表所示:
X | Y | Z | M | R | Q | |
原子半径 | 0.186 | 0.074 | 0.099 | 0.143 | ||
主要化合价 | -4,+4 | -2 | -1,+7 | +3 | ||
其他 | 阳离子无核外电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
(1)X和M的原子可构成18电子的分子,该分子的结构式为_______ .
(2)Z与Q相比,金属性较强的是_______ (用元素符号表示),下列事实能证明一结论的是_______ (填字母序号)。
a.Q的熔点比Z的熔点高,Q的硬度比Z的硬度大
b.Z与冷水反应迅速,而Q与冷水几乎不反应
c.Z的最高价氧化物对应水化物是强碱,而Q的最高价氧化物对应水化物具有两性
(3)与Y元素同主族的短周期元素E在自然界中存在多种核素,它们之间的关系互为_______,其中用于测定一些文物年代的核素的符号为_______ 。
(4)写出Z2M2的电子式:_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验操作叙述正确的是( )
A. 萃取操作必须在漏斗中进行
B. 振荡试管中液体时,手拿住试管,用手腕甩动
C. 用剩的药品应收集起来,放回原试剂瓶中
D. 称量物质时,先取小砝码,再依次取较大的砝码
查看答案和解析>>
科目: 来源: 题型:
【题目】把与下列元素有关性质相符的曲线标号填入相应空格中:
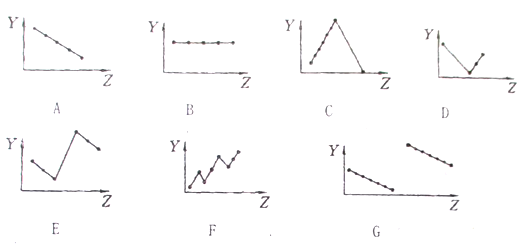
(1)第IIA族元素的价电子数_________;
(2)第三周期元素的最高化合价有_______ ;
(3)碱金属单质熔点_______ ;
(4)第三周期离子Na+、Mg2+、A13+、P3-、S2-、Cl-的离子半径_______ ;
(5)第二、三周期元素随原子序数递增原子半径的变化_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,纯水中的c(H+)=2.0×10﹣7mol/L,此时溶液的c(OH﹣)=mol/L;若温度不变,滴入稀盐酸使c(H+)=5.0×10﹣4mol/L,则溶液中,由水电离产生的c(H+)=mol/L,此时温度25℃(填“高于”、“低于”或“等于”).
查看答案和解析>>
科目: 来源: 题型:
【题目】氮可形成多种气态氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是 ![]() 和
和 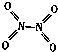 .实验测得N﹣N键的键能为167kJmol﹣1 , NO2中氮氧键的键能为 466kJmol﹣1 , N2O4中氮氧键的键能为438.5kJmol﹣1 .
.实验测得N﹣N键的键能为167kJmol﹣1 , NO2中氮氧键的键能为 466kJmol﹣1 , N2O4中氮氧键的键能为438.5kJmol﹣1 .
(1)写出N2O4转化NO2为的热化学方程式 .
(2)对反应N2O4(g)2NO2(g),在温度T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.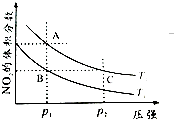
①A、C两点的反应速率v(A)v(C)(填“>”“=”或“<”).
②B、C两点的气体平均相对分子质量M(B)M(C)(填“>”、“=”或“<”).
③由状态B到达状态A可用的方法是 .
④A点气体的颜色比C点(填“深”、“浅”或“相同”),原因是 .
(3)在100℃时,将0.40mol的NO2气体充入2L的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到下表所示数据.
时间/s | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
①在上述条件下,从反应开始直至20s时,v(NO2)=molL﹣1s﹣1 .
②若在相同的情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,N2O4的起始浓度应是molL﹣1 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列变化过程与能量的说法中正确的是( )
A.中和反应是吸热反应
B.燃烧属于放热反应
C.化学键断裂放出能量
D.吸热反应中,反应物总能量大于生成物总能量
查看答案和解析>>
科目: 来源: 题型:
【题目】下列措施是为了降低化学反应速率的是( )
A.铁粉代替铁钉与稀硫酸反应制取氢气
B.双氧水制氧气时加入少量二氧化锰
C.镁和水反应时,适当进行加热
D.食品放在冰箱中贮藏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com