
科目: 来源: 题型:
【题目】已知25℃时有关弱酸的电离平衡常数:
弱酸化学式 | CH3COOH | HCN | H2CO3 |
电离平衡常数(25℃) | 1.8×10﹣5 | 4.9×10﹣10 | K1=4.3×10﹣7 |
则下列有关说法正确的是( )
A.等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Ma2CO3)>pH(CH3COONa)
B.amol/L HCN 溶液与b mol/L NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN﹣),则一定a大于b
C.冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离(程)度、c(H+)均先增大后减小
D.NaHCO3和Na2CO3的混合溶液中,一定存在:c(Na+)+c(H+)=c(OH﹣)+c(HCO3﹣)+2c(CO ![]() )
)
查看答案和解析>>
科目: 来源: 题型:
【题目】13C—NMR(核磁共振)可用于含碳化合物的结构分析,表示的碳原子
A. 核外有13个电子,核内有13个质子B. 核内有6个质子,核外有7个电子
C. 质量数为13,原子序数6,核内有7个质子D. 质量数为13,原子序数6,核内有7个中子
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外活动小组利用如图所示的装置进行乙醇的催化氧化实验并制取乙醛(试管丙中用水吸收产物),图中铁架台等固定装置已略去.实验时,先加热玻璃管中的铜丝,约1min后鼓入空气.请填写下列空白: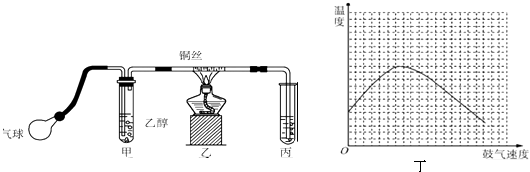
(1)检验乙醛的试剂是(填字母).
A.银氨溶液
B.碳酸氢钠溶液
C.新制Cu(OH)2
D.氧化铜
(2)乙醇发生催化氧化反应的化学方程式为: .
(3)实验时,常常将甲装置浸在70~80℃的水浴中,目的是 , 由于装置设计上的缺陷,实验进行时可能会 .
(4)反应发生后,移去酒精灯,利用反应自身放出的热量可维持反 应继续进行.进一步研究表明,鼓气速度与反应体系的温度关系曲线如图丁所示.试解释鼓气速度过快,反应体系温度反而下降的原因 , 该实验中“鼓气速度”这一变量你认为可用来估量.
(5)该课外活动小组偶然发现向溴水中加入乙醛溶液,溴水褪色.该同学为解释上述现象,提出两种猜想:①溴水将乙醛氧化为乙酸;②溴水与乙醛发生加成反应.请你设计一个简单的实验,探究哪一种猜想正确? .
查看答案和解析>>
科目: 来源: 题型:
【题目】已知25℃时Agl饱和溶液中c(Ag+)为1.22×10﹣6mol/L,AgCl的饱和溶液中c(Ag+)为1.25×10﹣6mol/L.若在5mL含有KCl和KI各为0.01mol/L的溶液中,加入8mL0.01mol/LAgNO3溶液,这时溶液中所含溶质的离子浓度大小关系正确的是( )
A.c(K+)>c(NO![]() )>c(Cl﹣)>c(Ag+)>c(I﹣)
)>c(Cl﹣)>c(Ag+)>c(I﹣)
B.c(K+)>c(NO![]() )>c(Ag+)>c(Cl﹣)>c(I﹣)
)>c(Ag+)>c(Cl﹣)>c(I﹣)
C.c(NO3﹣)>c(K+)>c(Ag+)>c(Cl﹣)>c(I﹣)
D.c(K+)>c(NO ![]() )>c(Ag+)=(Cl﹣)+c(I﹣)
)>c(Ag+)=(Cl﹣)+c(I﹣)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 将AgBr放入水中不能导电,故AgBr不是电解质
B. CO2溶于水得到的溶液能导电,所以CO2是电解质
C. 熔融的金属能导电,所以金属是电解质
D. 固态的NaCl不导电,但 NaCl是电解质
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组取一定质量的FeSO4固体,利用下图装置进行实验.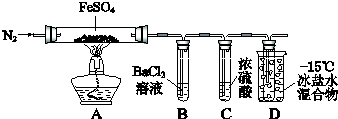
实验过程 | 实验现象 | |
① | 通入一段时间N2 , 加热 | A中固体变为红棕色,B中有白色沉淀,D试管中有无色液体 |
② | 用带有火星的木条靠近装置D的导管口 | 木条复燃 |
③ | 充分反应,停止加热,冷却后,取A中固体,加盐酸 | 固体溶解,溶液呈黄色 |
④ | 将③所得溶液滴入D试管中 | 溶液变为浅绿色 |
已知:SO2 熔点﹣72℃,沸点﹣10℃;SO3熔点16.8℃,沸点44.8℃.
(1)实验③反应的离子方程式是 .
(2)分解过程除产生使木条复燃的气体外,仅由A中固体颜色变化推测,还一定有气体,依据是 .
(3)实验④反应的离子方程式是 .
(4)某同学依据B中的现象,认为FeSO4分解一定有SO3生成.你认为是否正确,原因是(用必要的文字和化学方程式解释)
查看答案和解析>>
科目: 来源: 题型:
【题目】化学反应N2(g)+3H2(g) ![]() 2NH3(g)的能量变化如图所示(△E为能量变化值,a、b、c均为正值)。下列相关说法正确的是
2NH3(g)的能量变化如图所示(△E为能量变化值,a、b、c均为正值)。下列相关说法正确的是

A. 此反应为吸热反应
B. 1mol N+3mol H中的总能量等于1mol NH3中的能量
C. 1mol NH3(l)转变为1mol NH3(g)需要吸收c kJ能量
D. 反应N2(g)+3H2(g) ![]() 2NH3(g)的能量变化值为a+b
2NH3(g)的能量变化值为a+b
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.
(1)Ⅰ.将钠、钾、镁、铝各1mol分别投入到足量的0.1molL﹣1的盐酸中,试预测实验结果:与盐酸反应最剧烈,与盐酸反应最慢.
(2)将NaOH溶液与NH4Cl溶液混合生成NH3H2O,从而验证NaOH的碱性大于NH3H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由: , .
(3)Ⅱ.利用如图装置可以验证非金属性的变化规律.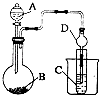
仪器A的名称为 , 干燥管D的作用是 .
(4)实验室中现有药吕Na2S、KMnO4、浓盐酸、MnO2 , 请选择合适药品设计实验验证氯的非金属性大于硫;装置A、B、C中所装药品分别为、、 . 装置C中实验现象为有淡黄色沉淀生成,离子方程式为 .
(5)若要证明非金属性:C>Si,则A中 , B中加Na2CO3、C中加 , 观察到C中溶液的现象为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下图为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素原子的核电荷数为X元素的2倍。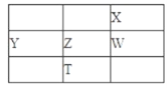
下列说法正确的是
A. X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次递增
B. Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增
C. YX2晶体熔化时需克服离子键
D. 根据元素周期律,可以推测T元素的单质具有半导体特性,T2X3具有氧化性和还原性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com