
科目: 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列描述正确的是

A. 反应的化学方程式为X(g)+Y(g)===Z(g)
B. 反应开始到10s时Y的转化率为79.0%
C. 反应开始到10s,X的物质的量浓度减少了0.79mol/L
D. 反应开始到10s,用Z表示的反应速率为0.158mol/(L·s)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.氢氧化钡溶液与稀硫酸反应:Ba2++SO ![]() +H++OH﹣=BaSO4↓+H2O
+H++OH﹣=BaSO4↓+H2O
B.淀粉碘化钾溶液在空气中变蓝:4I﹣+O2+2H2O=4OH﹣+2I2
C.磁性氧化铁溶于盐酸:Fe2O3+6H+=2Fe3++3H2O
D.用氨水吸收足量的SO2气体:OH﹣+SO2=HSO ![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】如图甲、乙是电化学实验装置.
(1)若甲、乙两烧杯中均盛有饱和NaCl溶液.①甲中石墨棒上的电极反应式 , 电子的移动方向为 .
②乙中总反应的离子方程式为 , Cl﹣移向电极(填Fe或C).
③将湿润的淀粉﹣KI试纸放在乙烧杯上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2 . 若反应中Cl2和I2的物质的量之比为5:1,且生成两种酸,该反应的化学方程式为: .
(2)如果起始时乙中盛有200mL pH=5的CuSO4溶液(25℃),一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入CuO的质量为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列方法中不能证明2HI(g)![]() H2(g)+I2(g)已达到平衡状态的是
H2(g)+I2(g)已达到平衡状态的是
A. 温度和体积一定时,某一生成物浓度不再变化
B. 一个H-H键断裂的同时有两个H-I键断裂
C. 单位时间内生成nmolH2的同时生成nmolHI
D. 温度和体积一定时混合气体的颜色不再变化
查看答案和解析>>
科目: 来源: 题型:
【题目】科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如右图所示),与白磷分子相似。已知断裂1molN-N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则下列说法不正确的是

A. N4与N2互为同素异形体
B. 1molN4气体转化为N2时要吸收724kJ能量
C. N4变成N2是化学变化
D. N4分子中有6个共价键
查看答案和解析>>
科目: 来源: 题型:
【题目】最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:

下列说法正确的是
A. 状态I→状态Ⅲ表示CO与O2反应生成CO2的过程
B. CO和O生成CO2是吸热反应
C. 状态I→状态Ⅲ表示CO与O反应生成CO2的过程
D. 在该过程中,CO断键形成C和O
查看答案和解析>>
科目: 来源: 题型:
【题目】【题目】某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成碳族元素中C与Si的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律。A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。

(1)写出对应装置中选用的物质:A______________________,B________________,C________________;
(2)其中装置B中所盛试剂的作用为___________________;C中反应的离子方程式为_______________________________。
(3)乙同学的实验原理是________________________________________________;写出B处的离子方程式:________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图表示由元素周期表中1~20号且不同主族元素组成的单质及化合物之间转化关系(产物中的水已略去).其中A为黄绿色气体单质;在实验室中,常用固体B和固体C加热制取刺激性气味气体F;F与G的组成元素相同.G与I分子所含电子数相同.请回答:
(1)写出B、I的化学式B , I .
(2)反应④的实验现象为;写出F的一种具体用途 .
(3)向具有漂白作用的D溶液加入I的浓溶液有A生成,其反应的离子方程式为: .
(4)写出反应③的化学方程式 .
查看答案和解析>>
科目: 来源: 题型:
【题目】有某种含有少量FeCl2杂质的FeCl3样品.现要测定其中铁元素的质量分数,实验采用下列步骤进行:①准确称量mg样品(在2~3g范围内);
②向样品中加入10mL 6molL﹣1的盐酸,再加入蒸馏水,配制成250mL溶液;
③量取25mL操作②中配得的溶液,加入3mL氯水,加热使其反应完全;
④趁热迅速加入10%氨水至过量,充分搅拌,使沉淀完全;
⑤过滤,将沉淀洗涤后,移至坩埚,灼烧、冷却、称重,并重复操作至恒重.
试回答下列问题:
(1)溶解样品时,要加入盐酸,原因是 .
(2)加入氯水后,反应的离子方程式为 .
(3)若不用氯水,可用下列试剂中的代替(填序号).
A.H2O2
B.碘水
C.NaClO
(4)步骤⑤中检验沉淀是否洗净的方法是 .
(5)若坩埚质量为W1g,坩埚及灼烧后的固体总质量为W2g,样品中铁元素的质量分数为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】铜、铬都是用途广泛的金属.工业上利用电镀污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收金属铜和铬的流程如图甲,已知:部分物质沉淀的pH如表:
Fe3+ | Cu2+ | Cr3+ | |
开始沉淀pH | 2.1 | 4.7 | 4.3 |
完全沉淀pH | 3.2 | 6.7 | a |
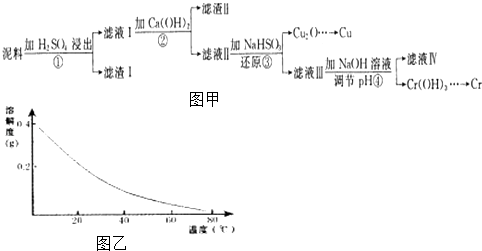
CaSO4的溶解度曲线如图乙,请回答下列问题:
(1)滤液I中所含溶质主要有(填化学式).
(2)第②步操作中,先加人Ca(OH)2调节溶液的pH,调节范围为 , 然后将浊液加热至80℃趁热过滤,所得滤渣Ⅱ的成分为 .
(3)第③步操作中,发现除了生成砖红色沉淀外,还产生了无色刺激性气味的气体.写出该步骤中发生反应的离子方程式
(4)当离子浓度≤1×10﹣5molL﹣1l时,可以认为离子沉淀完全.第④步操作中,若要使Cr3+完全沉淀,则室温下溶液中a的最小值为 . (已知Kap[Cr(OH)3]=6.3×10﹣31 , ![]() ≈4.0;lg4=0.6)
≈4.0;lg4=0.6)
(5)Cr(OH)3受热分解为Cr2O3 , 用铝热法可以冶炼金属铬.写出铝热法炼铬的化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com