
科目: 来源: 题型:
【题目】如图是一种综合处理SO2废气的工艺流程。下列说法正确的是( )

A. 向溶液B中滴加KSCN溶液,溶液一定不会变红色
B. 溶液A转化为溶液B发生反应的离子方程式为:2Fe3++2H2O+SO2===2Fe2++SO![]() +4H+
+4H+
C. 溶液酸性:B>C>A
D. 加氧化亚铁可以使溶液C转化为溶液A
查看答案和解析>>
科目: 来源: 题型:
【题目】维生素C是一种水溶性维生素(其水溶液呈酸性),它的分子式是C6H8O6 . 人体缺乏这种维生素易得坏血症,所以维生素C又称抗坏血酸.维生素C易被空气中的氧气氧化.在新鲜水果、蔬菜、乳制品中都含维生素C,如新鲜橙汁中维生素C的含量在500mgL﹣1左右.某校课外活动小组测定了某品牌的软包装橙汁中维生素C的含量.下面是测定实验分析报告,请填写有关空白.
(1)测定目的:测定某品牌软包装橙汁中维生素C的含量. 测定原理:C6H8O6+I2→C6H6O6+2H++2I﹣ .
实验用品:①仪器:(自选,略).
试剂:指示剂(填名称)、浓度为7.5×10﹣3 molL﹣1的标准碘溶液、蒸馏水等.
(2)实验过程: ①洗涤仪器,检查滴定管是否漏液,润洗后装好标准碘溶液待用.
②打开橙汁包装,目测:颜色﹣﹣橙黄色,澄清度﹣﹣好.用(填仪器名称)向锥形瓶中量入20.00mL待测橙汁,滴入2滴指示剂.
③用左手控制滴定管的(填部位),右手摇动锥形瓶,眼睛注视 , 直到滴定终点,滴定至终点的现象是 .
(3)数据记录与处理:如图1为某一次滴定管滴定前液面,其读数值为mL图2为滴定结束液面,则本次滴定过程共使用了mL标准碘溶液 几次滴定消耗NaOH溶液的体积如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
则此橙汁中维生素C的含量是mgL﹣1 .
(4)问题讨论:取标准碘溶液的滴定管洗涤之后直接装液开始滴定,则测定结果 . (填“偏高”、“偏低”、“无影响”) 
查看答案和解析>>
科目: 来源: 题型:
【题目】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。下列说法错误的是( )

A. zh3中各原子最外层都达到8e-稳定结构
B. y与g可形成化合物yg2,结构式为g=y=g
C. d和f形成的简单离子半径大小关系为:d2- < f3+
D. f 和h 形成的化合物属于离子化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】已知Ba(AlO2)2可溶于水。下图表示的是向A12(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系。下列有关叙述正确的是( )

A. a—b时沉淀的物质的量:A1(OH)3比BaSO4多
B. c—d时溶液中离子的物质的量:AlO2-比Ba2+多
C. a—d时沉淀的物质的量:BaSO4可能小于A1(OH)3
D. d—e时溶液中离子的物质的量:Ba2+可能等于OH-
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上制备相关物质,涉及的反应原理及部分流程较为合理的是
A. 制取镁:海水![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO![]() Mg
Mg
B. 冶炼铝:铝土矿![]() NaAlO2
NaAlO2![]() 无水AlCl3
无水AlCl3![]() Al
Al
C. 制溴:浓缩海水![]() Br2
Br2![]() HBr(aq)
HBr(aq) ![]() Br2
Br2
D. 制碘:海带![]() 海带灰
海带灰![]() I2(aq)
I2(aq) ![]() I2
I2
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为一些常见物质间的相互转化关系,其中F为金属,高温下能与某些金属氧化物反应,是工业冶炼金属的方法之一. A为无色气体,B为淡黄色固体,C为无色液体,E和J为无色气体单质.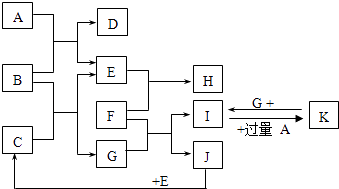
试回答下列问题:
(1)写出B的化学式: , 写出A的电子式;
(2)写出I→K的离子方程式;
(3)写出F与Fe3O4在高温下反应的化学方程式;
(4)已知3g J完全燃烧放出a kJ的热量,请写出表示J的燃烧热的热化学方程式: .
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,反应 N2(g)+O2(g)2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是( )
A.缩小体积使压强增大
B.恒容,充入N2
C.恒容,充入He
D.恒压,充入He
查看答案和解析>>
科目: 来源: 题型:
【题目】茉莉花香气的成分有多种,乙酸苯甲酯( ![]() )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
(1)写出反应①的化学方程式: .
(2)反应③的反应类型为 .
(3)C的结构简式为 .
(4)反应①~③中,原子的理论利用率为100%,符合绿色化学要求的是(填序号).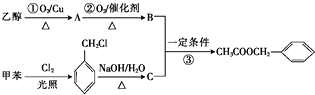
查看答案和解析>>
科目: 来源: 题型:
【题目】W、R、X、Q、Z为前18号元素中的五种,W的低价氧化物与X单质分子的电子总数相等,R与W同族,Q2-和Z-的离子与Ar原子的电子层结构相同且Q的原子序数小于Z。
(1)W位于元素周期表中第_____周期第______族;
(2)R的氢化物分子的结构式是_________;
(3)X的常见氢化物与下一周期同族元素氢化物相比,沸点比较大的是________ (填化学式);它的另一6核氢化物,其电子式是________ ;
(4)W与Z形成的共价化合物的化学式是________;W 与Q形成的分子含有______键(填“极性”或“非极性”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据要求填空:
(1)3﹣甲基﹣2﹣丙基﹣1﹣戊烯结构简式为
(2)![]() 名称为 .
名称为 .
(3) 名称为: .
名称为: .
(4)![]() 名称为:
名称为:
(5)有机物A只由C、H、O三种元素组成,常用作有机合成的中间体,测得8.4g该有机物经燃烧生成22.0g CO2和7.2g水.质谱图表明其相对分子质量为84;红外光谱分析表明A中含有﹣O﹣H和位于分子端的C H,核磁共振氢谱显示有3种峰,且峰面积之比为6:1:1. ①写出A的分子式;
②写出A的结构简式;
③下列物质一定能与A发生反应的是(填序号)
a.H2 b.Na c.KMnO4 d.Br2
④有机物B是A的同分异构体,1mol B可以与1mol Br2加成,该有机物的所有碳原子在同一平面上,核磁共振氢谱显示有3种峰,且峰面积之比为6:1:1,则B的结构简式是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com