
科目: 来源: 题型:
【题目】实验室里用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO47H2O>,其过程如图:
(1)过程①中,FeS和O2、H2SO4反应的化学方程式为 .
(2)过程②中产生的尾气会对大气造成污染,可选用下列试剂中的吸收.
a.浓H2SO4 b.蒸馏水 c.NaOH溶液 d.浓硝酸
(3)过程③中,需要加人的物质名称是 .
(4)过程④的实验操作是
(5)过程⑥中,将溶液Z加热到7080℃,目的是 .
(6)实验室为测定所得到的聚铁样品中铁元素的质量分数,进行下列实验.①用分析天平称取 样品2.700g;②将样品溶于足量盐酸后,加人足量的氯化钡溶液;③过滤、洗涤、干燥,称量,得 固体质量为3.495g.若该聚铁主要成分为[Fe(OH)SO4],则该聚铁中铁元素的质量分数为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组对电化学问题进行了实验探究.
(1)Ⅰ.利用如图1装置探究金属的防护措施,实验现象是锌电极不断溶解,铁电极表面有气泡产生.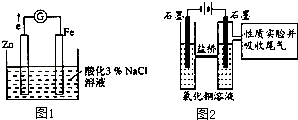
a.写出负极的电极反应式 .
b.某学生认为,铁电极可能参与反应,并对产物作出假设:
假设1:铁参与反应,被氧化生成Fe2+;
假设2:铁参与反应,被氧化生成Fe3+;
假设3: .
c.为了探究假设1、2,他采取如下操作:
①取0.01mol/L FeCl3溶液2mL于试管中,加入过量铁粉;
②取操作①试管的上层清夜加入2滴K3[Fe(CN)6]溶液,生成蓝色沉淀;
③取少量正极附近溶液加入2滴K3[Fe(CN)6]溶液,未见蓝色沉淀生成;
④取少量正极附近溶液加入2滴KSCN溶液,未见溶液变红;
据②、③、④现象得出的结论是 .
d.该实验原理可应用于防护钢铁腐蚀,请再举一例防护钢铁腐蚀的措施 .
(2)Ⅱ.利用图2装置作电解50mL 0.5mol/L的CuCl2溶液实验.实验记录:
A.阳极上有黄绿色气体产生,该气体使湿润的淀粉碘化钾试纸先变蓝后褪色;
B.电解一段时间以后,阴极表面除有铜吸附外,还出现了少量气泡和浅蓝色固体.
a.分析实验记录A中试纸颜色变化,用离子方程式解释:
①;
② .
b.分析实验记录B中浅蓝色固体可能是(写化学式),试分析生成该物质的原因 .
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A,B,C,D,E,F,G是七种原子序数依次增大的短周期元素,它们的原子结构特征或有关物质的性质等如表所示.
元素 | 原子结构特征或有关物质的性质 |
A | 原子的最外层电子数是其内层电子数的2倍 |
B | 其单质是空气中含量最多的物质 |
C | 原子的最外层电子数是其电子层数的4倍 |
D | 位于第ⅡA族,其原子半径比E的大 |
E | 是金属元素,其氧化物和氢氧化物都有两性,且与D在同一周期 |
F | 原子序数16,其单质在通常状况下为固体 |
G | 原子的最外层电子数比其次外层电子数少1个 |
(1)元素F在元素周期表中的位置是 . 这七种元素中,不属于主族元素的元素的名称是 .
(2)在E,F,G三种元素中,原子半径最小的是(填元素符号).
(3)元素A与G可形成化合物AG4 , 在该化合物中含有的化学键类型为 , 分子的空间结构为 . A与氧元素可形成化合物AO2 , 该化合物分子的电子式为 .
(4)元素B能与氢元素形成化合物BH3 , 在通常状况下,BH3的水溶液呈(填“酸”、“碱”或“中”)性,原因为(用方程式表示)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列两种物质的溶液混合后,能发生离子反应,且溶液的总质量不会发生改变的是( )
A.澄清石灰水和稀盐酸混合
B.小苏打溶液和醋酸混合
C.盐(含有硫酸钠、碳酸氢钠、氯化钠、硫酸钾)溶液与BaCl2溶液混合
D.氯化钠溶液和蔗糖水混合
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A,B,C,D,E,F,G是七种原子序数依次增大的短周期元素,它们的原子结构特征或有关物质的性质等如表所示.
元素 | 原子结构特征或有关物质的性质 |
A | 原子的最外层电子数是其内层电子数的2倍 |
B | 其单质是空气中含量最多的物质 |
C | 原子的最外层电子数是其电子层数的4倍 |
D | 位于第ⅡA族,其原子半径比E的大 |
E | 是金属元素,其氧化物和氢氧化物都有两性,且与D在同一周期 |
F | 原子序数16,其单质在通常状况下为固体 |
G | 原子的最外层电子数比其次外层电子数少1个 |
(1)元素F在元素周期表中的位置是 . 这七种元素中,不属于主族元素的元素的名称是 .
(2)在E,F,G三种元素中,原子半径最小的是(填元素符号).
(3)元素A与G可形成化合物AG4 , 在该化合物中含有的化学键类型为 , 分子的空间结构为 . A与氧元素可形成化合物AO2 , 该化合物分子的电子式为 .
(4)元素B能与氢元素形成化合物BH3 , 在通常状况下,BH3的水溶液呈(填“酸”、“碱”或“中”)性,原因为(用方程式表示)
查看答案和解析>>
科目: 来源: 题型:
【题目】根据要求书写化学方程式或离子方程式
(1)氢氟酸刻蚀玻璃的化学方程式为______________。
(2)利用铝热反应焊接钢轨的化学方程式为______________。
(3)铜鼎在潮湿的空气中被锈蚀生成铜绿的化学方程式为______________。
(4)铝粉与氢氧化钠溶液反应的离子方程式______________。
(5)氯化铝和过量氨水反应的离子方程式______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是一些重要工业生产的转化关系(反应条件略去):
![]()
请完成下列问题.
(1)若D为固体单质,与A属于同一主族短周期元素,则
①反应的化学方程式是________________;
②D的原子结构示意图是__________;
③D单质的一种重要用途是____________。
(2)若A为黑色固体,D为可燃性气体单质,则该反应的化学方程式_________。
(3)若B是一种能使湿润的红色石蕊试纸变蓝的气体,则
①B分子的电子式是_____________;
②B在一定条件下可与C反应生成无毒无害的物质,则该反应的化学方程式为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com