
科目: 来源: 题型:
【题目】有机物A的相对分子质量184.5,其结构如图1所示,(﹣R﹣代表某种烷基),A在一定条件下还有如图2所示的反应关系,D不能发生银镜反应.
(1)C中含有的官能团为 , E→F的反应类型为;
(2)写出A的结构简式;
(3)写出C→E的化学方程式;
(4)H的同分异构体很多,其中属于酯类,含苯环,且水解产物中含有乙酸的同分异构体有种
(5)G显酸性,M(B),M(G)分别表示B、G的相对分子质量,试求:M(G)﹣M(B)= .
查看答案和解析>>
科目: 来源: 题型:
【题目】在25℃时,密闭容器中X,Y,Z三种气体的起始浓度和平衡浓度如表,下列说法错误的是( )
物质 | X | Y | Z |
初始浓度/molL﹣1 | 0.1 | 0.2 | 0 |
平衡浓度/molL﹣1 | 0.05 | 0.05 | 0.1 |
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y2Z,平衡常数为1600
C.其他条件不变时,增大压强可使平衡常数增大
D.改变温度可以改变该反应的平衡常数
查看答案和解析>>
科目: 来源: 题型:
【题目】某校学生为探究苯与溴发生反应的原理,用如图装置进行实验.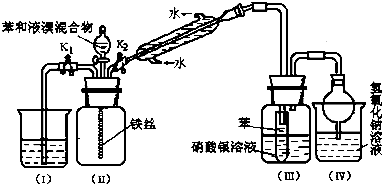
根据相关知识回答下列问题:
(1)实验开始时,关闭K1 , 开启K2和分液漏斗活塞,滴加苯和液溴的混合液,反应开始.过一会儿,在(Ⅲ)中可能观察到的现象是
(2)整套实验装置中能防止倒吸的装置有(填装置序号).
(3)反应结束后要使装置(I)中的水倒吸入装置(Ⅱ)中.这样操作的目的是 . 简述这一操作方法
(4)你认为通过该实验后,有关苯跟溴反应的原理方面能得出的结论是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】A~J是中学化学中常见的几种物质,它们之间的转化关系如图所示.已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,且E可由C、F化合生成,J可作杀菌消毒剂.
(1)写出B的电子式 .
(2)写出反应⑤的化学方程式: .
(3)写出反应⑦的离子方程式: .
(4)向AlCl3溶液中加入少量固体B,写出反应的化学方程式: .
(5)以Pt为电极电解滴加有少量酚酞的H饱和溶液,则极(填“阴”或“阳”)附近溶液先由无色变为红色,请说明理由: .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验事实与图象对应正确的是( ) 
A.I表示向Na2SO3溶液中通入Cl2
B.II表示向纯CH3COOH中逐滴加水并不断振荡
C.III表示向KOH和Ca(OH)2混合液中通入CO2
D.Ⅳ表示向NaOH溶液中逐滴加入AlCl3溶液并不断振荡
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学研究小组设计如下图装置制备纯净的氯化铁。

资料:
①氯化铁遇水能发生剧烈反应生成Fe(OH)3;
②CCl4难溶于水,密度大于水,且Cl2在CCl4中的溶解度远大于水中的溶解度。
回答下列问题:
(1)试剂X的作用是__________________,试剂Y是__________________。
(2)实验过程中,A、E两处有酒精灯,应先点燃___________(填“A”或“E”)处;实验完毕后,关闭旋塞K,熄灭酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是______________,B的作用是______________________。
(3)用量简量取20mLG中溶液。倒入密封性良好的分液漏斗中,然后再注入10mL CCl4,盖好玻璃塞,振荡、静置、分液,分别取上层液、下层液滴在有色布条上,能使有色布条褪色的是__________(填“上层液”或“下层液”)。
(4)写出装置A中反应的离子方程式:_____________________________。实验结束后,测得装置E中的铁丝网质量增加mg,则理论上装置A中反应转移电子的物质的量为_________mol(用含m的式子回答)。
(5)有同学认为上述装置存在不足,用该装置制取的氯化铁中还含有其他杂质(不考虑铁),建议进行改进,请提出你的改进办法_____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学学习和研究离不开元素周期表。下表为元素周期表的一部分,表中①-⑩分别代表一种元素。回答下列问题:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
3 | ⑧ | ⑨ | ⑩ |
(1)上述元素中,有一种元素在自然界中形成的物质种类最多,该元素在周期表中的位置是_______。
(2)⑧、⑨、⑩元素的离子半径由大到小的顺序为________________(用离子符号表示)。
(3)写出由①、⑥、⑧三种元素形成的一种离子化合物的电子式__________________。
(4)上述元素中有一种元素的氧化物和氢氧化物都有两性,面出该元素的原子结构示意图______________;高温条件下,该元素的单质与铁红能发生反应,此反应常用于野外焊接钢轨,则该反应的能量变化可用图__________________表示。(填“甲“或“乙”)
(5)知W+X→Y+Z,且W、X、Y、Z分别是由①、⑤、⑥三种元素中的两种形成的10电子粒子,写出并配平上述反应式___________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在其他条件不变时,改变某一条件对反应A2(g)+3B2(g)2AB3(g)的化学平衡状态的影响如图所示(T表示温度,n表示物质的量).下列判断正确的是( ) 
A.反应速率:a>b>c
B.达到平衡时A的转化率大小:b>a>c
C.若T2>T1 . 则正反应一定是吸热反应
D.达到平衡时,n( AB3)的大小:b>a>c
查看答案和解析>>
科目: 来源: 题型:
【题目】我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如下:

回答下列问题:
(1)二氧化碳分子中的化学键是_________________,物质乙的化学式是______________。
(2)写出反应①的化学方程式__________________________________。
(3)实验室常用纯净碳酸钙与稀盐酸反应制取二氧化碳气体,反应过程中产生二氧化碳的速率V(CO2) 与时间关系如下图:

①由图像分析,化学反应速率最快一段是___________。
②为了增大上述化学反应的反应速率,欲向溶液中加入下列物质,你认为可行的是_________(填写序号)。
A.蒸馏水 B.氯化钠溶液 C.浓盐酸 D.加热
(4)二氧化碳能与氢氧化钠溶液反应,当氢氧化钠过量时反应生成碳酸钠,当氢氧化钠少量时反应生成碳酸氢钠。当二氧化碳与氢氧化钠反成的物质的量比为2:3时,溶液中的溶质是_______________。
(5)从原子结构角度说明氧原子得电子能力强于碳原子:___________________________________。
(6)在一定条件下,工业上也可用CO2合成甲醇(CH3OH),其化学方程式为:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)。 将a molCO2与bmolH2充入容积为2L的密闭容器中发生上述反应,t min时测得甲醇的物质的量为c mol。计算0-t min内CO2的反应速率为_________ mol·L-1·s-1。 [X 的反应速率ν(X)=X的物质的量浓度变化/变化需要的时间]
CH3OH(g)+H2O(g)。 将a molCO2与bmolH2充入容积为2L的密闭容器中发生上述反应,t min时测得甲醇的物质的量为c mol。计算0-t min内CO2的反应速率为_________ mol·L-1·s-1。 [X 的反应速率ν(X)=X的物质的量浓度变化/变化需要的时间]
查看答案和解析>>
科目: 来源: 题型:
【题目】半导体工业用石英砂做原料通过三个重要反应生产单质硅:
①SiO2(s)+2C(s)═Si(s)+2CO(g)△H=+682.44kJmol﹣1 ,
(石英砂) (粗硅)
②Si(s)+2Cl2(g)═SiCl4(g)△H=﹣657.01kJmol﹣1
③SiCl4(g)+2Mg(s)═2MgCl2(s)+Si(s)△H=﹣625.63kJmol﹣1
(纯硅)
用石英砂生产1.00kg纯硅的总放热为( )
A.2.43×104 kJ
B.2.35×104 kJ
C.2.23×104 kJ
D.2.14×104 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com