
科目: 来源: 题型:
【题目】某同学为了探究锌与盐酸反应过程的速率变化以及影响反应快慢的因素,在100 mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如表所示(累计值):
时间/min | 1 | 2 | 3 | 4 | 5 |
氢气体积/mL | 50 | 120 | 232 | 290 | 310 |
(1)反应速率最大的时间段(指0~1、1~2、2~3、3~4、4~5 min)是_______________min,该时间段以盐酸的浓度变化表示的该反应的速率是______________________。从影响反应速率的外界条件分析原因是_______________________________________。
(2) 反应速率最小的时间段(指0~1、1~2、2~3、3~4、4~5 min)是_____________min,原因是_______________________________________________。
(3)如果反应过于剧烈,为了减缓反应速率而又不减少产生氢气的量,可以在盐酸中分别加入等体积的下列溶液,你认为可行的是________(填序母)。
A.蒸馏水 B.NaCl溶液 C.NaNO3溶液 D.CuSO4溶液 E.Na2CO3溶液,
查看答案和解析>>
科目: 来源: 题型:
【题目】2SO2(g)+O2(g)2SO3(g)是制备硫酸的重要反应.下列叙述正确的是( )
A.催化剂V2O3不改变该反应的逆反应速率
B.增大反应体系的压强,反应速率一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,SO3(g)的浓度分别是c1、c2 , 则时间间隔t1~t2内,SO3(g)生成的平均速率为v= ![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物的结构简式为 ,关于该有机物的说法不正确的是( )
,关于该有机物的说法不正确的是( )
A. 1 mol该有机物能与2 mol NaOH发生反应
B. 1 mol该有机物能与2 mol Na反应生成1 mol H2
C. 1 mol该有机物能与1 mol NaHCO3反应生成1 mol CO2
D. 1 mol该有机物最多能与4 mol H2发生加成反应
查看答案和解析>>
科目: 来源: 题型:
【题目】偏二甲肼(C2H8N2)是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭的推动力。下列叙述正确的是( )
A. 偏二甲肼的摩尔质量为60 g B. 1 mol 偏二甲肼的质量为60 g/mol
C. 1mol偏二甲肼的质量为60 g D. 6 g偏二甲肼(C2H8N2)含有NA个分子
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组设计用50mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液在如图装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: 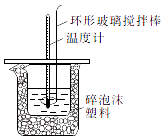
(1)环形玻璃搅拌棒的作用是 .
(2)中和反应放出的热量会造成少量盐酸在反应中挥发,则测得的中和热的数值(填“偏大”、“偏小”或“不变”).
(3)该实验小组做了三次实验,每次取溶液各50mL,并将实验数据记录如表:
实验序号 | 起始温度t1/℃ | 终止温度(t2)℃ | 温差(t2﹣t1)℃ | ||
盐酸 | NaOH溶液 | 平均值 | |||
1 | 25.1 | 24.9 | 25.0 | 31.8 | 6.8 |
2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
3 | 25.1 | 25.1 | 25.1 | 32.0 | 6.9 |
已知盐酸、NaOH溶液的密度与水相同,中和后生成的溶液的比热容c=4.18×10﹣3kJ/(g℃),则该反应的中和热△H= .
(4)在中和热测定实验中,测量起始温度时需要两个温度计,如果只用一个温度计测量,则测得的中和热的数值(填“偏大”、“偏小”或“不变”).
查看答案和解析>>
科目: 来源: 题型:
【题目】锂是最轻的活泼金属,其单质及其化合物有广泛的用途。回答下列问题:
(1)用碳酸锂和反应可制备氯化锂,工业上可由电解LiCl-KCl的熔融混合物生产金属锂,阴极上的电极反应式为。
(2)不可使用二氧化碳灭火器扑灭因金属锂引起的火灾,其原因是。
(3)硬脂酸锂是锂肥皂的主要成分,可作为学科&网高温润滑油和油脂的稠化剂。鉴别硬脂酸锂与硬脂酸钠、硬脂酸钾可采用的实验方法和现象分别是。
(4)LiPF6易溶于有机溶剂,常用作锂离子电池的电解质。LiPF6受热易分解,其热分解产物为PF3和。
查看答案和解析>>
科目: 来源: 题型:
【题目】碳酸钠是一种重要的化工原料,主要采用氨碱法生产。回答下列问题:
(1)碳酸钠俗称 , 可作为碱使用的原因是(用离子方程式表示)。
(2)已知:①2NaOH(s)+CO2(g) ![]() Na2CO3(s)+H2O(g) ΔH1=127.4 kJ·mol1 ②NaOH(s)+CO2(g)
Na2CO3(s)+H2O(g) ΔH1=127.4 kJ·mol1 ②NaOH(s)+CO2(g) ![]() NaHCO3(s) ΔH1=131.5 kJ·mol1
NaHCO3(s) ΔH1=131.5 kJ·mol1
反应2Na2CO3(s) ![]() Na2CO3(s)+ H2O(g) +CO2(g)的ΔH= kJ·mol1 , 该反应的平衡常数表达式K=。
Na2CO3(s)+ H2O(g) +CO2(g)的ΔH= kJ·mol1 , 该反应的平衡常数表达式K=。
(3)向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时溶液中 ![]() =。已知Ksp(BaCO3)=2.6×109 , Ksp(BaSO4)=1.1×1010。
=。已知Ksp(BaCO3)=2.6×109 , Ksp(BaSO4)=1.1×1010。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关物质分类正确的是( )
①混合物:盐酸、王水、水玻璃、水银
②化合物:CaCl2、烧碱、聚苯乙烯、O3
③电解质:H2SO4、胆矾、冰醋酸、硫酸钡
④同素异形体:C60、C70、金刚石、石墨
A. ①③ B. ②④ C. ②③ D. ③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com