
科目: 来源: 题型:
【题目】氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:
(1)氨的水溶液显弱碱性,其原因为 (用离子方程式表示),0.1mol/L的氨水中加入少量的NH4Cl固体, 溶液的pH(填“升高”或“降低”);若加入少量的明矾,溶液中的NH4+的浓度(填“增 大”或“减小”)。
(2)硝酸铵加热分解可得到N2O和2H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为 , 平衡常数表达式为;若有1mol硝酸铵完全分解,转移的电子数为mol。
(3)由N2O、H2O反应生成N2和NO2的能量变化如图所示,若生成1molN2 , 其△H= kJ/mol。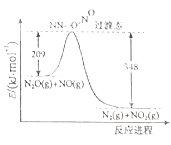
查看答案和解析>>
科目: 来源: 题型:
【题目】1.52g 铜镁合金完全溶解于50mL 密度为1.40 g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(标准状况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是( )。
A. 该合金中铜与镁的物质的量之比是2:1
B. 该浓硝酸中HNO3的物质的量浓度是14.0 mol/L
C. NO2和N2O4的混合气体中,NO2的体积分数是80%
D. 得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL
查看答案和解析>>
科目: 来源: 题型:
【题目】将不同体积同物质的量浓度的NaCl、MgCl2、AlCl3三种溶液中的Cl-完全沉淀,消耗同体积同物质的量浓度的AgNO3溶液,NaCl、MgCl2、AlCl3三种溶液的体积比为
A. 1:2:3 B. 3:2:1 C. 1:1:1 D. 6:3:2
查看答案和解析>>
科目: 来源: 题型:
【题目】一种充电电池放电时的电极反应为:H2+2OH﹣﹣2e﹣=2H2O;NiO(OH)+H2O+e﹣=Ni(OH)2+OH﹣当为电池充电时,与外电源正极连接的电极上发生的反应是( )
A.H2O的还原
B.NiO(OH)的还原
C.H2的氧化
D.Ni(OH)2的氧化
查看答案和解析>>
科目: 来源: 题型:
【题目】银是一种贵金属,古代常用于制造钱币及装饰器皿,现代在电池和照明器材等领域亦有广泛应用。回答下列问题。
(1)久存的银制器皿表面会变黑,失去银白色的光泽,原因是。
(2)已知,Ksp=(AgCl)=1.8×10-10 , 若向50mL0.018mol/L的AgNO3溶液中加入50mL0.020mol/L的盐酸,混合后溶液中的Ag+的浓度为 mol/L,pH为 。
(3)AgNO3溶液光照易分解,生成Ag和红棕色气体等物质,其光照分解的化学方程式为 。
(4)右图所示原电池正极的反应式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】X原子的核电荷数为a,它的阴离子Xm-与Y原子的阳离子Yn+的电子层 结构相同,则Y原子的核电荷数为( )
A.a+m+nB.a-m-nC.m+n-aD.m-n-a
查看答案和解析>>
科目: 来源: 题型:
【题目】在硫酸铜饱和溶液中,投入不规则的硫酸铜晶体, 下列说法正确的是
A.晶体形状不变B.晶体溶解,溶液的浓度变大
C.晶体不溶解,溶液浓度不变D.晶体形状改变,溶液浓度不变
查看答案和解析>>
科目: 来源: 题型:
【题目】在相同温度下,下列两个反应放出的热量分别以Q1和Q2表示
2H2(g) + O2(g) → 2H2O(g) +Q1
2H2(g) + O2(g) → 2H2O(l) +Q2
则Q1和Q2的关系为
A.Q1<Q2B.Q1>Q2C.Q1=Q2D.2Q1=Q2
查看答案和解析>>
科目: 来源: 题型:
【题目】将等物质的量的乙烷和溴蒸气混合后,在光照条件下充分反应,所得产物中物质的量最大的是( )
A.CH3CH2Br
B.CHBr2CHBr2
C.CBr3CBr3
D.HBr
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com