
科目: 来源: 题型:
【题目】将聚丙烯废塑料在隔绝空气条件下加强热的实验装置如图所示,处理后可“变废为宝”,生成物主要含CH4、C2H4、C6H6、H2、C3H6(丙烯)和C(炭黑)等。回答下列问题:

(1)上述生成物中互为同系物的是______(填物质名称,下同),试管A中的残余物主要为____,试管B中收集的产物为________。
(2)锥形瓶C中观察到的现象是___________,经溴水吸收后逸出气体的主要成分为_______(填化学式)。
(3)相同条件下,使生成物CH4、C2H4、C6H6分别在足量氧气中燃烧,若三者物质的量相同,则消耗氧气的体积由大到小的顺序为_________(用化学式表示,下同);若三者的质量相同,则消耗氧气的体积由大到小的顺序为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组设计如下微型实验装置.实验时,先断开K2 , 闭合K1 , 两极均有气泡产生;一段时间后,断开K1 , 闭合K2 , 发现电流表指针偏转,下列有关描述正确的是( ) 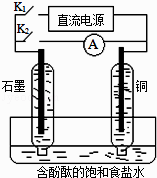
A.断开K2 , 闭合K1时,总反应的离子方程式为:2H++2Cl﹣ ![]() Cl2↑+H2↑
Cl2↑+H2↑
B.断开K2 , 闭合K1时,石墨电极附近溶液变红
C.断开K1 , 闭合K2时,铜电极上的电极反应为:Cl2+2e﹣=2Cl﹣
D.断开K1 , 闭合K2时,石墨电极作正极
查看答案和解析>>
科目: 来源: 题型:
【题目】元素M、T、U、V、N在元素周期表中的相对位置如图所示,其中M单质在冷暗处与H2剧烈化合并爆炸。回答下列问题:

(1)元素T的原子序数为______,元素U的简单离子结构示意图为_________。
(2)V元素形成的单质中______ (填“存在”或“不存在”)化学键。
(3)M、N两元素分别与氢形成的气态氢化物是甲和乙,其中甲的电子式为______,甲和乙的稳定性强弱顺序为______ (用化学式表示,下同),其水溶液的酸性强弱顺序为______。
(4)写出元素U的单质置换出元素T的单质的离子方程式: ____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据问题填空:
(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、 ![]() (PAN)等二次污染物.
(PAN)等二次污染物.
①1mol PAN中含有的σ键数目为 . PAN中四种元素的第一电离能由大到小的顺序为 .
②NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4 , 该配合物中中心离子的配位数为 , 中心离子的核外电子排布式为 .
③相同压强下,HCOOH的沸点比CH3OCH3(填“高”或“低”),其原因是 .
(2)PM2.5微细粒子包含(NH4)2SO4、NH4NO3等.
①(NH4)2SO4晶体中各种微粒间的作用力不涉及(填序号).
a.离子键 b.共价键 c.配位键 d.范德华力 e.氢键
②NH4NO3中阳离子的空间构型为 , 阴离子的中心原子轨道采用杂化.
(3)测定大气中PM2.5的浓度方法之一是β﹣射线吸收法,β﹣射线放射源可用85Kr.已知Kr晶体的晶胞结构如图所示,设晶体中与每个Kr原子紧相邻的Kr原子有m个,晶胞中Kr原子为n个,则 ![]() =(填数字).
=(填数字).
查看答案和解析>>
科目: 来源: 题型:
【题目】硼酸(H3BO3)是一种一元弱酸,微溶于水,回答下列问题.
(1)H3BO3本身不能电离,只能通过结合来自水中的OH﹣而释放出H+ , 试写出H3BO3溶液的电离方程式 , 该物质的电离方式和中学另一种常见物质的电离相似,该物质是(写化学式);
(2)硼砂(Na2B4O710H2O)是硼酸的一种重要钠盐,工业上可利用碳碱法制取,以下是某化工集团利用合成氨脱碳尾气生产硼砂及其它化工产品的流程图.
回答下列问题:
①合成氨常用CH4与水蒸气反应,制取H2的同时获得脱碳尾气(上述流程图中的某物质),所发生的化学方程式为 .
②轻质碳酸镁的组成可表示为xMgCO3 . yMg(OH)2 . zH2O,某小组为测定其成份,准确称取2.33g样品,充分加热后称得剩余物质质量为1.00g,所得气体经浓硫酸吸收,浓硫酸增重0.45g,则该轻质碳酸镁的化学式为: .
③结合②中的结论,推测该工厂生产硼砂溶液的化学方程式为: .
④a处的操作为: .
⑤该工艺可实现多种产品的联产,其中属于联产产品的是 .
a.轻质碳酸镁 b.轻质氧化镁 c.液态二氧化碳 d.纯碱.
查看答案和解析>>
科目: 来源: 题型:
【题目】合理应用和处理氮的化合物,在生产生活中有重要意义.
(1)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料.
①以尿素为原料在一定条件下发生反应:CO(NH2)2 (s)+H2O(l)2NH3(g)+CO2(g)△H=+133.6kJ/mol.该反应的化学平衡常数的表达式K= . 关于该反应的下列说法正确的是(填序号).
a.从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
b.在平衡体系中增加水的用量可使该反应的平衡常数增大
c.降低温度使尿素的转化率增大
②尿素在一定条件下可将氮的氧化物还原为氮气.
已知: 
结合①中信息,尿素还原NO(g)的热化学方程式是 .
③密闭容器中以等物质的量的NH3和CO2为原料,在120℃、催化剂作用下反应生成尿素:CO2(g)+2NH3(g)═CO (NH2)2 (s)+H2O(g),混合气体中NH3的物质的量百分含量[φ(NH3)]随时间变化关系如图2所示
则a点的正反应速率v正(CO2)b点的逆反应速率v(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 .
(2)NO2会污染环境,可用Na2CO3溶液吸收NO2并生成CO2 . 已知9.2g NO2和Na2CO3溶液完全反应时转移电子0.1mol,此反应的离子方程式是;恰好反应后,使溶液中的CO2完全逸出,所得溶液呈弱碱性,则溶液中存在的所有离子浓度大小关系是c(Na+)> .
查看答案和解析>>
科目: 来源: 题型:
【题目】铁、铜等金属及其化合物在日常生产生活中用途非常广泛.
(1).实验室欲制备0.3mol Cu(NO3)2晶体,甲、乙两同学分别设计实验方案如下: 甲:Cu ![]() Cu(NO3)2 乙:Cu
Cu(NO3)2 乙:Cu ![]() CuO
CuO ![]() Cu(NO3)2
Cu(NO3)2
①从绿色化学的角度分析,同学的方案更合理
②乙同学实验时通入O2的速率不宜过大,为便于观察和控制产生O2的速率,宜选择装置(填字母序号).
(2).某化学实验小组通过实验来探究一包黑色粉是否由Fe3O4、CuO组成探究过程如下: ①提出假设:
假设1.黑色粉末是CuO;
假设2.黑色粉末是Fe3O4;
假设3.黑色粉末是CuO和Fe3O4的混合物.
②设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂.
a若假设1成立,则实验现象是溶液显蓝色.
b若假设2或3成立,则实验现象是 .
为进一步探究,继续向所得溶液加入足量铁粉,若产生的现象,则假设3成立.
有另一小组同学提出,若混合物中CuO含量较少,可能加入铁粉后实验现象不明显.
查阅资料:Cu2+与足量氨水反应生成深蓝色溶液,Cu2++4NH3H2O=Cu(NH3)42++4H2O.
为探究是假设2还是假设3成立,另取少量粉末加稀硫酸充分溶解后,再加入足量氨水,若假设2成立,则产生现象;若假设3成立,则产生现象.
(3).由Fe3O4、FeO、CuO、Fe组成的固体混合物,在加热条件下用足量的CO还原,得到金属混合物2.86g,将生成的CO2气体用足量的澄清石灰水吸收后,产生5.00g白色沉淀.固体混合物的质量是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,H2SO3及其钠盐的溶液中,H2SO3、HSO3﹣、SO32﹣的物质的量分数(α)随溶液pH变化关系如图所示,下列叙述错误的是( ) 
A.溶液的pH=5时,硫元素的主要存在形式为HSO3﹣
B.当溶液恰好呈中性时:c(Na+)>c(SO32﹣)+c(HSO3﹣)
C.向pH=8的上述溶液中滴加少量澄清石灰水, ![]() 的值增大
的值增大
D.向pH=3的上述溶液中滴加少量稀硫酸,α(HSO3﹣)减小
查看答案和解析>>
科目: 来源: 题型:
【题目】在“石蜡→液体石蜡→石蜡蒸气→裂化气”的变化过程中,被破坏的作用力依次是( )
A.范德华力、范德华力、范德华力
B.范德华力、范德华力、共价键
C.范德华力、共价键、共价键
D.共价键、共价键、共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com