
科目: 来源: 题型:
【题目】工业回收铅蓄电池中的铅,常用Na2CO3或NaHCO3溶液处理铅膏(主要成分PbSO4)获得PbCO3:PbSO4(s) + CO32-(aq) ![]() PbCO3(s) + SO42-(aq) K = 2.2×105。 经处理得到的PbCO3灼烧后获得PbO,PbO再经一步转变为Pb。下列说法正确的是( )
PbCO3(s) + SO42-(aq) K = 2.2×105。 经处理得到的PbCO3灼烧后获得PbO,PbO再经一步转变为Pb。下列说法正确的是( )
A.PbSO4的溶解度小于PbCO3
B.处理PbSO4后,Na2CO3或NaHCO3溶液的pH升高
C.若用等体积、等浓度的Na2CO3和NaHCO3溶液分别处理PbSO4 , Na2CO3溶液中的PbSO4转化率较大
D.整个过程涉及一个复分解反应和两个氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】新制氢氧化铜存在平衡:Cu(OH)2 + 2OH—![]() Cu(OH)42—(深蓝色)。某同学进行下列实验:( )
Cu(OH)42—(深蓝色)。某同学进行下列实验:( )
下列说法不正确的是
A.①中出现蓝色沉淀
B.③中现象是Cu(OH)2 + 2OH—![]() Cu(OH)42—正向移动的结果
Cu(OH)42—正向移动的结果
C.④中现象证明葡萄糖具有还原性
D.对比②和④可知Cu(OH)2氧化性强于Cu(OH)42—
查看答案和解析>>
科目: 来源: 题型:
【题目】在某容积一定的密闭容器中,有下列的可逆反应:A(g)+B(g)xC(g) , 有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( ) 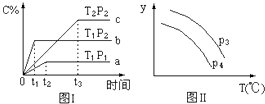
A.P3>P4 , y轴表示B的转化率
B.P3<P4 , y轴表示B的体积分数
C.P3<P4 , y轴表示混合气体的密度
D.P3<P4 , y轴表示混合气体的平均摩尔质量
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外小组研究铝土矿中Al2O3的含量。查阅资料得知,铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:
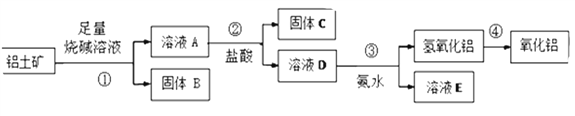
(1)固体B的主要用途有(写出1条即可)__________________________ 。
(2)第①步,向铝土矿中加入足量烧碱溶液后,发生反应的离子方程式是:_____________________________________________________________;___________________________________________________________。
(3)第③步中,生成氢氧化铝的离子方程式是____________________________________________________________。
(4)工业上制取AlCl3用Al2O3与C、Cl2在高温条件下反应,每消耗0.5 mol碳单质,转移1 mol电子,反应的化学方程式是___________________________________________________。
(5)将实验过程中所得固体精确称量。课外小组发现所得氢氧化铝固体的质量与原铝土矿质量相等,则该铝土矿中Al2O3的质量分数是________。(保留一位小数)
查看答案和解析>>
科目: 来源: 题型:
【题目】密闭容器中,由H2和CO直接制备二甲醚(CH3OCH3),其过程包含以下反应:
i.CO(g)+2H2(g) ![]() CH3OH(g) H1=90.1kJ·mol1
CH3OH(g) H1=90.1kJ·mol1
ii.2CH3OH(g) ![]() CH3OCH3(g)+H2O(g) H2=24.5kJ·mol1
CH3OCH3(g)+H2O(g) H2=24.5kJ·mol1
当其他条件相同时,由H2和CO直接制备二甲醚的反应中,CO平衡转化率随条件X 的变化曲线如右图所示。下列说法正确的是( )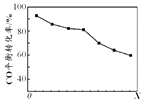
A.由H2和CO直接制备二甲醚的反应为放热反应
B.条件X为压强
C.X增大,二甲醚的产率一定增大
D.X增大,该反应的平衡常数一定减小
查看答案和解析>>
科目: 来源: 题型:
【题目】向容积为2L的密闭器中充入2molA气体和1molB气体,在一定条件下发生如下反应:2A(g)+B(g)3C(g);经2s后达到平衡,测得C气体的浓度为0.6molL﹣1 . 下列说法中正确的是( )
①用物质A表示该反应的平均反应速率为0.2molL﹣1s﹣1
②用物质B表示该反应的平均反应速率为0.2molL﹣1s﹣1
③平衡时物质A与B的转化率相等
④平衡时物质B的浓度为0.2molL﹣1
⑤其它条件不变,向容器中再加入1molC气体,达到新平衡时,C的体积分数不变.
A.①②③
B.①③⑤
C.②④⑤
D.①③④
查看答案和解析>>
科目: 来源: 题型:
【题目】反应A+B→C分两步进行:①A+B→X,②X→C,反应过程中能量变化如图所示,E4表示反应A+B→X的活化能,下列有关叙述正确的是( ) 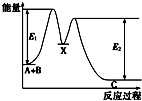
A.Ee表示反应X→C的活化能
B.X是反应A+B→C的催化剂
C.反应A+B→C的△H<0
D.加入催化剂可改变反应A+B→C的焓变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com