
科目: 来源: 题型:
【题目】下列实验能说明SO2具有漂白作用的是
A.SO2气体能使溴水褪色
B.SO2能使酸性高锰酸钾溶液褪色
C.SO2气体能使含NaOH的酚酞溶液褪色
D.SO2气体能使黄色的草帽辫变白色
查看答案和解析>>
科目: 来源: 题型:
【题目】掌握仪器的名称、组装及使用方法是中学化学实验的基础,根据如图实验装置回答问题. 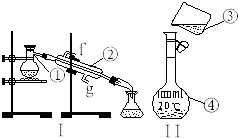
(1)写出下列仪器的名称:①;④;
(2)仪器①~④中,使用时必须检查是否漏水的是 . (填序号)
(3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器有 , 将仪器补充完整后进行的实验操作的名称为;
(4)现需配制250mL、0.2mol/LNaCl溶液,装置II是某同学转移溶液的示意图,图中的错误之处: ① ;②
查看答案和解析>>
科目: 来源: 题型:
【题目】不可以用于实验室制取氨气的方法是
A.在浓氨水中加入固体氢氧化钠并加热
B.加热分解氯化铵晶体
C.在浓氨水中加入固体氧化钙并加热
D.加热氯化铵和消石灰的固体混合物
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下列实验操作中,错误的是 (填序号,下同)
①用10mL量筒量取6.4mL盐酸;
②切割金属钠时,将残留物放入废物缸中;
③配制FeSO4溶液时一般要加入适量铁屑;
④配制一定物质的量浓度的溶液定容时仰视读数会使所配溶液浓度偏高;
⑤不慎接触过多的氨,应及时吸入新鲜的空气和水蒸气,并用大量水冲洗眼睛;
⑥用带橡皮塞的棕色试剂瓶存放浓HNO3;
⑦稀释浓硫酸时应把水倒入浓硫酸中.
(2)如图为实验室制H2的装置.若液面刚好不与锌粒接触而又无酸液可加入,则可以从长颈漏斗中加入适量试剂是
①食盐水 ②苯 ③四氯化碳④Na2CO3溶液 ⑤硫酸铜溶液 ⑥KNO3溶液.
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA代表阿伏加德罗常数,下列说法正确的是
A. 常温下,5.6g铁与足量的盐酸反应,失去的电子数为0.2NA
B. 标准状况下11.2L二氧化硫中含有的原于数为2NA
C. 标准状况下,22.4L氯气发生反应转移电子数一定为2NA
D. 0.1mol/LCuCl2溶液中Cl-数目是0.2NA
【答案】A
【解析】 A、因为Fe和盐酸反应氧化产物是Fe 2+ ,5.6 g铁失去电子数为0.2 N A,选项A错误;B、B. 标准状况下11.2L二氧化硫中含有的原子数为![]() 3NA=3NA,选项B错误;C、1 mol 氯气参加反应时,氯气可以只做氧化剂,也可以自身氧化还原反应,电子转移数目可以为2NA或NA,选项C错误;D、溶液体积不明确,故溶液中的氯离子的个数无法计算,选项D错误。答案选A。
3NA=3NA,选项B错误;C、1 mol 氯气参加反应时,氯气可以只做氧化剂,也可以自身氧化还原反应,电子转移数目可以为2NA或NA,选项C错误;D、溶液体积不明确,故溶液中的氯离子的个数无法计算,选项D错误。答案选A。
【题型】单选题
【结束】
23
【题目】实验室利用以下反应制取少量氨气:NaNO2+NH4Cl=NaC1+N2↑+2H2O,关于该反应的下列说法正确的是
A. NaNO2发生氧化反应
B. 每生成1molN2转移的电子的物质的量为3mol
C. NH4Cl中的氯元素被还原
D. N2既是氧化剂,又是还原剂
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组气体中,通常情况下能共存,并都能用浓硫酸和碱石灰干燥的是
A.SO2,H2S,O2B.NH3,H2,N2
C.N2,H2,COD.HCl,Cl2,CO2
查看答案和解析>>
科目: 来源: 题型:
【题目】(15分)凯氏定氨法是测定蛋白质中氮含量的经典方法,其原理是用浓硫酸在催化剂存在下将样品中有机氮转化成铵盐,利用如图所示装置处理铵盐,然后通过滴定测量.已知:NH3+H3BO3=NH3H3BO3;NH3H3BO3+HCl=NH4Cl+H3BO3 . 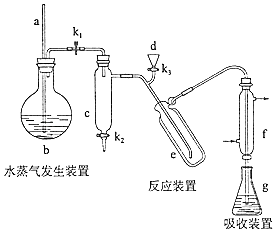
回答下列问题:
(1)a的作用是 .
(2)b中放入少量碎瓷片的目的是 . f的名称是 .
(3)清洗仪器:g中加蒸馏水:打开K1 , 关闭K2、K3 , 加热b,蒸气充满管路:停止加热,关闭K1 , g中蒸馏水倒吸进入c,原因是;打开K2放掉水,重复操作2~3次.
(4)仪器清洗后,g中加入硼酸(H3BO3)和指示剂,铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭K1 , d中保留少量水,打开K1 , 加热b,使水蒸气进入e.
①d中保留少量水的目的是 .
②e中主要反应的离子方程式为 , e采用中空双层玻璃瓶的作用是 .
(5)取某甘氨酸(C2H3NO2)样品m 克进行测定,滴定g中吸收液时消耗浓度为cmolL﹣1的盐酸V mL,则样品中氮的质量分数为%,样品的纯度≤%.
查看答案和解析>>
科目: 来源: 题型:
【题目】将NaC1O3和NaI按物质的量之比1:1混合于烧瓶中,滴入适量硫酸,并水浴加热,反应后测得NaC1O3和NaI恰好完全反应,生成I2、Na2SO4和H2O,并产生棕黄色的气体X,则X为
A. Cl2 B. Cl2O C. Cl2O3 D. ClO2
【答案】D
【解析】试题分析:根据转移电子数守恒得,1molNaI中的碘元素由-1价生成单质碘,化合价升高转移1mol电子,故NaClO3中的氯元素化合价降低转移1mol电子,故X气体中氯元素的价态为+4价,答案选D.
考点:氧化还原反应
【题型】单选题
【结束】
25
【题目】把4.48LCO2通过一定量的固体过氧化钠后收集到3.36L气体(气体的测量均在标准状况下),所得气体的总质量是
A. 3.2g B. 4.8g C. 5.4g D. 6g
查看答案和解析>>
科目: 来源: 题型:
【题目】已知质量分数为25%的氨水密度是0.91g·cm-3,质量分数为5%的氨水密度是0.98 g·cm-3,若将上述两溶液等体积混合,所得氨水的质量分数是
A. 等于15% B. 小于15% C. 大于15% D. 无法确定
查看答案和解析>>
科目: 来源: 题型:
【题目】教材中有两个关于混合物分离的实验,请回答下列有关问题
实验一:通过蒸馏的方法除去自来水中含有的氯离子等杂质制取纯净水,如图所示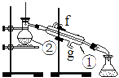
(1)写出下列仪器的名称:①②
(2)若利用以上装置分离酒精和四氯化碳两种溶液的混合物,还缺少的仪器是 , 将仪器补充完整后进行的实验操作的名称是;②的进水口是 (填“f”或“g”)
(3)仪器①中常加入碎瓷片,这样做的目的是
实验二:用CCl4从碘水中萃取I2并分液漏斗分离两种溶液.
其实验操作中有如下两步:①将漏斗上口玻璃塞打开或使塞上的凹槽或小孔准漏斗的小孔.②静置分层后,旋开活塞,用烧杯接收下层液体
(4)这样做的目的是
(5)下层流出的是溶液,上层液体从得到(填“上口”或“下口”)
(6)萃取碘水中的I2单质时要用到萃取剂,下列关于所加萃取剂的说法正确的是
A.不与碘反应
B.碘在其中的溶解度大于在水中的溶解度
C.该萃取剂与水不互溶且密度不同
D.可以选用CCl4 , 酒精灯做萃取剂.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com