
科目: 来源: 题型:
【题目】(酸碱中和滴定是利用中和反应,用已知浓度的酸(或碱)来测定未知浓度的碱(或酸)的实验方法,其中溶液的pH变化是判断滴定终点的依据.
实验 | 消耗0.1000molL﹣1的 | 待测氢氧化钠 |
1 | 29.02 | 25.00 |
2 | 28.01 | 25.00 |
3 | 27.99 | 25.00 |
(1)如图所示A的pH范围使用的指示剂是;
(2)用0.1000molL﹣1的盐酸溶液滴定未知浓度的氢氧化钠溶液,重复三次的实验数据如表所示.则待测氢氧化钠的物质的量浓度是molL﹣1 . 在上述滴定过程中,若滴定前滴定管下端尖嘴中有气泡,滴定后气泡消失,则测定结果将(填“偏高”、“偏低”或“不影响”).
(3)下列关于上述中和滴定过程中的操作正确的是(填序号)
A.用碱式滴定管量取未知浓度的烧碱溶液
B.滴定管和锥形瓶都必须用待盛放液润洗
C.滴定中始终注视锥形瓶中溶液颜色变化
D.锥形瓶中的待测液可用量筒量取.
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,向10mL0.1mol/LCaCl2溶液中滴加0.1mol/L的Na2CO3溶液,滴加过程中溶液中-lgc(Ca2+)与Na2CO3溶液体积(V)的关系如图所示,下列有关说法正确的是( )
A.z点对应的分散系很稳定
B.w、x、y三点中,水的电离程度最大的为y点
C.若用等浓度的Na2SO4溶液代替Na2CO3溶液,则图像在x点后的变化如虚线部分所示
D.Ksp(CaCO3)=5×10-10mol2/L2
查看答案和解析>>
科目: 来源: 题型:
【题目】已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | Ka=1.8×10﹣5 | Ka1=4.3×10﹣7 | Ka=3.0×10﹣8 |
(1)物质的量浓度均为0.1molL﹣1的四种溶液: a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
pH由小到大排列的顺序是(用编号填写).
(2)常温下,0.1molL﹣1 CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是(填字母).
A.c(H+)
B.![]()
C.c(H+)c(OH﹣)
D.![]()
E.![]()
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式: .
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO﹣)﹣c(Na+)=(填准确数值).
(5)25℃时,将a molL﹣1的醋酸与b molL﹣1氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为 .
(6)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数. 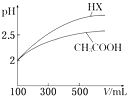
(7)标准状况下,将1.12L CO2通入100mL 1molL﹣1的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式: ①c(OH﹣)=2c(H2CO3)+ .
②c(H+)+c(Na+)= .
查看答案和解析>>
科目: 来源: 题型:
【题目】已知在室温的条件下,pH均为5的H2SO4溶液和NH4Cl溶液,回答下列问题:
(1)两溶液中c(H+)c(OH﹣)= .
(2)各取5mL上述溶液,分别加水稀释至50mL,pH较大的是溶液.
(3)各取5mL上述溶液,分别加热到90℃,pH较小的是溶液.
(4)两溶液中由水电离出的c(H+)分别为:H2SO4溶液;NH4Cl溶液 .
(5)取5mL NH4Cl溶液,加水稀释至50mL, ![]() (填“增大”、“减小”或“不变”).
(填“增大”、“减小”或“不变”).
(6)在0.10molL﹣1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=molL﹣1(Ksp[Cu(OH)2]=2.2×10﹣20).若在0.1molL﹣1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是molL﹣1 .
查看答案和解析>>
科目: 来源: 题型:
【题目】宋代著名的医学家宋慈《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理是:4Ag + 2H2S + O2![]() 2X(黑色)+ 2H2O,下列说法中,不正确的是
2X(黑色)+ 2H2O,下列说法中,不正确的是
A. 银针验毒时,空气中的氧气得到电子
B. 每生成1molX,反应转移2mole-
C. 氧化剂和还原剂的物质的量之比为1: 4
D. 反应中Ag和H2S均为还原剂
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学设计如下实验方案,用以分离 KCl和BaCl2两种混合物,供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸。
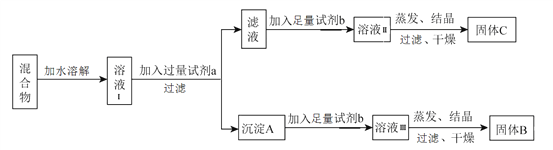
下列说法中,正确的是
A. 试剂 a是K2SO4 溶液
B. 试剂 b是盐酸
C. 固体 C是BaCl2
D. 不加试剂 b,将滤液直接蒸发、结晶,过滤后干燥也能得到纯净的固体C
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,如果取0.1molL﹣1 HA溶液与0.1molL﹣1 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因:(用离子方程式表示).
(2)混合溶液中由水电离出的c(OH﹣)(填“>”、“<”或“=”)0.1molL﹣1 NaOH溶液中由水电离出的 c(OH﹣).
(3)求出混合溶液中下列算式的精确计算结果(填具体数字):c(OH﹣)﹣c(HA)=molL﹣1 .
(4)已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH7(填“>”、“<”或“=”);将同温度下等浓度的四种盐溶液NH4+按由大到小的顺序排列是(填序号). A.NH4HSO4 B.NH4A C.(NH4)2SO4 D.NH4Cl.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com