
科目: 来源: 题型:
【题目】羰基硫(COS)可用于合成除草剂、杀草丹等农药。H2S与CO2在高温下反应可制得COS: H2S(g)+CO2(g) ![]() COS(g) +H2O(g) △H > 0。在 2 L 容器中充入一定量的H2S和CO2发生上述反应,数据如下:
COS(g) +H2O(g) △H > 0。在 2 L 容器中充入一定量的H2S和CO2发生上述反应,数据如下: 下列判断不正确的是( )
下列判断不正确的是( )
A.K1= ![]()
B.K2=K3 且n3=2n2
C.初始反应速率:实验3 >实验2 >实验1
D.实验2中平衡时的c(COS)约为0.0286 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,向10 mL 0.40 mol·L-1 H2O2溶液中加入适量FeCl3溶液,不同时刻测得生成O2的体积(已折算为标准状况)如下表所示。( )
t / min | 0 | 2 | 4 | 6 |
V(O2) / mL | 0 | 9.9 | 17.2 | 22.4 |
资料显示,反应分两步进行:
①2Fe3++ H2O2 ![]() 2Fe2++O2↑+2H+
2Fe2++O2↑+2H+
② H2O2 + 2Fe2++2H+ ![]() 2H2O+2Fe3+
2H2O+2Fe3+
反应过程中能量变化如右图所示。下列说法不正确的是
A.0~6 min的平均反应速率:v(H2O2) = 3.33×10-2 mol·L-1·min-1
B.Fe3+的作用是加快过氧化氢的分解速率
C.反应①是吸热反应、反应②是放热反应
D.反应2H2O2(aq) ![]() 2H2O(l) + O2(g)的△H =E1-E2 < 0
2H2O(l) + O2(g)的△H =E1-E2 < 0
查看答案和解析>>
科目: 来源: 题型:
【题目】观察下列实验装置图,回答问题:


(1)石灰水长时间露置于空气中,溶液表面会产生一层“膜”,“膜”物质的化学式是____,可用上图中________装置(填序号)进行相关实验操作除去膜物质。
(2)提纯含有少量NaCl的KNO3,可将混合物溶解在热水中形成饱和溶液,然后在②装置中进行蒸发浓缩,________后进行过滤、________、干燥。
(3)实验室制Cl2用装置③吸收尾气,集气瓶中可放入________溶液,尾气应从_______通入(填a、b)。
查看答案和解析>>
科目: 来源: 题型:
【题目】铁红(主要成分为Fe2O3)是一种用途广泛的颜料,用废铁屑制备铁红的流程如下:

(1)操作Ⅰ的名称是_________。
(2)检验FeCO3沉淀是否洗净的实验方法是________。
(3)加入NH4HCO3溶液的反应除了生成FeCO3沉淀,还会生成一种气体,生成气体的离子方程式为________。
(4)在空气中煅烧FeCO3的化学方程式是________,若煅烧不充分,产品Fe2O3中会有FeO,为了避免产品中有FeO,可以采取的措施是________。
(5)称取3.0 g 产品,用稀硫酸溶解,逐滴加入0.10 mol·L-1 KMnO4溶液20.00 mL,二者恰好反应完全。若此产品中只含有FeO、Fe2O3,求算产品中Fe2O3的质量分数,写出计算过程___。
(已知:10FeSO4+2KMnO4+8H2SO4===5Fe2(SO4)3+2MnSO4+K2SO4+8H2O)
查看答案和解析>>
科目: 来源: 题型:
【题目】若甲烷与氯气以物质的量之比1:1混合,在光照下得到的有机取代产物是( ) ①CH3Cl、②CH2C12、③CHCl3、④CCl4 .
A.只有①
B.只有③
C.①②③的混合物
D.①②③④的混合物
查看答案和解析>>
科目: 来源: 题型:
【题目】碘循环工艺不仅能吸收SO2降低环境污染,同时还能制得氢气,具体流程如下: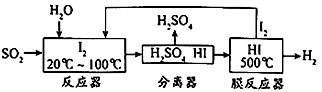
下列说法正确的是( )
A.分离器中的物质分离操作为过滤
B.膜反应器中,增大压强有利于提高HI的分解速率和平衡转化率
C.该工艺中I2和HI的相互转化体现了“碘循环”
D.碘循环工艺的总反应为2SO2+4H2O+I2 = H2+2H2SO4+ 2HI
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机化合物A广泛存在于多种水果中.
(1)经测定,A中仅含有C,H,O三种元素,67gA在空气中完全燃烧时可生成27g H2O和88g CO2 . 则A的实验式或最简式为 . 若要确定A的分子式,还需要知道A的相对分子质量,测定物质的相对分子质量可以采用(填“质谱”或“红外光谱”)法.
经测定A的相对分子质量为134,则A的分子式为 .
(2)又知1molA与足量的NaHCO3溶液充分反应可生成标准状况下的CO2气44.8L,1molA与足量的Na反应可生成1.5mol的H2 , 则A分子中所含官能团的名称为 .
(3)若A分子中不存在甲基且有一个手性碳原子,则A的结构简式为 . 该A在浓硫酸存在下加热,可以生成多种产物,请写出A发生消去反应后所得有机产物的结构简式 .
(4)A的一种同分异构体B,与A所含官能团的种类和数目均相同,且能催化氧化成醛,则B的1H核磁共振谱图中将会出现组特征峰.
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化还原反应原理在生产生活和科学研究中应用广泛。
(1)下列表述中没有氧化还原反应发生的是________。
a.滴水成冰 b.蜡炬成灰 c.百炼成钢
(2)NH3和Cl2反应的方程式为: NH3+ Cl2—N2+ HCl
①该反应中被氧化的元素是________(填元素名称),氧化剂是______(填化学式)。
②配平该方程式:NH3 + Cl2 — N2 + HCl __
③工业生产中常用喷洒氨水的方法来检查是否有Cl2泄漏,若Cl2有泄漏,可以观察到的现象是________,产生该现象的反应方程式为________。
(3)“地康法”制氯气的反应原理图示如下:

①反应I的化学方程式为________。
②反应II属于________反应。(填四种基本反应类型之一)。
③若要制得标准状况下氯气11.2L,则整个反应中转移电子的物质的量为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】合理使用药物是保证身心健康、提高生活质量的有效手段.药物化学已经成为化学的一个重要领域.
(1)我国科学家屠呦呦因发现治疗疟疾的特效药﹣﹣青蒿素,而获得2015年诺贝尔生理学或医学奖.青蒿素的结构简式如图所示,其含有的过氧基(﹣O﹣O﹣)具有强氧化性. 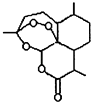
请回答下列问题:
①青蒿素的分子式为 .
②下列有关青蒿素的叙述中,正确的是(填字母).
A、青蒿素属于芳香族化合物
B、青蒿素具有强氧化性,可用于杀菌
C、青蒿素分子中的所有碳原子在同一个平面上
D、在一定条件下,青蒿素能与NaOH溶液发生反应
(2)阿司匹林(乙酰水杨酸) ![]() 是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为
是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为 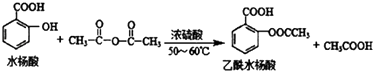
请回答下列问题:
①乙酰水杨酸中的含氧官能团的名称为
②制得的阿司匹林中常含有少量的杂质水杨酸,下列试剂可用于检验阿司匹林样品中是否混有水杨酸的是(填字母).
A、碳酸氢钠溶液 B、三氯化铁溶液 C、石蕊试液
③写出水杨酸与足量的NaHCO3溶液完全反应所得有机产物的结构简式: .
(3)丙烷的一氯代物有种,写出其一氯代物在氢氧化钠醇溶液共热条件下的有机产物的结构简式 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于氧化还原反应的叙述中正确的是( )
A.失去电子的反应为还原反应
B.含有氧元素的物质是氧化剂
C.氧化剂得到电子的数目和还原剂失去的电子的数目一定相等
D.氧化剂和还原剂不可能是同一种物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com