
科目: 来源: 题型:
【题目】氯气可用于制取漂白剂和自来水消毒。
(1)将氯气通入水中制得氯水,氯水可用于漂白,其中起漂白作用的物质是 (填写化学式)。
(2)“84”消毒液也可用于漂白,其工业制法是控制在常温条件下,将氯气通入NaOH溶液中,反应的离子方程式为。
(3)同学们探究“84”消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售“84”消毒液稀释100倍,测得稀释后溶液的pH=12;
步骤2:取稀释后溶液各20 mL分别加入3个洁净的小烧杯中;
步骤3:用硫酸将3个烧杯内溶液的pH分别调至10、7和4。(溶液体积变化忽略不计)
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
烧杯 | 溶液的pH | 现象 |
a | 10 | 10 min后,红纸基本不褪色;4h后红纸褪色 |
b | 7 | 10 min后,红纸颜色变浅;4 h后红纸褪色 |
c | 4 | 10 min后,红纸颜色变得更浅;4h后红纸褪色 |
已知,溶液中Cl2、HC1O和ClO-物质的量分数(α) 随pH变化的关系如下图所示:
①由实验现象可获得以下结论:溶液的pH在4 ~10范围内,pH越大,红纸褪色。
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是。
(4)由于氯气会与自来水中的有机物发生反应,生成对人体有害的物质,人们尝试研究并使用新的自来水消毒剂,如ClO2气体就是一种新型高效含氯消毒剂。
①一种制备ClO2的方法是将SO2通入硫酸酸化的NaClO3溶液中,反应的离子方程式为。
②另一种制备ClO2的方法是用NaClO3与盐酸反应,同时有Cl2生成,产物中Cl2体积约占1/3。则每生成0.5 mol ClO2 , 转移mole-。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,向1L密闭容器中加入1mol HI(g),发生反应2HI(g)H2(g)+I2(g),2s时生成0.1mol H2 , 则以HI表示该时段的化学反应速率是( )
A.0.05 molLˉ1sˉ1
B.0.1 molLˉ1sˉ1
C.0.2 molLˉ1sˉ1
D.0.8 molLˉ1sˉ1
查看答案和解析>>
科目: 来源: 题型:
【题目】为了研究化学反应A+B═C+D的能量变化情况,某同学设计了如图所示装置.当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升.试回答下列问题:

(1)该反应为 __________ 反应(填“放热”或“吸热”).
(2)A和B的总能量比C和D的总能量 __________ (填“高”或“低”).
(3)物质中的化学能通过化学反应转化成 ________________ 释放出来.
(4)反应物化学键断裂吸收的能量 ______ (填“高”或“低”)于生成物化学键形成放出的能量.
(5)写出一个符合题中条件的化学方程式: ________________________________________________________________________________
Ⅱ.已知:P4(白磷,s)+5O2(g)═P4O10(s)△H=-2 983.2kJmol-1①
P(红磷,s)+![]() O2(g)═
O2(g)═![]() P4O10(s)△H=-738.5kJmol-1 ②
P4O10(s)△H=-738.5kJmol-1 ②
则白磷转化为红磷的热化学方程式为 _________________________________________ .相同状况下,能量状态较低的是 __________ ;白磷的稳定性比红磷 ______ (填“高”或“低”).
查看答案和解析>>
科目: 来源: 题型:
【题目】肼(N2H4)是火箭发动机的燃料,反应时N2O4为氧化剂,生成氮气和水蒸气.已知:N2(g)+2O2(g)=N2O4(g)△H=+8.7kJ/mol;N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534.0kJ/mol.下列表示肼跟N2O4反应的热化学方程式,正确的是( )
A. 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=-542.7kJ/mol
B. 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=-1059.3kJ/mol
C. 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=-1076.7kJ/mol
D. N2H4(g)+![]() N2O4(g)=
N2O4(g)=![]() N2(g)+2H2O(g)△H=-1076.7kJ/mol
N2(g)+2H2O(g)△H=-1076.7kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】合成氨是人类科学技术上的一项重大突破,是化学和技术对社会发展与进步的巨大贡献之一.在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒.除去CO的化学反应方程式(HAc表示醋酸):Cu(NH3)2Ac+CO+NH3═Cu(NH3)3(CO)Ac. 请回答下列问题:
(1)C,N,O的第一电离能由大到小的顺序为 .
(2)写出基态Cu+的核外电子排布式 .
(3)配合物Cu(NH3)3(CO)Ac中心原子的配位数为
(4)写出与CO互为等电子体的离子: . (任写一个)
(5)某化合物的晶胞如图所示,写出该化合物的化学式 , 距离每个X+最近的Cl﹣的个数为 . 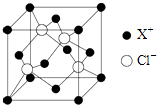
查看答案和解析>>
科目: 来源: 题型:
【题目】一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO).
(1)向一定物质的量浓度的Cu(NO3)2 和Mn(NO3)2 溶液中加入Na2CO3 溶液,所得沉淀经高温灼烧,可制得CuMn2O4 . ①写出基态Mn原子的价电子排布式为 .
②CO32﹣的空间构型是(用文字描述).
(2)在铜锰氧化物的催化下,CO 被氧化为CO2 , HCHO 被氧化为CO2 和H2O. ①根据等电子体原理,CO 分子的结构式为 .
②CO2 分子中C 原子轨道的杂化类型为 .
③1mol甲醛(HCHO)分子中含有的σ键数目为 .
(3)向CuSO4溶液中加入过量NH3﹒H2O溶液可生成[Cu (NH3)4]2+ . 不考虑空间构型,[Cu (NH3)4]2+的结构可用示意图表示为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是( )
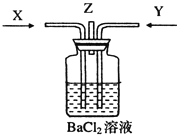
A. 洗气瓶中产生的沉淀中有碳酸钡 B. 在Z导管出来的气体中无二氧化碳
C. 洗气瓶中产生的沉淀是硫酸钡 D. 洗气瓶中无沉淀产生
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸铜是一种重要的化工产品。某工厂用刻蚀印刷电路板产生的碱性废液[含较多[Cu(NH3)4]2+及少量Cu2+、NH4+、NH3和Cl-]制备硫酸铜晶体,流程如下:
(1)通过“中和、沉淀和过滤”可得碱式氯化铜[Cu(OH)Cl]固体,请将生成该固体的反应的离子方程式补充完整:[Cu(NH3)4]2+ +。
(2)制备Cu(OH)Cl沉淀时,溶液的pH对铜元素含量的影响如下图所示:
①若要提高Cu(OH)Cl沉淀的量,应将溶液的pH控制在(填字母序号)。
A. <5.2 B. 5.2~5.8 C. >5.8
②pH< 5.2 时,随pH减小,溶液中铜元素含量增大,其原因用反应的离子方程式可表示为。
(3)“化浆、酸化"过程可得到硫酸铜粗品,发生的反应为Cu(OH)Cl+ 4H2O+ H2SO4= CuSO4·5H2O+ HCl。则硫酸铜粗品中,含铜元素的杂质为 , 检验样品中含有该杂质的方法是:取少量硫酸铜粗品,加入适量水使其充分溶解,。
(4)硫酸铜粗品还需要通过重结晶法进行提纯,具体操作是:将粗晶体溶解于热水中形成饱和溶液,然后加入适量乙醇,搅拌,冷却,过滤并洗涤,得到高纯度的硫酸铜晶体。加入乙醇能够提高硫酸铜的产率,从溶解性角度解释其可能的原因是。
查看答案和解析>>
科目: 来源: 题型:
【题目】有机化合物分子中的基团之间存在着相互影响.
(1)在甲烷、苯、甲苯这三种物质中,可以使酸性高锰酸钾溶液褪色的有(填名称),能用于制取炸药梯恩梯(TNT)的是(填分子式).
(2)某学习小组通过实验探究①苯酚、②醋酸、③碳酸这三种物质分子中的羟基在水中电离能力的强弱.主要实验步骤如下: a、取三支试管,分别加入三种物质的水溶液(适量),再分别滴加2~3滴紫色石蕊试液,发现仅②、③的溶液变红.
b、另取一支试管,加入少量滴加了酚酞的NaOH溶液,再滴加①的溶液,发现试管中溶液的红色明显变浅.
c、再取一支试管,加入少量碳酸钠溶液,向其中滴加②的溶液,发现有气体生成.
d、将CO2气体通入苯酚钠的水溶液中,发现溶液变浑浊.
请回答以下问题:
①步骤b的现象说明苯酚具有性.
②步骤d中,发生反应的化学方程式为 .
③三种物质分子中的羟基在水中的电离能力由强到弱的顺序是(填序号).
④在苯酚分子中,羟基对苯基的性质也有影响.写出苯酚与浓溴水反应生成的有机产物的结构简式: .
(3)同学甲设计了如右图所示的实验装置一次性地验证苯酚、醋酸、碳酸的酸性强弱.同学乙认为该实验装置设计的不严密,理由是 . 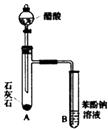
查看答案和解析>>
科目: 来源: 题型:
【题目】A~J是常见的化学物质,转化关系如下图所示。A是生活中的一种调味剂,I是一种用途广泛的金属,常温下C、D、E、F、J皆为气体, H由两种元素构成,摩尔质量为41 g·mol-1。

(1)I的化学式为________,H的化学式为________。
(2)写出反应①②③④的化学方程式
①_______;②________; ③_______; ④________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com