
科目: 来源: 题型:
【题目】已知某温度下,反应2SO2+O22SO3 , 的平衡常数K=19,在该温度下的体积固定的密闭容器中充入C(SO2)=1molL﹣1 , C(O2)=1 molL﹣1 , 当反应在该温度下SO2 , 为80%时,该反应(填“是”或“否”)达到化学平衡状态,若未达到,向(填“正反应”或“逆反应”)方向进行.
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学实验小组的同学为探究和比较SO2和氯水的性质,设计了如下的实验装置。
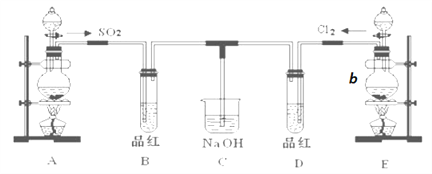
(1)实验室用装置A制备SO2。试剂组合最好是________。
a.稀 H2SO4+Cu b.浓HNO3+Na2SO3 c.70% H2SO4+K2SO3
(2)实验室用装置E制备Cl2,仪器b中装有MnO2粉末。写出仪器b的名称_______,该实验制备Cl2的化学方程式 ___________________________。若该反应消耗8.7g氧化剂,则参加反应的还原剂的物质的量为_____________mol;
(3)反应开始一段时间后,观察到B试管中的品红溶液出现的现象是:_____________;完全反应后,停止通气,再给D试管加热,D试管现象是__________________。
(4)C装置的作用是_______________________。
(5)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图表示在密闭容器中反应:2SO2+O22SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是;bc过程中改变的条件可能是; 若增大压强时,反应速度变化情况画在c~d处 . 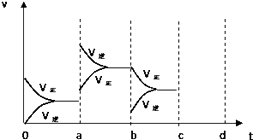
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室需用2 mol·L-1氯化钠溶液450 mL,配置时应选用容量瓶的规格和称取氯化钠的质量分别是
A. 450 mL,52.7g B.500 mL,58.5g
C.1000 mL,117g D.任意规格,111.2g
查看答案和解析>>
科目: 来源: 题型:
【题目】遇到下列情况,处理得当的是( )
A. 不小心将少量浓硫酸沾到皮肤,立即用水冲洗。
B. 皮肤上沾有浓碱溶液时,立即用盐酸洗。
C. 为了避免浪费,应该把实验用剩的药品放回原试剂瓶中。
D. 连接并组装成套仪器时,一般按自上而下、从左到右的顺序进行安装。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)0.5 mol H2O的质量为____ ,含有______个原子。
(2)质量都是50 g的 HCl、CH4、N2三种气体中,原子数目最多的是气体是_______ ,在相同温度和相同压强条件下,密度最大的气体是__________ 。
(3)标准状况下11.2L,由CO和H2组成的混合气体的质量为7.2g,则混合气体的平均摩尔质量为_______。
(4)实验室需用浓硫酸配制100 mL 1 molL-1的稀硫酸。可供选用的仪器有:
①量筒;②烧杯;③胶头滴管,还必须需要的玻璃仪器有________________ (写仪器名称)。
(5)一定条件下,RO![]() 和Cl2可发生如下反应:RO3n-+Cl2+H2O==RO42-+2Cl-+2H+ ,从而可知在RO
和Cl2可发生如下反应:RO3n-+Cl2+H2O==RO42-+2Cl-+2H+ ,从而可知在RO![]() 中,元素R的化合价是_____,当有标准状况下8.96L Cl2被消耗时,反应中共转移电子物质的量为____mol。
中,元素R的化合价是_____,当有标准状况下8.96L Cl2被消耗时,反应中共转移电子物质的量为____mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验时,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气.为了验证甲、乙两位同学的判断是否正确,丙同学设计了如图所示的实验装置(锌与浓硫酸共热时产生的气体为X,反应装置略去).
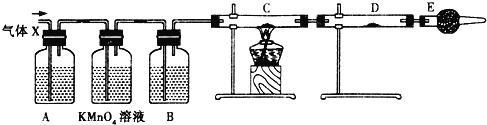
注:C中为氧化铜粉末,试回答下列问题:
(1)上述反应中生成二氧化硫的化学方程式为:________________________________;
(2)乙同学认为还可能产生氢气的理由是:____________________________________;
(3)丙同学在安装好装置后,必不可少的一步操作是:__________________________;
(4)A中试剂是______,D中试剂是______;
(5)E装置的作用是_________________________;
(6)可以证明气体X中含有氢气的实验现象是:______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅.
时间(s) | 0 | 20 | 40 | 60 | 80 | 100 |
C(N2O4) | 0.20 | a | 0.10 | c | d | e |
C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
(1)该反应的化学方程式为 , 表中bc(填“<”、“=”、“>”).
(2)20s时,N2O4的浓度为mol/L,0~20s内N2O4的平均反应速率为 .
(3)该反应的平衡常数表达式K= , 在80℃时该反应的平衡常数K值为(保留2位小数).
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时 . A、N2O4的转化率越高 B、NO2的产量越大
C、N2O4与NO2的浓度之比越大 D、正反应进行的程度越大.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com