
科目: 来源: 题型:
【题目】可逆反应X(g)+Y(g)2N(g)(正反应为放热反应)从反应开始到t1 s达到平衡,在t2 s末由于条件改变,平衡被破坏,在t3 s末又建立新的平衡.图中表示上述变化过程中X和N的浓度(c)与反应时间的关系.在t2 s~t3 s之间的曲线变化是由下列哪种条件改变引起的( ) 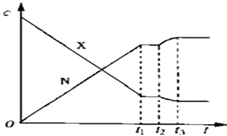
A.降低温度
B.增大N的浓度
C.减小X的浓度
D.增大压强
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2]是一种重要的化工原料,下列有关说法正确的是( )
A.Na+、Fe3+、NO3﹣、Cl2都可在该物质的溶液中大量共存
B.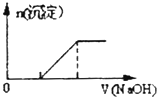
向O.1mo1﹣L﹣1该物质的溶液中清加0.Lmol﹣1NaOH溶液,生成沉淀的物质的量与逐滴加入NaOH溶液体积关系如图所示
C.检验该物质中Fe2+是否变质的方法是向该物质的溶液中滴入几滴KSCN溶液,观察溶液是否变红色
D.向该物质的溶液中摘加Ba(OH)2溶液,恰好使SO42﹣完全沉淀的离子方程式为:Fe2++2SO42﹣+3Ba2++2OH﹣═2BaSO4↓+Fe(OH)2↓
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为一个装有活塞的密闭容器,内盛有22.4mL的NO,若通入11.2mL的O2(体积为标况下测得),保持温度,压强不变,则容器中的密度为( ) ![]()
A.等于1.369g/L
B.等于2.054g/L
C.于1.369g/L和2.054g/L之间
D.大于2.054g/L
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.铁粉溶于氯化铁溶液:Fe+2Fe3+═3Fe2+
B.硫化钠溶液呈碱性:S2﹣+2H2OH2S+OH﹣
C.用FeCl3溶液回收废旧电路板中的Cu:Fe3++Cu═Fe2++Cu2+
D.工业上利用电解饱和食盐制氯气:2H++2Cl﹣ ![]() H2↑+Cl2↑
H2↑+Cl2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】中学化学中几种常见物质的转化关系如图K8﹣4所示.将D溶液滴入沸水中可得到以F为分散质的红褐色胶体.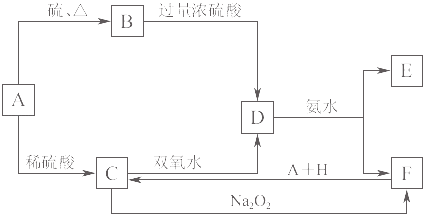
请回答下列问题:
(1)红褐色胶体中F粒子直径大小的范围: .
(2)A,B,H的化学式:A、B、H .
(3)①H2O2分子的电子式为 .
②写出C的酸性溶液与双氧水反应的离子方程式: .
(4)写出鉴定E中阳离子的实验方法和现象: .
(5)在C溶液中加入与C等物质的量的Na2O2 , 恰好使C转化为F,写出该反应的离子方程式: .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于胶体说法正确的是
A. 有些胶体是纯净物,有些胶体是混合物
B. 胶体、溶液和浊液的本质区别是能否产生丁达尔效应
C. 胶体不带电荷
D. 胶体分散质粒子的直径在10-9~10-7cm
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关酸、碱、盐的说法正确的是
A. 能电离出H+的化合物称为酸 B. 水溶液显碱性的化合物是碱
C. 盐中一定含有金属阳离子 D. 酸、碱、盐在一定条件下都能发生电离
查看答案和解析>>
科目: 来源: 题型:
【题目】碘是人体不可缺少的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去.某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:在溶液中 KIO3+5KI+3H2SO4═3I2+3H2O+3K2SO4
(1)用双线桥表示该反应中电子转移的方向和数目 , 该反应中还原产物与氧化产物的物质的量比是 , 0.2mol KIO3参加反应时转移电子mol
(2)实验结束后分离I2和K2SO4溶液所用的试剂是 ,
A.CCl4 B.酒精 C.Na2SO4溶液 D.食盐水
所用的分离方法是 , 所用主要玻璃仪器是
(3)上面实验中用到一定物质的量浓度的稀硫酸,若配制1mol/L的稀硫酸溶液480mL,需用18mol/L浓H2SO4mL,配制中需要用到的主要玻璃仪器是(填序号) .
A.100mL量筒 B.托盘天平 C.玻璃棒 D.100mL容量瓶 E.50mL 量筒 F.胶头滴管 G.烧杯 H.500mL容量瓶
(4)下面操作造成所配稀硫酸溶液浓度偏高的是
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com