
科目: 来源: 题型:
【题目】实验室中将盛有甲烷与氯气的混合气体的量筒倒立在盛有饱和食盐水的水槽中,光照使其发生反应,下列说法错误的是( )
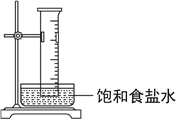
A. 通过量筒内壁上出现的油状液滴可以说明生成四种有机产物
B. 氯化氢极易溶于水,导致量筒中液面上升
C. 饱和食盐水能够抑制氯气的溶解
D. 量筒中气体颜色逐渐变浅
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值.下列叙述中不正确的是( )
A.分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA
B.28g乙烯(C2H4)和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA
C.常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
D.常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】已知![]() (b)、
(b)、![]() (d)、
(d)、![]() (p)的分子式均为C6H6,下列说法正确的是( )
(p)的分子式均为C6H6,下列说法正确的是( )
A. b的同分异构体只有d和p两种
B. 它们的二氯代物均只有三种
C. 它们均可与酸性高锰酸钾溶液反应
D. 只有b的所有原子处于同一平面
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA表示阿伏伽德罗常数值.下列说法正确的是( )
A.1L0.1mol/L的NaHCO3溶液中HCO3﹣和CO3 2﹣离子数之和为0.1NA
B.标准状况下,22.4LC2H4与C3H6混合气体所含有分子数为NA
C.1molNa2O2与足量的CO2反应转移的电子数为2NA
D.18gNH4+所含的电子数11NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述错误的是( )
A.光导纤维的主要成分是硅酸盐B.金属钠着火时不可以用水灭火
C.氧化铁常用作红色油漆和涂料D.常温下可用铝制容器盛装浓硫酸或浓硝酸
查看答案和解析>>
科目: 来源: 题型:
【题目】金属钠与水的反应是中学化学中的一个重要反应。高一化学教材中该实验曾出现过几种不同的演示方法。分别如下图中(A)(B)(C)所示:

(1)现按图(A)所示的方法,在室温时,向盛有饱和Na2CO3溶液(滴有几滴酚酞)的烧杯中,加入一小块金属钠。
①不可能观察到的现象是___________(填字母代号)。
A.钠浮在液面上,并四处游动,最后消失
B.反应过程中钠熔化成一个光亮的小球
C.反应开始后,溶液由无色变红色
D.恢复到室温时,烧杯底部有固体物质析出
②按图(B)所示方法来收集产生的气体,需将钠包好,再放入水中。取相同质量的钠按下列几种情况收集产生的气体,在相同条件下体积最大的是______(填字母代号)。
A.用扎有小孔的铝箔包住钠
B.用扎有小孔的铜箔包住钠
C.直接将钠投人水中
(2)按图(C)所示的方法进行该实验,若500mL的矿泉水瓶开始时装有477.6mL水,用手挤压矿泉水瓶至水刚好充满矿泉水瓶并塞紧带有钠的塞子,要使倒置的矿泉水瓶正好恢复原状,假设矿泉水瓶内外均为标准状况,则大头针上扎着的钠粒质量约为_______g。
(3)1998年全国高考试题中的实验题就是根据图(B)的原理设计的。题目及部分答案如下:测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数。现有下列实验用品:800毫升烧杯、10毫升量筒、短颈玻离漏斗、长颈漏斗、玻璃棒、铜网、铝锌合金样品、浓盐酸(密度1.19克/毫升)、水。按图示装置进行实验,回答下列问题。(设合金样品完全反应产生的气体体积不超过100毫升。)
I、补充下列实验步骤,直到反应开始进行(铁架台和铁夹的安装可省略):
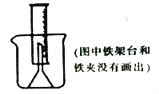
①将称量后的合金样品用铜网小心包裹好,放在800毫升烧杯底部,把短颈漏斗倒扣在样品上面。……
[答案]
②往烧杯中注入水,直至水面没过漏斗颈。[评分标准,凡加水改为加酸者,不论其他后续步骤是否正确,本小题一律0分]
③在100毫升量筒中装满水,倒置在盛水的烧杯中(量筒中不应留有气泡),使漏斗颈插入量筒中。烧杯中水面到杯口至少保留约100毫升空间。
④将“仪器A”插入烧杯并接近烧杯底部,通过它慢慢加入浓盐酸,至有气体产生。
回答下列问题:
a.合金样品用用铜网包裹的目的是______________。
b.为什么在“②往烧杯中注入水,直至水面没过漏斗颈”这一步中改加水为加酸会得0分(请写出两条原因):_____________________。
c. “仪器A”可以是_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】粉煤灰(主要含有SiO2、Fe2O3、Al2O3等)是燃煤发电过程中产生的废渣,粉煤灰的综合利用具有很大的价值.
Ⅰ.研究人员通过实验对粉煤灰中铝和铁元素的分离工艺进行了研究.
(1)以硫酸溶液分解粉煤灰,使其中的铝、铁元素溶出,过滤实现初步分离.
①写出硫酸溶液与Fe2O3反应的离子方程式 .
②初步分离得到的滤渣主要成分是 .
(2)向(1)分离所得的滤液中加入还原剂使Fe3+转化为Fe2+ , 结合表分析其原因 .
物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
沉淀区间(pH) | 7.06~8.95 | 1.94~3.20 | 3.69~4.8 |
(3)使用碱性较弱的氨水为pH调节剂,进行分离实验.
①氨水使滤液中铝离子沉淀的离子方程式为 .
②反应终点的pH对铝和铁分离效果的影响如图1.根据实验结果,为达到好的分离效果,反应过程中控制pH的范围是 , 选择该范围的理由是 . 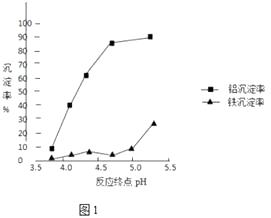
(4)Ⅱ.NH4HSO4和H2SO4按物质的量比1:1混合配制成浸取液,220℃时,可将高铝粉煤灰中Al2O3转化为硫酸铝铵[NH4Al(SO4)2],然后分离、煅烧获得纯Al2O3 .
已知硫酸铝铵:①溶解度:0℃时,S=5.2g;100℃时,S=421.9g.
②280℃时分解.
依据资料可知,将硫酸铝铵与其他溶质分离的方法是 .
(5)煅烧NH4Al(SO4)2同时得到混合气体(NH3、N2、SO2、SO3、H2O).若16mol混合气体按图2装置被完全吸收制得浸取液,请将图2中试剂及其物质的量补充完整.
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是一些含氯产品。

(1)储氯钢瓶中应贴的标签为_________(填字母代号)。
A.易燃品 B.有毒品 C.爆炸品
(2)“威猛先生”使用注意事项中特别说明在使用时切勿与漂白剂一同使用,否则会产生有害气体。“84”消毒液的有效成分是次氯酸钠,写出“84”消毒液与“威猛先生”(有效成分为盐酸)混合后反应的离子方程式_______。
(3)漂白粉的有效成分是_______(填化学式),老师新买的漂白粉没有保存说明书,请你为漂白粉设计一份保存注意事项,并用化学用语解释设计原因。
注意事项(不超过30个字):_________________。
解释(用化学用语):___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com