
科目: 来源: 题型:
【题目】标准状况下1mol烃完全燃烧时,生成89.6L CO2 , 又知0.1mol此烃能与标准状况下4.48L H2加成,则此烃的结构简式是( )
A.CH3CH2CH2CH3
B.CH3﹣C≡C﹣CH3
C.CH3CH2CH═CH2
D.CH2═CH﹣CH═CH﹣CH3
查看答案和解析>>
科目: 来源: 题型:
【题目】2016年IUPAC命名117号元素为TS(中文名![]() ,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
A. TS是第七周期第ⅦA族元素 B. TS的同位素原子具有相同的电子数
C. TS在同族元素中非金属性最弱 D. 中子数为176的TS核素符号是![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质分类正确的是( )
A. SO2、SiO2、CO、CO2均为酸性氧化物,也为非金属氧化物
B. 干冰、氨气、冰水混合物均为纯净物,也为化合物
C. 稀豆浆、雾、淀粉溶液、氯化铁溶液均为胶体,也为混合物
D. 粗盐、酸雨、盐酸、胆矾(CuSO4·5H2O)均为混合物
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:某废水中可能含有H+、NH4+、Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品100 mL,进行了三组实验,其操作和有关图像如下所示:
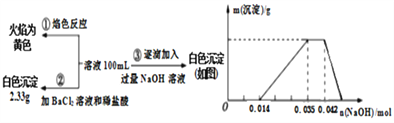
请回答下列问题:
(1)根据上述3组实验可以分析废水中一定不存在的阴离子是______________,一定存在的阳离子是______________________。
(2)写出实验③图像中沉淀达到最大量且质量不再发生变化阶段发生反应的离子反应方程式:_____________________________________________。
(3)分析图像,在原溶液中c(NH4+)与c(Al3+)的比值为________,所得沉淀的最大质量是____g。
(4)若通过实验确定原废水中c(Na+)=0.14 mol·L-1,c(NO3-)=____________ mol·L-1。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于实验基本操作的叙述不正确的是( )
A. 使用分液漏斗和容量瓶时,首先要查仪器是否漏液
B. 蒸馏实验中,要在烧瓶中加入几粒沸石或碎瓷片,以防止液体发生暴沸
C. 用蒸发皿进行加热蒸发时,不需垫石棉网可直接进行
D. 将浓硫酸倒入盛水的量筒中稀释成稀硫酸
查看答案和解析>>
科目: 来源: 题型:
【题目】某学生用0.1032molL﹣1的盐酸标准溶液滴定未知浓度的KOH溶液,其操作分解为如下几步: A.取已用蒸馏水洗净的酸式滴定管,用盐酸标准溶液润洗滴定管2~3次;
B.移取20mL待测KOH注入洁净的锥形瓶中,并加入2~3滴甲基橙;
C.取标准盐酸溶液注入酸式滴定管至“0”刻度以上1~2cm;
D.把盛有标准溶液的酸式滴定管固定好,调节滴定管尖嘴使之充满溶液;
E.调节液面至“0”或“0”以下某一刻度,记录读数;
F.把锥形瓶放在滴定管的下面,用标准盐酸滴定至终点并记录滴定管液面的刻度.
完成下列问题:
(1)上述操作步骤的正确顺序是(填写字母序号).
(2)判断溶液到达滴定终点的方法是 .
(3)上述A步骤操作的目的是 .
(4)若上述B步骤操作之前,先用待测液润洗锥形瓶,则对滴定结果产生的影响是;若称取一定量的KOH固体(含少量NaOH)配制待测溶液并用上述盐酸标准溶液进行滴定,则对滴定结果产生的影响是 , 理由是 .
(5)用0.1032molL﹣1的盐酸滴定未知浓度的KOH溶液,重复三次的实验数据如下表所示:
序号 | 消耗盐酸的体积/mL | 待测KOH溶液的体积/mL |
1 | 27.23 | 25.00 |
2 | 28.24 | 25.00 |
3 | 27.25 | 25.00 |
则待测KOH的物质的量浓度是molL﹣1 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图像均为实验过程中产生沉淀的物质的量(Y)与加入试剂的量(X)之间的关系图,则其中正确的是( )


A B C D
A. 向AlCl3溶液中逐滴加入NaOH溶液至过量且边滴边振荡
B. 向NaAlO2溶液中逐滴滴加稀盐酸至过量且边滴边振荡
C. 向NH4Al(SO4)2溶液中逐滴加入NaOH溶液直至过量
D. 向等物质的量浓度的NaOH、Ba(OH)2、NaAlO2的混合溶液中逐渐通入CO2至过量
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:氮气和氢气合成氨反应为:N2(g)+3H2(g)═2NH3(g)△H=﹣92kJmol﹣1请回答下列问题:
(1)取1mol N2(g)和3molH2(g)充入一密闭容器中,一定条件下进行反应并达平衡时,测得反应放出的热量92kJ(填“大于”、“等于”或“小于”),原因是;若升高温度,上述反应中△H(填“变大”、“变小”或“不变”).
(2)已知:分别破坏1molN﹣H键、1mol H﹣H键需要吸收的能量为:391kJ、436kJ,则破坏1mol N≡N键需要吸收的能量为 .
(3)一定条件下,向体积为2L的恒容密闭容器中充入1molNH3(g) 并发生上述反应.半分钟后反应达到平衡,测得v(NH3)=0.40mol/(Lmin),则上述合成氨反应的平衡常数为 .
(4)向三个体积均为1L的恒容密闭容器中分别充入1molN2和3molH2 , 当分别只改变其中一个外界条件时使反应达到平衡,测得氨的体积分数随时间的变化如图所示. 
上述图像中,只改变温度的为(填“I”“II”“III”,下同),只改变压强的为 , 只改变催化剂的为 .
(5)若把标准状况下8.96L氨气通入到100g9.8%的硫酸溶液中并完全吸收,所得溶液中离子浓度从大到小的顺序是 .
(6)常温下,向浓度均为0.1mol/L的MgCl2、FeCl3和AlCl3混合溶液中通入NH3至过量,最先生成沉淀的化学式为 , 当pH=时,开始生成Mg(OH)2沉淀. (已知:Ksp[Mg(OH)2]=1.0×10﹣13; Ksp[Fe(OH)3]=1.0×10﹣40;Ksp[Al(OH)3]=1.0×10﹣33)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列组成生物体的化学元素中属于微量元素的一组是
A.C、H、N、P、MnB.C1、Fe、S、N、Mg
C.B、Cu、Zn、Mn、MoD.N、P、K、Cu、Fe、I
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com