
科目: 来源: 题型:
【题目】二氯化砜(SO2Cl2)是一种重要的有机合成试剂,实验室可利用SO2与Cl2反应制取少量的SO2Cl2。装置如图(有些支持装置省略了)所示。已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃;常温下比较稳定,受热易分解,遇水能发生剧烈的水解反应,产物之一为氯化氢气体。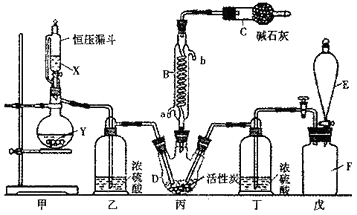
(1)仪器E的名称是 , 由B的使用可知SO2与氯气之间的反应属于(填“放”或“吸”)热反应,B处反应管冷却水应从 (填“a”或“b”)接口通入。如果将丙装置放入冰水中,会更有利于二氯化砜的生成,其原因是。
(2)试剂X、Y的组合最好是。
a.98%硫酸和铜 b.稀硝酸和亚硫酸钠固体 c.60%硫酸和亚硫酸钾固体
(3)戊是贮气装置,则E中的试剂是;若缺少装置乙和丁,潮湿的氯气和二氧化硫之间发生反应的化学方程式是 .
(4)取1.00g蒸馏后的液体,小心地完全溶于水,向所得的溶液中加入足量氯化钡溶液,测得生成沉淀的质量为1.50g,则所得馏分中二氯化砜的质量百分含量为 %(结果保留小数点后1位)。
(5)二氯化砜应储存于阴凉、干燥、通风良好的库房,但久置后微显黄色,其原因是。
查看答案和解析>>
科目: 来源: 题型:
【题目】银铜合金广泛用于航空工业。从切割废料中回收银并制备铜化工产品的工艺如下: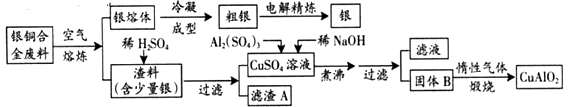
(注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃)
(1)固体混合物B的组成为;在生成固体B的过程中,需控制NaOH的加入量,若NaOH过量,则因过量引起的反应的离子方程式为。
(2)完成煅烧过程中一个反应的化学方程式:。
(3)若银铜合金中铜的质量分数为64%,理论上5.0kg废料中的铜可完全转化为CuAlO2 , 至少需要1.0mol·L-1的Al2(SO4)3溶液 L。
(4)某同学用FeCl3溶液吸收H2S,得到单质硫;过滤后,再以石墨为电极,在一定条件下电解滤液。
①FeCl3与H2S反应的离子方程式为。
②电解池中H+在阴极放电产生H2 , 阳极的电极反应为。
③综合分析实验II的两个反应,可知该实验有两个显著优点:
H2S的原子利用率100%;。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:① 
② ![]()
HPE是合成苯氧基丙酸类除草剂的重要中间体,其合成路线如下:
据此回答下列问题:
(1)B中含有的官能团名称为 , D的结构简式为。
(2)C + E →F的反应类型为。
(3)M的核磁共振氢谱中各吸收峰的面积之比为。
(4)写出G + M → HPE的化学方程式。
(5)X是G的同分异构体,其中满足以下条件的X共有种,写出其中一种X的结构简式。
A.苯环上有3个取代基且苯环上的一氯取代物有两种
B.遇FeCl3溶液发生颜色反应
C.X不能与NaHCO3反应产生CO2
D.1 mol X最多能和3 mol NaOH反应
查看答案和解析>>
科目: 来源: 题型:
【题目】欲测定烟雾中的SO2含量,可做下列实验:取100 L该烟雾(标准状况),通过盛放100 mL过氧化氢(H2O2)水溶液的吸收瓶,使它们充分反应,生成硫酸。在吸收后的水溶液中加入BaCl2溶液,生成白色沉淀,经测定其质量为11.65 g,则该烟雾中SO2的体积分数是( )
A. 1.12% B. 2.24%
C. 3.36% D. 无法计算
查看答案和解析>>
科目: 来源: 题型:
【题目】海水开发利用的部分过程如图所示。下列说法错误的是

A. 向苦卤中通入Cl2是为了提取溴
B. 粗盐可采用除杂和重结晶等过程提纯
C. 工业生产中常选用NaOH作为沉淀剂
D. 富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
查看答案和解析>>
科目: 来源: 题型:
【题目】在容积为2L的3个密闭容器中发生反应3A(g)+B(g)xC(g),按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 3mol A、2mol B | 6mol A、4mol B | 2mol C |
到达平衡的时间(min) | 5 | 8 | |
A的浓度(mol/L) | c1 | c2 | |
C的体积分数 | w1 | w3 | |
混合气体密度(g/L) | ρ1 | ρ2 |
下列说法正确的是( )
A.若x<4,则2c1<c2
B.若w3=w1 , 可断定x=4
C.无论x的值是多少,均有2ρ1=ρ2
D.容器甲中反应从开始到达平衡平均速率为v(A)=0.3 molL﹣1min﹣1
查看答案和解析>>
科目: 来源: 题型:
【题目】从淡化海水中提取溴的流程如下图所示,下列有关说法错误的是( )
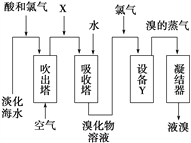
A. X为SO2气体,也可将SO2换成Na2SO3
B. 设备Y为蒸馏塔
C. 在提取溴的过程中一定有Br-被氧化
D. 工业上,每获得1 mol Br2,需要消耗Cl2的体积最多为44.8 L(标准状况)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组微粒具有相同的电子数的是( )
A.Ar、H2O2 和 C2H6B.CH4、Na+和 K+
C.SiH4、Al3+ 和 Ca2+D.OH﹣,S2﹣ 和 NH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com