
科目: 来源: 题型:
【题目】下列关于摩尔质量的描述或应用中,正确的是( )
A.1mol OH-的质量为17g/mol
B.二氧化碳的摩尔质量为44g
C.铁原子的摩尔质量等于它的相对原子质量
D.一个钠原子的质量等于23/(6.02×1023)g
查看答案和解析>>
科目: 来源: 题型:
【题目】现有A、B、C、D四种元素,其原子序数依次递增.已知,A、C为短周期非金属元素,其单质在常温下均为气体,两单质混合见光爆炸生成AC,AC溶液显强酸性.B、D为金属元素,B的原子序数为D的一半,D与C2和AC溶液反应分别得DC3和DC2 , 烧碱溶液不能与D单质反应,而能与B单质反应.请回答下列问题:
(1)C的原子结构示意图为;B在周期表中的位置是 。
(2)用电子式表示AC的形成过程 。
(3)写出B单质与NaOH溶液反应的离子方程式 。
(4)电浮选凝聚法是工业上采用的一种污水处理方法,右图是该方法处理污水的实验装置示意图(B、D金属单质作电极).实验过程中,污水的pH始终保持在5.0~6.0之间.接通电源后,阴极产生的气体将污物带到水面形成浮渣而刮去,起到浮选净化作用;阳极产生的沉淀具有吸附性,吸附污物而沉积,起到凝聚净化作用.阳极的电极反应有两个,分别是2H2O-4e-=4H++O2↑和 。阳极区生成沉淀的离子方程式是。 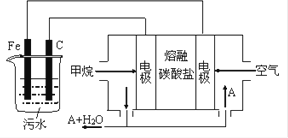
(5)一定条件下,2mol B与3mol D的氧化物W恰好反应,则W的化学式。
查看答案和解析>>
科目: 来源: 题型:
【题目】反应mA(s)+nB(g)pC(g)△H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是( ) 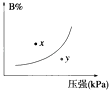
①m+n>p
②x点表示的正反应速率大于逆反应速率
③n>p
④x点比y点时的反应速率慢
⑤若升高温度,该反应的平衡常数增大.
A.①②⑤
B.②④
C.①③
D.①③⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】金属钛(Ti)被誉为21世纪金属,具有良好的生物相容性,它兼具铁的高强度和铝的低密度.其单质和化合物具有广泛的应用价值.氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品.以TiCl4为原料,经过一系列反应可以制得Ti3N4和纳米TiO2(如图1). 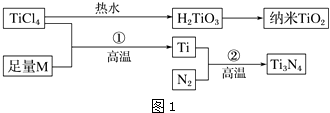
图1中的M是短周期金属元素,M的部分电离能如下表:
I1 | I2 | I3 | I4 | I5 | |
电离能/kJmol﹣1 | 738 | 1451 | 7733 | 10540 | 13630 |
请回答下列问题:
(1)Ti的基态原子外围电子排布式为;
(2)M是(填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为;
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示.化合物甲的分子中采取sp2方式杂化的碳原子有个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为; 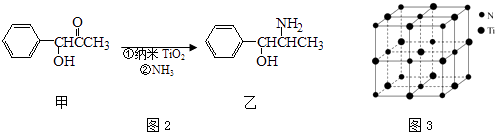
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为gcm﹣3(NA为阿伏加德罗常数的值,只列计算式).该晶体中与N原子距离相等且最近的N原子有个;
(5)科学家通过X﹣射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.且知三种离子晶体的晶格能数据如下:
离子晶体 | NaCl | KCl | CaO |
晶格能/kJmol﹣1 | 786 | 715 | 3401 |
KCl、CaO、TiN三种离子晶体熔点由高到低的顺序为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法错误的是( )
A.工业上电解熔融状态的Al2O3制备Al涉及氧化还原反应
B.四川灾区重建使用了大量钢材,钢材是合金
C.金属材料都是导体,非金属材料都是绝缘体
D.合金材料中可能含有非金属元素
查看答案和解析>>
科目: 来源: 题型:
【题目】黄铜矿(CuFeS2)是炼铜的最主要矿物,在野外很容易被误会为黄金,又称愚人金.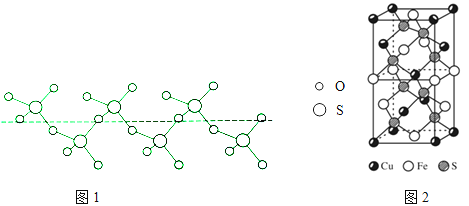
(1)火法冶炼黄铜矿的过程中,利用了Cu2O与Cu2S反应生成Cu单质,反应的化学方程式是
(2)S位于周期表中 族,该族元素氢化物中,H2Te比H2S沸点高的原因是 ,H2O比H2Te沸点高的原因是
(3)S有+4和+6两种价态的氧化物,回答下列问题:
①下列关于气态SO3和SO2的说法中,正确的是 .
A.中心原子的价层电子对数目相等 B.都是极性分子
C.中心原子的孤对电子数目相等 D.都含有极性键
②将纯液态SO3冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构如图1,此固态SO3中S原子的杂化轨道类型是
(4)Cu有+1和+2两种价态的化合物,回答下列问题:
①Cu+的价层电子排布为 ,Cu2+有 个未成对电子.
②新制的Cu(OH)2能够溶解于过量浓碱溶液中,反应的离子方程式是
(5)CuFeS2的晶胞如图2所示,晶胞参数a=0.524nm,c=1.032nm;CuFeS2的晶胞中每个Cu原子与 个S原子相连,列式计算晶体密度 ρ= gcm﹣3 .
查看答案和解析>>
科目: 来源: 题型:
【题目】可逆反应2NO2![]() 2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
A. ①④ B. ②③
C. ①③④ D. ①②③④
查看答案和解析>>
科目: 来源: 题型:
【题目】向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)![]() SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是
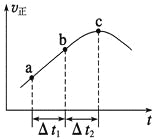
A. 反应在c点达到平衡状态
B. 反应物浓度:a点小于b点
C. 反应物的总能量低于生成物的总能量
D. Δt1=Δt2时,SO2的转化率:a~b段小于b~c段
查看答案和解析>>
科目: 来源: 题型:
【题目】在周期表中1~36号之间的W、X、Y、Z、Q六种元素,它们的原子序数依次增大,已知W与其余五种元素既不同周期也不同主族,X原子的L层p轨道中有2个电子,Y元素原子的最外层有3个自旋方向相同的未成对电子,Z元素原子基态时,核外电子排布在3个能级上,且有2个未成对电子.Q元素在第四周期,原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态.
(1)按电子排布,Q元素在周期表中属区.
(2)第一电离能YZ,电负性YZ(填“>”,“=”或“<”).
(3)W与Z形成的常见化合物有W2Z、W2Z2 , W与Y能形成多种二元化合物,如YW3、Y2W4、Y3W5、Y4W6…,W2Z分子中Z原子的杂化类型为 , YW3分子的立体构型为 , YW3极易溶于W2Z的主要原因有 .
(4)若向含有Q2+的硫酸盐溶液中滴加过量氨水,得到深蓝色溶液后再加乙醇,有深蓝色晶体析出,该晶体阳离子中含有的化学键有 .
(5)Q+与Y3﹣形成的晶胞结构如图所示,阴、阳离子间的核间距为 a pm,阿伏伽德罗常数用NA 表示,则晶体的密度为gcm﹣3 . 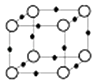
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com