
科目: 来源: 题型:
【题目】亚甲基蓝(MethyleneBlue)在碱性条件下与葡萄糖作用生成亚甲基白(MethyleneWhite)。亚甲基蓝的结构简式如下: 
著名的蓝瓶子实验的操作步骤如下:
①如上图所示,在250mL的锥形瓶中,依次加入2gNaOH、100mLH2O,3 gC6H12O6(葡萄糖),搅拌溶解后,再加入3~5滴0.2%的亚甲基蓝溶液,振荡,混合液呈现蓝色。
②关闭活塞a、b,塞紧瓶塞,将溶液静置,溶液变为无色。
③再打开瓶塞,振荡溶液又变为蓝色。
④关闭活塞a、b,再塞紧瓶塞,将溶液静置,溶液又变为无色。
以上③④可重复多次
试回答:
(1)某学生将起初配得的蓝色溶液装在A试管中(如上图,A试管充满溶液),塞上橡皮塞静置片刻,溶液变为无色。若振荡A试管,溶液能否再变为蓝色。(选填能或不能)
(2)若塞紧锥形瓶瓶塞并打开活塞a、b,通入足量氢气后,再关闭活塞a、b并振荡,溶液能否由无色变为蓝色(选填能或不能);若塞紧锥形瓶瓶塞并打开活塞a、b,通入足量氧气后,溶液能否由五色变为蓝色。(选填能或不能)
(3)该实验中,影响溶液颜色互变快慢的主要因素有。
(4)从上述变化的总结果看,葡萄糖的作用是 , 亚甲基蓝的作用是。
(5)上述实验中,葡萄糖也可用鲜橙汁代替,因为其中含丰富的维生素C,由此可推测维生素C具有性。
(6)该实验中③④的操作能否无限次重复进行(选填能或不能),理由是。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于物质的量的叙述中,正确的是
A.1mol任何物质都含有6.02×1023个分子B.0.012gC-12中约含有6.02×1023个碳原子
C.1mol水中含有2mol氢和1mol氧D.1molH2分子中含有2molH
查看答案和解析>>
科目: 来源: 题型:
【题目】铁及其化合物有重要用途,如聚合硫酸铁[Fe2(OH)n(SO4)3-n/2]m是一种新型高效的水处理混凝剂,而高铁酸钾(其中铁的化合价为+6)是一种重要的杀菌消毒剂,某课题小组设计如下方案制备上述两种产品:

请回答下列问题:
(1)若A为H2O(g),可以得到Fe3O4,写出H2O的电子式:________________。
(2)若B为NaClO3与稀硫酸,写出其氧化Fe2+生成Fe3+的离子方程式___________________。
(3)若C为KNO3和KOH的混合物,写出其与Fe2O3加热共熔制得高铁酸钾的化学方程式,并配平:___________
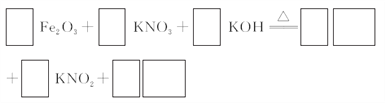
(4)为测定溶液Ⅰ中铁元素的总含量,实验操作如下:准确量取20.00 mL溶液Ⅰ于带塞锥形瓶中,加入足量H2O2,调节pH<3,加热除去过量H2O2;加入过量KI充分反应后,再用0.1 00 0 mol·L-1 Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00 mL。
已知:2Fe3++2I-===2Fe2++I2 ;I2+2S2O![]() ===2I-+S4O
===2I-+S4O![]() 。
。
①写出滴定选用的指示剂________,滴定终点观察到的现象_______________________。
②溶液Ⅰ中铁元素的总含量为__________g·L-1。若滴定前溶液中H2O2没有除尽,所测定的铁元素的含量将会________(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如图所示的实验装置,通过测量反应产生的CO2和H2O的质量,来确定该混合物中各组分的质量分数。
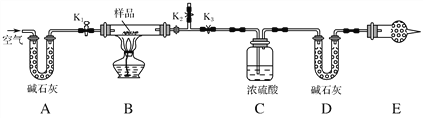
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是_________。
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是________________。
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为_________________________________________。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是___________________。
②E处干燥管中盛放的药品是________,其作用是__________________ ________________,如果实验中没有该装置,则会导致测量结果NaHCO3的质量________(填“偏大”、“偏小”或“无影响”)。
③若样品质量为w g,反应后C、D装置增加的质量分别为m1 g、m2 g,则混合物中Na2CO3·10H2O的质量分数为________(用含w、m1、m2的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法及对应化学方程式或离子方程式正确的是( )
A. 用二氧化硅和水反应可制得硅酸:SiO2+H2O=H2SiO3
B. 食醋与蛋壳反应:CaCO3+2H+=Ca2++CO2↑+H2O
C. 铁在氯气中燃烧:Fe+Cl2=FeCl2
D. 84消毒液与洁厕灵混合可能产生毒气:ClO-+Cl-+2H+=Cl2↑H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】.实验室用下列有关装置先制取干燥、纯净的氯气,后进行有关性质实验。试回答下列问题。
(1)上述装置中各仪器从左至右的连接顺序为接接接接接接。
(2)E装置的作用是 , G装置的作用是 , D中的现象为 , B中的现象为
。
(3)写出下列反应的离子方程式:B中 , G中。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯气的制取及其性质的微型实验: ①用滤纸剪成四个适当大小的长方形,然后将这些滤纸都用凡士林粘在集气瓶内部。
②将饱和NaI、NaBr、Na2S、品红溶液(1~2滴)滴在如图所示的滤纸上。
③向集气瓶内加1.5 g KClO3 , 用滴管吸取约2 mL浓盐酸,然后将滴管装在双孔塞上,最后把该双孔塞塞在集气瓶上,如图所示。
④用滴管向漏斗中加NaOH溶液,注意所加NaOH溶液应以刚好装满漏斗下端的弯管处为宜(NaOH溶液在此起液封作用同时又有减压功能)
⑤挤压胶头滴管向集气瓶中加浓盐酸。
⑥整个现象看完后,用滴管向漏斗中加NaOH溶液吸收尾气。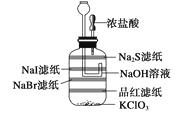
(1)该实验的主要现象: ;
(2)该实验的化学方程式:。
查看答案和解析>>
科目: 来源: 题型:
【题目】将一小块钠投入到盛有100mL硫酸铜溶液的烧杯里,不可能观察到的现象是( )
A.钠熔成小球并在液面上四处游动B.有气体产生
C.烧杯底部有红色的物质生成D.溶液有蓝色沉淀生成
查看答案和解析>>
科目: 来源: 题型:
【题目】锰酸锂(LiMn2O4)可作为锂离子电池的正极材料.工业上利用软锰矿浆吸收含硫烟气(SO2 和O2)制备锰酸锂,生产流程如图1: 
已知:①软锰矿主要成分为MnO2 , 含少量Fe2O3、FeO、Al2O3、SiO2等杂质.
②软锰矿浆在吸收含硫烟气的过程中酸性逐渐增强.
③部分氢氧化物沉淀相关的溶液pH如表一:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 3.4 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 4.7 | 9.8 |
(1)已知:(图2)表二 表二
实验序号 | SO2浓度(gm﹣3) | 烟气流速(mLmin﹣1) |
① | 4.1 | 55 |
② | 4.1 | 96 |
下列措施可提高SO2吸收率的是(填序号)
a.降低通入含硫烟气的温度 b.升高通入含硫烟气的温度
c.减少软锰矿浆的进入量 d.减小通入含硫烟气的流速
(2)加入试剂X能提高产品纯度,则X可以是(填化学式)
(3)加氨水调溶液pH在5~6之间,目的是 .
(4)锰酸锂可充电电池(图3)的总反应式为:Li1﹣xMnO4+LixC ![]() LiMnO4+C(x<1) ①放电时,电池的正极反应式为
LiMnO4+C(x<1) ①放电时,电池的正极反应式为
②充电时,若转移1mole﹣ , 则石墨电极将增重g.
查看答案和解析>>
科目: 来源: 题型:
【题目】根据反应:2H2S+O2=2S↓+2H2O,4NaI+O2+2H2SO4=2I2+2Na2SO4+2H2O,Na2S+I2=2NaI+S↓,下列物质的氧化性强弱判断正确的是
A. O2>I2>S B. H2S>NaI>H2O
C. S>I2>O2 D. H2O>NaI>H2S
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com