
科目: 来源: 题型:
【题目】物质A-J间的转化关系如图所示,A、C为金属氧化物,其中A 为红棕色粉末,B、D是生活中常见金属单质,F、J是难溶于水的白色化合物,G、J受热后容易分解。
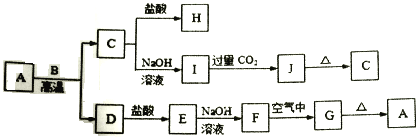
(1)A 的化学式是________________;
(2)I→J 反应的离子方程式是_______________________________;
(3)F转化为G的过程中观察到的现象是__________________________,反应的化学方程式是___________________________;
(4)检验E 中主要阳离子的方法________________________________;
查看答案和解析>>
科目: 来源: 题型:
【题目】为验证Cl2、Fe3+、I2三者氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器己略去,气密性已检验)。
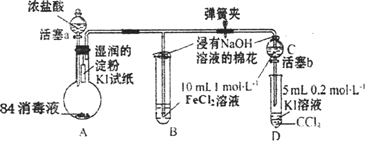
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.向B中加入一定量KSCN溶液,混合液显红色,一段时间后,B中溶液红色加深,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,写出A中发生反应的离子方程式________。
(2)验证氯气的氧化性强于碘单质的实验现象是________。
(3)B中溶液发生反应的离子方程式是________。
(4)为验证Fe3+的氧化性强于碘单质,过程Ⅳ的操作和现象是________,对应反应的离子方程式是________。
(5)浸有氢氧化钠溶液的棉花作用是________。
(6)过程Ⅲ实验的目的是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将由a mol NaHCO3和b mol NaOH组成的固体混合物放在密闭容器中加热到250℃,经充分反应后,排出气体,冷却后,称量残留固体的质量为W g,试计算W的值可能为( )
①84a+40b ②53a+40b ③66a+40b ④53(a+b)
A.①②
B.②④
C.只有④
D.③④
查看答案和解析>>
科目: 来源: 题型:
【题目】已知氢化锂固体不导电,隔绝空气熔融时能导电,它跟水反应能生成氢气.下列有关氢化锂的说法中,错误的是( )
A.LiH是离子晶体
B.LiH的水溶液呈酸性
C.LiH是一种氧化剂
D.LiH中H﹣半径大于Li+半径
查看答案和解析>>
科目: 来源: 题型:
【题目】把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡.则原混合溶液中钾离子的浓度为( )
A.![]() mol?L﹣1
mol?L﹣1
B.![]() mol?L﹣1
mol?L﹣1
C.![]() mol?L﹣1
mol?L﹣1
D.![]() mol?L﹣1
mol?L﹣1
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学通过以下装置测定M样品(只含Fe、Al、Cu) 中各成分的质量分数。取两份质量均为mg的M样品,按实验1(如图1)和实验2(如图2)进行实验,该同学顺利完成了实验并测得气体体积分别为V1mL和V2 mL(已折算到标准状况下)。
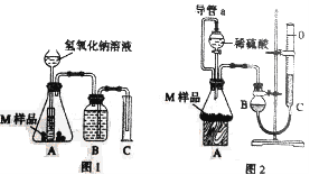
(1)写出实验1中可能发生反应的离子方程式:________________________;
(2)M样品中铜的质量的数学表达式为(用V1和V2表示):_________________________。
(3)实验1进行实验前,B瓶中水没有装满,使测得气体体积________________________。(填“偏大”、“偏小”或“无影响”,下同);若拆去实验2中导管a,使测得气体体积___________________。
(4)该实验需要0.50 mol·L-1的NaOH溶液470mL,配制时应用托盘天平称量______________gNaOH 。
(5)该实验中所用稀硫酸是用98%的浓硫酸(ρ=1.84g/cm3) 配制的,欲用该浓硫酸配制成浓度为0.5 mol/L的稀硫酸100mL。
①所需仪器除烧杯、玻璃棒外还需______________、______________、______________。
②所取浓硫酸的体积为_________mL。
下列操作引起所配溶液浓度偏高的是________________
A.取浓硫酸时俯视 B.在烧杯中稀释浓硫酸后,立即转移
C.定容时俯视 D.颠倒摇匀后发现液面低于刻度线,但未加水至刻度线
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化还原反应原理在化学中有广泛的运用,比如可以用酸性高锰酸钾溶液来测定双氧水的浓度。已知该反应中MnO4-只发生如下过程:MnO4-→Mn2+
(1)该反应中还原剂是_________________;
(2)写出该反应的离子方程式________________________________;
(3)如果反应中转移了0.5mol电子,则产生的气体在标准状况下的体积为____________L。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述中正确的是( )
A.化学键是分子间的强烈的相互作用
B.离子键是阴、阳离子间的强烈的相互作用
C.共价键只存在于非金属元素的原子之间
D.共价键一定只存在于共价化合物中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com