
科目: 来源: 题型:
【题目】有关锌-稀硫酸-铜构成的原电池的一些说法中,正确的是( )
A. 锌片为正极,且锌片逐渐溶解
B. 铜片为负极,且铜片上有气泡
C. 溶液中的H+移向铜极
D. 该电池工作的过程中溶液的酸性始终不变
【答案】C
【解析】A、较活泼的金属锌作负极,选项A错误;B、较活泼的金属锌作负极,较不活泼的金属铜作正极,正极上氢离子得电子生成氢气,所以铜片上有气泡生成,选项B错误;C、原电池中阳离子H+移向正极铜电极,选项C正确;D、负极上锌失电子生成锌离子进入溶液,正极上氢离子得电子生成氢气析出,所以一段时间后溶液中H+浓度降低,酸性减弱,选项D错误。答案选C。
【题型】单选题
【结束】
25
【题目】近几年科学家发明的一种新型可控电池——锂水电池,工作原理如图所示。下列有关说法不正确的是( )

A. 石墨极发生的反应是2H2O+2e— === H2↑+2OH—
B. 有机电解质和水溶液不可以互换区域
C. 该装置不仅可提供电能,还可得到清洁的氢气
D. 标准状况下产生22.4 L的氢气时,正极消耗锂的质量为14 g
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,浓度均为1.0molL﹣1的NH3H2O和NH4Cl混合溶液10mL,测得其pH为9.3.下列有关叙述正确的是( )
A.加入适量的NaCl,可使c(NH4+)=c(Cl﹣)
B.滴加几滴浓氨水,c(NH4+)减小
C.滴加几滴浓盐酸, ![]() 的值减小
的值减小
D.1.0 molL﹣1的NH4Cl溶液中c(NH4+)比该混合溶液大
查看答案和解析>>
科目: 来源: 题型:
【题目】
(1)第一电离能介于B、N之间的第二周期元素有种.
(2)CH4中共用电子对偏向C,SiH4中硅元素为+4价,则C、Si、H的电负性由大到小的顺序为。
(3)Fe3C晶体中碳元素为-3价,则其中基态铁离子的电子排布式为。
(4)甲醇(CH3OH)分子内的O-C-H键角(填“大于”、“等于”或“小于”)甲醛(H2C=O)分子内的O-C-H键角。
(5)BF3和NF3都是四个原子的分子,BF3分子的立体构型是平面三角形,而NF3分子的立体构型是三角锥形的原因是。
(6)测定大气中PM2.5的浓度方法之一是β-射线吸收法,β-射线吸收法可用85Kr.Kr晶体为面心立方晶体,若晶体中与每个Kr原子相紧邻的Kr原子有m个,晶胞中含Kr原子为n个,则 ![]() =(填数字)。已知Kr晶体的密度为ρg/cm3 , 摩尔质量为Mg/mol,阿伏加德罗常数用NA表示,列式表示Kr晶胞参数a=_nm。
=(填数字)。已知Kr晶体的密度为ρg/cm3 , 摩尔质量为Mg/mol,阿伏加德罗常数用NA表示,列式表示Kr晶胞参数a=_nm。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.某工厂的工业废水中含有大量的FeSO4和较多的Fe3+和Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。实验室模拟该工业流程如图:
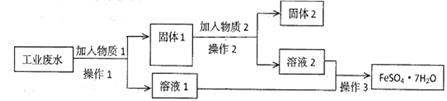
(1)检验废水中的Fe2+,实验室中用酸性KMnO4溶液检验,发生反应的离子方程式为________________________。
(2)加入过量物质1后,发生反应的离子方程式为___________________________。
(3)固体2是_____________________,实验室为长期保存硫酸亚铁溶液往往向其溶液中加入_______________________。
Ⅱ.工业上冶炼铝的原料是铝土矿(主要成分是Al2O3,杂质为Fe2O3、FeO、SiO2等)。某研究小组设计的提纯Al2O3的方案如下:

(1)加入过量的NaOH溶液,过滤后的滤液中含有的溶质有________(填化学式)。
(2)加入过量NaOH溶液过滤后,若滤渣中Fe(OH)2也被氧化,写出其被氧化的化学方程式__________________________。
(3)写出通入过量CO2生成沉淀A时反应的离子方程式为_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有关氧化还原反应的叙述正确的是( )
A.氧化还原反应的实质是电子的转移(得失或偏移)
B.氧化还原反应的实质是元素化合价的升降
C.氧化还原反应的实质是有氧元素的得失
D.物质所含元素化合价升高的反应是还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与环境保护、社会可持续发展密切相关,下列说法或做法合理的是( )
A. 将地沟油回收加工为生物柴油,提高资源的利用率
B. 进口国外电子垃圾,回收其中的贵重金属
C. 洗衣粉中添加三聚磷酸钠,增强去污效果
D. 大量生产超薄塑料袋,方便人们的日常生活
查看答案和解析>>
科目: 来源: 题型:
【题目】纳米级Cu2O是优良的催化剂和半导体材料,工业上常用下列方法制备Cu2O。
(1)热还原法
加热条件下,用液态肼(N2H4)还原新制的Cu(OH)2制备Cu2O,同时放出N2。该反应的化学方程式为。
(2)电解法 以氢氧燃料电池为电源,用电解法制备Cu2O的装置如图。
①A的化学式为。
②燃料电池中,OH-的移动方向为(填“由左向右”或“由右向左”);电解池中,阳极的电极反应式为。
③电解一段时间后,欲使阴极室溶液恢复原来组成,应向其中补充一定量 (填化学式)。
④制备过程中,可循环利用的物质为(填化学式)。
(3)干法还原法
利用反应Cu +CuO ![]() Cu2O制备Cu2O。将反应后的均匀固体混合物(含有三种成分)等分为两份,一份与足量H2充分反应后,固体质量减少6.4g;另一份恰好溶于500mL稀硝酸,生成标准状况下4.48LNO,该稀硝酸的物质的量浓度为。
Cu2O制备Cu2O。将反应后的均匀固体混合物(含有三种成分)等分为两份,一份与足量H2充分反应后,固体质量减少6.4g;另一份恰好溶于500mL稀硝酸,生成标准状况下4.48LNO,该稀硝酸的物质的量浓度为。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com