
科目: 来源: 题型:
【题目】某有机物结构简式为 ![]() ,下列叙述错误的是( )
,下列叙述错误的是( )
A.1 mol 该有机物在加热和催化剂作用下,最多能和4 mol H2反应
B.该有机物能使溴水褪色,也能使酸性KMnO4溶液褪色
C.该有机物遇硝酸银溶液产生白色沉淀
D.该有机物在一定条件下能发生消去反应和取代反应
查看答案和解析>>
科目: 来源: 题型:
【题目】有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是( ) 
A.①为简单立方堆积②为六方最密堆积③为体心立方堆积④为面心立方最密堆积
B.每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个
C.晶胞中原子的配位数分别为:①6,②8,③8,④12
D.空间利用率的大小关系为:①<②<③<④
查看答案和解析>>
科目: 来源: 题型:
【题目】某含氧酸盐X的化学式为ABO3 ;已知在元素周期表中,A、B均为前四周期主族元素,且A位于B的下一周期。
(1)若常温下A、B的单质都能与水发生反应,且A的焰色反应为紫色。
①B在元素周期表中的位置是___________________。
②下列说法正确的是__________(填代号)。
a.A离子的半径大于B离子的半径
b.A、B元素的最高价氧化物对应的水化物都是强电解质
c.A单质与水反应后溶液的pH比B单质与水反应后溶液的pH大
③400℃时,X能发生分解反应生成两种盐,其物质的量之比为1:3,其中一种是无氧酸盐。该反应的化学方程式为_______________________________________________。
(2)若含氧酸盐X难溶于水,在空气中易氧化变质;且B元素原子的最外层电子数是其电子层数的2倍。已知X能快速消除自来水中的C1O—,则该反应的离子方程式为_____________
(3)若含氧酸盐X能与稀硫酸反应,生成无色、无味的气体。
①该气体的电子式为______________。
②X可用作防火涂层,其原因是:
a.高温下X发生分解反应时,吸收大量的热;b.________________________(任写一种)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. Fe(OH)3胶体带有正电荷,电泳实验时,阴极附近颜色加深
B. 用平行光照射NaCl溶液和Fe(OH)3胶体,无法将两者加以区分
C. 在Fe(OH)3胶体中滴加稀盐酸,胶体逐渐溶解
D. 含有FeCl3杂质的Fe(OH)3胶体,可以通过渗析提纯
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分,回答下列有关问题:
族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
4 | ⑩ |
(1)写出下列元素符号:④_______;________。
(2)画出原子的结构示意图:⑤_________;________。
(3)在①~元素中,金属性最强的元素是_________,非金属性最强的元素是_______,最不活泼的元素是________ (均填元素符号)。
(4)元素⑦与元素⑧相比,非金属性较强的是___(用元素符号表示),下列表述中能证明这一事实的是___(填序号)。
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)元素⑥是构成地壳的主要元素之一,其氧化物是现代光学及光纤制品的基本原料,该氧化物的化学式为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】2016年夏季奥运会将在“足球王国”﹣﹣巴西首都里约热内卢举行,如图酷似奥林匹克旗中的五环的一种有机物被称之为奥林匹克烃,下列说法正确的是( ) ![]()
A.该有机物属于芳香族化合物,是苯的同系物
B.该有机物中只含非极性键
C.该有机物的一氯代物有11种
D.该有机物完全燃烧生成H2O的物质的量小于CO2的物质的量
查看答案和解析>>
科目: 来源: 题型:
【题目】科学家常采用将药物连接在高分子载体上,制成缓释长效药物.已知某种解热镇痛类药物,其结构简式为A,把它连接到高分子聚合物B上,形成缓释长效药物C.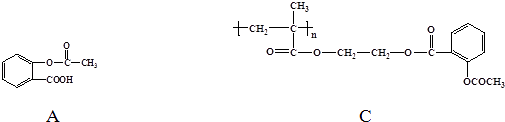
(1)分子聚合物B的结构简式为 .
(2)A与B反应生成C的有机反应类型是 .
(3)A可水解成和(写结构简式).
查看答案和解析>>
科目: 来源: 题型:
【题目】A,B,C,D为常见气态单质.已知:①A和B可以在一定条件下发生化合反应,其产物还可以与B化合生成红棕色气体;②C分别与A、B反应生成的两种化合物分子中都含有10个电子;③C和D反应生成的化合物易溶于水,在其溶液中滴加AgNO3溶液,生成白色沉淀.请回答下列问题:
(1)A单质的电子式是 , C和D反应生成的化合物的电子式是 .
(2)上述②中化合物的热稳定性强于(填化学式).
(3)写出A与B反应的化学方程式: .
(4)将D通入B,C反应生成的化合物中,发生反应的离子方程式是 , C,D形成的化合物与AgNO3溶液反应的离子方程式为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组欲探究SO2和Cl2能否发生反应,设计如下图所示的实验装置进行实验。
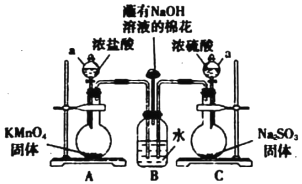
(1)图中仪器a的名称为_______。
(2)装置A中的反应为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,反应中的氧化剂是_____,生成71gCl2转移的电子是______mol。
(3)装置B中蘸有NaOH溶液的棉花的作用是______________。
(4)打开A、C装置a的活塞,一段时间后关闭活塞。待反应完全后.小组同学又继续做如下实验。
①甲同学取适量B中溶液于试管中,向其中滴加少量AgNO3溶液,有白色沉淀生成。甲同学由此认为SO2和Cl2,发生了反应,理由是该反应中生成了___________(填离子符号)。
②乙同学认为甲同学的结论不合理,认为A中生成的Cl2中混有杂质,应该在装置A、B间增加一个洗气瓶,然后再按甲同学的方法即可得到正确结论,乙同学认为Cl2中混有的杂质是_______,洗气瓶中盛有试剂的名称是____________。
③丙同学认为甲、乙两位同学的结论均不合理。丙同学取适量B中溶液于试管中,向其中滴加少量溶液X,有白色沉淀生成,得出结论即SO2与Cl2同时通入水中,可以发生反应。溶液X__________(填选项序号)。
a.BaCl2溶液 b.Ba(OH)2溶液 c.Ba(NO3)2溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρ g/cm3 , 溶质的质量分数为w,溶质的物质的量浓度为c mol/L.下列叙述中正确的是( )
①w= ![]() ×100%
×100%
②c= ![]()
③向上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w.
A.①③
B.②③
C.①②
D.只有②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com