
科目: 来源: 题型:
【题目】按要求填空
(1)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈(填“酸性”,“中性”或“碱性”,下同),溶液中c(Na+)c(CH3COO﹣)(填“>”或“=”或“<”,下同).
(2)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈 , 醋酸体积氢氧化钠溶液体积.
(3)将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后溶液的pH=7,则醋酸溶液中c(H+)氢氧化钠溶液中c(OH﹣),m与n的大小关系是mn.
(4)用标准的NaOH滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是 .
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E.未用标准液润洗碱式滴定管.
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下,下列叙述正确的是( )
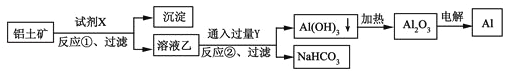
A. 试剂X氢氧化钠溶液
B. 反应①、过滤后所得沉淀为红褐色Fe2O3
C. 图中所示转化反应都不是氧化还原反应
D. 反应②的化学方程式为2NaAlO2+CO2+3H2O=2Al(OH)3↓+Na2CO3
查看答案和解析>>
科目: 来源: 题型:
【题目】下列对实验操作及结论的描述不正确的是( )
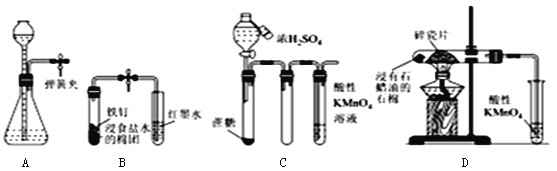
A. 夹紧弹簧夹,由长颈漏斗加水至产生液面差,一段时间后液面差不变,说明气密性良好
B. 打开弹簧夹,红墨水倒吸入导气管中,说明铁钉发生了吸氧腐蚀
C. 滴加浓硫酸后,高锰酸钾溶液褪色,说明浓硫酸使蔗糖脱水的同时还产生了二氧化硫
D. 加热片刻后高锰酸钾溶液褪色,说明石蜡油分解产生了乙烯
查看答案和解析>>
科目: 来源: 题型:
【题目】下列是某兴趣小组根据教材实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验.请观察如图所示实验装置,分析实验原理,并判断下列说法和做法,其中不科学的( )
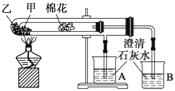
A. 甲为小苏打,乙为纯碱
B. 要证明碳酸氢钠受热能产生水,可在小试管内塞上沾有无水硫酸铜粉末的棉花球
C. 加热不久就能看到A烧杯的澄清石灰水变浑浊
D. 整个实验过程中都没有发现A烧杯的澄清石灰水变浑浊
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物H是一种有机光电材料中间体.实验室由芳香化合物A制备H的一种合成路线如下: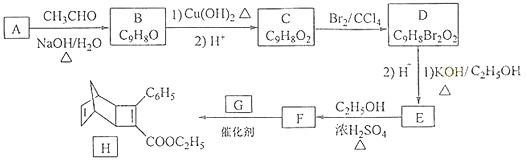
已知:①RCHO+CH3CHO ![]() RCH=CHCHO+H2O
RCH=CHCHO+H2O
② ![]() +
+ ![]()
![]()
![]()
回答下列问题:
(1)A的化学名称为为 .
(2)由C生成D和E生成F的反应类型分别为、 .
(3)E的结构简式为 .
(4)G为甲苯的同分异构体,由F生成H的化学方程式为 .
(5)芳香化合物X是F的同分异构体,X能与饱和碳酸氢钠溶液反应放出CO2 , 其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6:2:1:1,写出2种符合要求的X的结构简式 .
(6)写出用环戊烷和2﹣丁炔为原料制备化合物 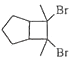 的合成路线(其他试剂任选).
的合成路线(其他试剂任选).
查看答案和解析>>
科目: 来源: 题型:
【题目】物质爆炸都伴随着能量变化,请回答下列问题:
(1)氯酸钾、火药及磷等组成的混合物极易爆炸。由于KClO3受热分解释放出O2,引发白磷(P4,固体)的燃烧而导致火药爆炸。31 g P4完全燃烧生成五氧化二磷固体释放出a kJ热量。下列说法不正确的是________ (填字母)。
A.KClO3的分解过程中只有共价键断裂没有共价键生成
B.火药爆炸会使周围空气体积迅速膨胀
C.若白磷完全燃烧释放出8a kJ热量,则需要标准状况下的O2体积为224 L
D.易燃易爆物应远离火源
(2)天然气已经成为我国主要的民用清洁能源,但天然气与空气混合达到一定比例后遇明火会发生爆炸,所以安全使用天然气,防止发生爆炸是极为重要的。已知天然气的主要成分甲烷燃烧时的能量变化如图所示。
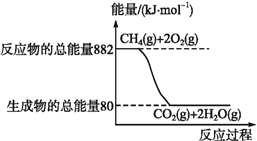
请回答下列问题:
①下列说法正确的是____(填字母)。
A.天然气属于清洁能源,所以它属于新能源
B.甲烷完全燃烧时化学能全部转化为热能
C.标准状况下44.8 L甲烷完全燃烧时有8 mol共价键断裂
D.用天然气做饭时,为使甲烷充分燃烧,通入的空气越多越好
②CH4(g)完全燃烧时生成18 g气态水放出的热量是____kJ。
③若家庭做饭需64160 kJ热量,假设天然气(按CH4算)的热效率为80%,则需要天然气(按CH4算)的质量为____g。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:Ksp(AgCl)=1.8×10﹣10 , Ksp(AgI)=1.5×10﹣16 , Ksp(Ag2CrO4)=2.0×10﹣12 , 则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是( )
A.AgCl>AgI>Ag2CrO4
B.AgCl>Ag2CrO4>AgI
C.Ag2CrO4>AgCl>AgI
D.Ag2CrO4>AgI>AgCl
查看答案和解析>>
科目: 来源: 题型:
【题目】某强酸性溶液中还可能存在Al3+、Fe2+、NH4+、Ba2+、Cl-、CO32-、SO42-、NO3-中的若干种,现取适量溶液进行如下一系列实验(已知硝酸根离子在酸性环境中具有强氧化性,还原产物一般为气体)

下列有关判断正确的是
A. 试液中一定有Fe2+、SO42-、H+、NH4+、Al3+
B. 试液中一定没有Ba2+、CO32-、NO3-
C. 步骤③中发生反应的离子方程式为:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
D. 沉淀B在空气中会迅速变为灰绿色,最后变为红褐色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com