
科目: 来源: 题型:
【题目】下列有关氧化还原反应的说法错误的是( )
A. 氧化剂得电子,还原剂失电子
B. 某元素从化合态到游离态,可能被氧化也可能被还原
C. 难失去电子的原子,不一定易得电子
D. 一种元素被氧化,一定有另一种元素被还原
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组为探究SO2的化学性质,设计了如下实验装置。
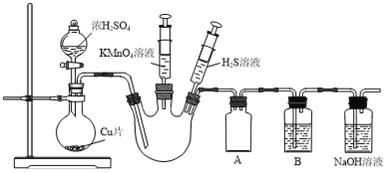
(1)该装置设计中存在的问题是___________________。
(2)装置A的作用是___________________。
(3)①当三颈烧瓶中充满SO2气体,证明SO2具有氧化性的实验操作及现象是___________________。
②若要证明SO2具有漂白性,可在洗气瓶B中加入___________________溶液。
(4)NaOH溶液用于吸收尾气中的SO2,由于空气氧化,溶液中可能会存在SO![]() ,检验溶液中是否存在SO
,检验溶液中是否存在SO![]() 的实验方法是___________________。
的实验方法是___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】物质的量之比为2:5的锌与稀硝酸恰好完全反应,若硝酸被还原的产物为N2O,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是
A. 1:4 B. 1:5 C. 2:3 D. 2:5
查看答案和解析>>
科目: 来源: 题型:
【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测和处理.某工厂对制铬工业污泥中Cr(Ⅲ)的回收与再利用工艺如下(硫酸浸液中金属离子主要是Cr3+ , 其次是Fe3+、Fe2+、Al3+、Ca2+、Mg2+): 
常温下部分阳离子的氢氧化物形成沉淀时溶液的pH见下表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Ca2+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.0 | 9.6 | 4.2 | 9.7 | |
沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8.0 | 11.7 | 9.0(>9.0 溶解) |
(1)酸浸时,为了提高浸取率可采取的措施是(至少一条).
(2)调pH=4.0是为了除去
(3)钠离子交换树脂的作用原理为Mn++nNaR→MRn+nNa+ , 被交换的杂质离子是
(4)试配平下列氧化还原反应方程式:Fe2++H2O2+H+═Fe3++
(5)通入SO2的目的是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】“84”消毒液是一种以NaClO为主的消毒剂,广泛应用于医院、食品加工、家庭等的卫生消毒。
(1)“84”消毒液中通入CO2能增强消毒效果,写出向“84”消毒液中通入过量CO2的离子方程式:___________________。
(2)测定“84”消毒液中NaClO的物质的量浓度的方法如下:
①配制100.00mL 0.5000 mol·L-1的Na2S2O3溶液。配制过程中需准确称取Na2S2O3固体___________________g,需要用到的玻璃仪器有烧杯、胶头滴管、量筒、___________________。
②准确量取10.00 mL消毒液于锥形瓶中,加入过量的KI溶液,用足量的乙酸酸化,充分反应后向溶液中滴加Na2S2O3溶液,完全反应时消耗Na2S2O3溶液25.00 mL。反应过程中的相关离子方程式为:
2CH3COOH+2I—+ClO—=I2+Cl—+2CH3COO—+H2O,I2+2S2O![]() =2I—+S4O
=2I—+S4O![]()
通过计算求出该“84”消毒液中NaClO的物质的量浓度。(写出计算过程)__________
查看答案和解析>>
科目: 来源: 题型:
【题目】由硫铁矿烧渣(主要含Fe2O3和SiO2)制备绿矾(FeSO4·7H2O),再通过绿矾制备铁矾[FeO(OH)]的流程如下:(已知FeS2和铁矾均难溶于水)
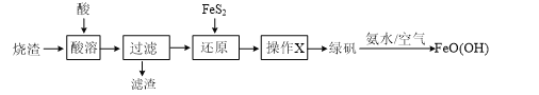
(1)“酸溶”步骤中,最好采用___________________(填“盐酸”、“硫酸”或“硝酸”)溶解烧渣。
(2)写出“还原”步骤发生反应的离子方程式:___________________。
(3)对“还原”后的溶液进行“操作X”,可得到绿矾。“操作X”是指___________________,过滤,洗涤,干燥。
(4)请补充完整检验“还原”后所得溶液中是否含有Fe3+的实验方案:取“还原”后溶液于试管内,___________________。
(5)最后一步制备铁矾的反应中,还生成一种可作化肥的物质,它的化学式为___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】满足下列条件的有机物的种类数正确的是
选项 | 有机物 | 条件 | 种类数 |
A |
| 该有机物的一氯代物 | 4 |
B | C6H12O2 | 能与NaHCO3溶液反应 | 3 |
C | C5H12O | 含有2个甲基的醇 | 5 |
D | C5H10O2 | 在酸性条件下会水解生成甲和乙,且甲、乙的相对分子质量相等 | 4 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】Cl2O是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物或还原剂接触会发生燃烧并爆炸。一种制取Cl2O的装置如图所示。

已知:Cl2O的熔点为-116℃,沸点为3.8 ℃;Cl2的沸点为-34.6℃;HgO+2Cl2=HgCl2+Cl2O。下列说法正确的是
A. 装置②、③中盛装的试剂依次是浓硫酸和饱和食盐水
B. 通干燥空气的目的是作氧化剂
C. 从装置⑤中逸出气体的主要成分是Cl2O
D. 装置④与⑤之间不用橡皮管连接,是为了防止橡皮管燃烧和爆炸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com