
科目: 来源: 题型:
【题目】下列化学实验事实及其结论都正确的是
选项 | 实验事实 | 结论 |
A | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体, | HNO3分解成了NO2 |
B | 向某溶液中加入2滴KSCN溶液,溶液不显红色。再向溶液中加入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
C | 取久置的Na2O2粉末,向其中滴加过量的盐酸,产生无色气体 | Na2O2没有变质 |
D | 取某溶液少量,加入盐酸酸化的氯化钡溶液,出现白色沉淀 | 该溶液中一定含有大量的SO |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】反应4A(g)+5B(g)4C(g)+6D(g) 在5L的密闭容器中进行反应,30min后,C的物质的量增加了0.30mol.下列叙述正确的是( )
A.30min中A的平均反应速率是0.010molL﹣1min﹣1
B.容器中D的物质的量一定增加了0.45mol
C.容器中A,B,C,D的物质的量的比一定是4:5:4:6
D.容器中A的物质的量一定增加0.30mol
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素,它们在一定条件下相互转化的关系如下图所示(部分反应中的H2O已略去)。请填空:

(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,则反应②的离子方程式为_______________________,由此判断实验室保存C的水溶液应加入____________(填试剂名称),3molD与足量水蒸气高温下充分反应转移的电子数为_______。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为______________________。
(3)若C是一种能形成硫酸型酸雨的污染性气体,D是一种能支持燃烧和呼吸的气体,则反应③中氧化产物和还原产物的质量比为______________。
(4)若D是一种常见的温室气体,A、B、C的的焰色反应都呈黄色,现有120gB和C的混合物,充分加热后测得剩余固体质量为89g,则混合物中B的质量分数为_______
查看答案和解析>>
科目: 来源: 题型:
【题目】已知I-、Fe2+、SO2和Cl-均有还原性,它们在酸性溶液中还原性的强弱顺序为SO2>I->Fe2+>Cl-,下列反应不可能发生的是( )
A. Cl2+SO2+2H2O=H2SO4+2HCl B. 2Cl-+2Fe3+=2Fe2++Cl2↑
C. 2Fe3++2I-=2Fe2++I2 D. 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B、C为中学化学中常见的单质。室温下,A为固体,B和C均为气体。在适宜的条件下,它们可以按如图进行反应。下列说法中正确的是

A. A、B、C中三种元素的任意两种元素形成的化合物所属物质类别可能是氧化物
B. A、B、C中三种元素的任意两种元素形成的化合物所属物质类别一定不是碱
C. 如果E溶液是一种强酸,则E溶液为硫酸
D. A、B、C中有一种金属且为B
查看答案和解析>>
科目: 来源: 题型:
【题目】在25℃的纯水中通入一定量的氯化氢,当溶液的pH=1时,则由水电离出的c(H+)是( )
A.1×10﹣1mol/L
B.1×10﹣6mol/L
C.1×10﹣3mol/L
D.1×10﹣13mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】已知在1×105Pa、298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是( )
A.H2O(g)=H2(g)+ ![]() O2(g);△H=+242kJmol﹣1
O2(g);△H=+242kJmol﹣1
B.2H2(g)+O2(g)+2H2O(l);△H=﹣484kJmol﹣1
C.H2(g)+ ![]() O2(g)=H2O(g);△H=+242kJmol﹣1
O2(g)=H2O(g);△H=+242kJmol﹣1
D.2H2(g)+O2(g)=2H2O(g);△H=﹣484kJmol﹣1
查看答案和解析>>
科目: 来源: 题型:
【题目】四氧化三铁(Fe3O4)的组成可表示为Fe2O3·FeO,下列说法不正确的是( )
A.四氧化三铁是一种混合物B.四氧化三铁是一种纯净物
C.四氧化三铁有固定的组成和结构D.四氧化三铁是一种黑色固体
查看答案和解析>>
科目: 来源: 题型:
【题目】铁是人类较早使用的金属之一。运用所学知识,回答下列问题。
(1)鉴别Fe(OH)3胶体和FeCl3溶液的方法是_____________________________。
(2)有一铁的氧化物样品,用5mol/L盐酸140mL恰好完全溶解,所得溶液还能吸收标况下560mL氯气,Fe2+全部变成Fe3+,则该样品中Fe 和O 的个数比为_____________。
(3)某研究性学习小组用Fe2(SO4)3溶液腐蚀绝缘板上的铜,制造印刷电路板,为测定Fe2(SO4)3腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则可检出待测液中含有的金属阳离子是_____;
②验证该溶液中含有Fe2+,正确的实验方法是__________(用字母代号填)。
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.取适量溶液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+
(4)工程师欲从制造印刷电路板的废水中回收铜,并获得FeCl3溶液,设计如下方案:
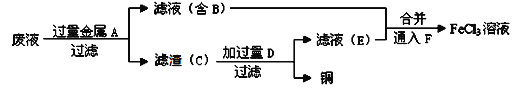
①滤渣C的主要成分的化学式为___________________________________。
②加过量D发生反应的离子方程为__________________________________。
③通入F发生反应的化学方程式为 __________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com