
科目: 来源: 题型:
【题目】常温向20mL 0.1mol·L-1氨水中滴加0.1mol·L-1盐酸,溶液pH随滴加盐酸溶液体积的变化如图2所示。下列说法正确的是

A. a点时,c(NH3·H2O)>c(C1-)>c(NH4+)>c(OH-)>c(H+)
B. a~b区域内c(NH4+)+c(NH3·H2O)=0.1mol·L-1
C. 当V(HC1)=10mL时,c(NH4+)-c(NH3·H2O)=2[c(OH-)-c(H+)]
D. 当V(HCl)=20mL时,c(H+)+c(C1-)>c(NH4+)+c(NH3·H2O)+c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,X原子核外最外层电子数是次外层的2倍,Y的氟化物YF3分子中各原子均达到8电子稳定结构,Z是同周期中原子半径最大的元素,W的最高正价为+7价。下列说法正确的是
A. 简单离子半径大小顺序: rX>rZ>rY
B. 元素W的氧化物对应水化物的酸性比Y的强
C. X与Y形成的原子晶体X3Y4的熔点比金刚石高
D. X与W形成的化合物和Z与W形成的化合物的化学键类型相同
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是温度和压强对X+Y2Z 反应影响的示意图.图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数.下列叙述正确的是( ) 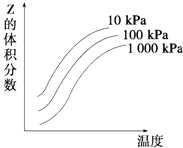
A.上述可逆反应的正反应为放热反应
B.X,Y,Z均为气态
C.X和Y中只有一种是气态,Z为气态
D.上述反应的正反应的△H>0
查看答案和解析>>
科目: 来源: 题型:
【题目】在检验用FeCl3溶液生产铜制印刷线路板后所得的废液成分的实验中,下列根据实验现象得出的结论不正确的是
A. 若用惰性电极电解该废液,阴极没有立即产生红色物质,说明废液中不含Cu2+
B. 若向废液中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明废液中含有C1-
C. 若向废液中加少量铁粉,充分反应后无固体剩余,说明废液中含有Fe3+
D. 若向废液中滴加KSCN 溶液,无现象,再加入氯水后溶液呈血红色,说明废液中含有Fe2+
查看答案和解析>>
科目: 来源: 题型:
【题目】除去下列物质中的杂质(括号内的物质),所使用的试剂和主要操作都正确的是( )
选项 | 物质 | 使用的试剂 | 主要操作 |
A | 乙醇(水) | 金属钠 | 蒸馏 |
B | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 分液 |
C | 苯(苯酚) | 浓溴水 | 过滤 |
D | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸镁晶体(MgSO4·7H2O)是一种重要的化工原料。以菱镁矿(主要成分是MgCO3,含少量FeCO3和不溶性杂质)为原料制取硫酸镁晶体的流程如下:

(1)MgCO3溶于稀硫酸的离子方程式是_________________________。
(2)加入H2O2溶液的目的是____________________(用离子方程式表示)。
(3)已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
阳离子 | Mg2+ | Fe2+ | Fe3+ |
开始沉淀 | 9.1 | 7.6 | 1.9 |
完全沉淀 | 11.1 | 9.7 | 3.2 |
“沉淀”步骤中,用氨水调节溶液pH的范围是______________________________。
(4)“过滤”所得滤液中存在大量的阳离子有Mg2+、____________。
(5)“结晶”步骤中需蒸发浓缩滤液,使用的仪器有铁架台、酒精灯和_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国政府为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾。检验食盐中是否加碘,可利用如下反应:
KIO3+ KI+ H2SO4═ K2SO4+ I2 + H2O
(1)配平该方程式,并且用双线桥法表示该方程式电子转移的方向与数目:____________________
(2)该反应中氧化剂和还原剂的物质的量之比为______________;
(3)如果反应中转移0.5mol电子,则生成I2的物质的量为____________;
查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实,不能用勒夏特列原理解释的是( )
A.氨水中加酸,NH ![]() 的浓度增大
的浓度增大
B.合成氨工业中不断从反应混合物中液化分离出氨气
C.实验室中常用排饱和食盐水的方法收集Cl2
D.合成氨控制在500℃左右的温度
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关说法不正确的是
A. 在氨水中加入少量的水或氯化铵固体后,都能使溶液中的c(NH4+) 减小
B. 相同体积、pH均为3的HA和HB两种酸分别与足量的锌充分反应,HA放出的氢气多,说明HB 的酸性比HA 的酸性强
C. 工业电解食盐水中,电解池被阳离子交换膜隔成阴极室和阳极室,目的是避免阳极产生的气体与烧碱反应
D. 在等浓度的NaCl 和Na2CrO4稀溶液中滴加AgNO3溶液,先析出AgCl 沉淀,则Ksp(AgCl)![]() Ksp(Ag2CrO4)
Ksp(Ag2CrO4)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com